Foram encontradas 35.933 questões.
A aromaterapia tem sido muito utilizada como alternativa para o tratamento dos sintomas da ansiedade. Dentre vários óleos essenciais conhecidos, o óleo de lavanda é um dos mais aplicados, sendo o acetato de linalila o seu principal componente. Considerando que cada sessão de tratamento necessita de uma solução 1.0 mol.L-1 em 2 mL de solvente, qual a massa de acetato de linalina (em miligramas) necessária para sua preparação?
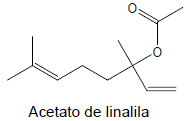
Dados: Massas molares em g.mol-1: H = 1; C = 12; O = 16.
Provas
Os elementos da família dos halogênios são largamente aplicados na medicina por serem mais reativos que outros ametais. Dentre os halogênios encontrados na natureza, qual deles apresenta maior raio atômico?
Provas
O bromato de potássio é um sal utilizado em pães para o fortalecimento das cadeias de glúten, proporcionando retenção de gases, umidade e melhor textura para pães do tipo francês. Se utilizado em excesso, pode ser nocivo à saúde humana. A sua produção envolve uma reação entre um ácido e uma base. Quais são o ácido e a base, respectivamente, aplicados na produção do bromato de potássio?
Provas
- Química InorgânicaSubstância e mistura: substância simples, substância composta e mistura. Alotropia
O granito é uma rocha magmática composta essencialmente por quartzo, mica e feldspato. É encontrado em placas continentais da crosta terrestre. Dado que é possível separar um mineral dos demais, é possível classificar o granito como uma:
Provas
O dióxido de nitrogênio (NO2) é um gás altamente oxidante; quando liberado na atmosfera pode reagir com a água, formando o ácido nítrico, que é um dos componentes da chuva ácida. Nas condições normais de temperatura e pressão, um mol de NO2 ocupa um volume de 22,4 L. Nas mesmas condições, uma massa de 460 g de NO2 ocuparia qual volume em litros?
Dados: Massas molares em g.mol-1: N = 14; O = 16.
Provas
No organismo, o fósforo possui diversas funções de extrema importância, sendo encontrado em membranas celulares, na estrutura de ossos e dentes e em atividades metabólicas. Em 100 g de uma amostra de leite desnatado em pó, foi encontrada uma massa de 1,6 g de fósforo. Considerando a dissolução total da massa de leite em pó em 100 mL de água, qual a concentração molar (mol.L-1) de fósforo na solução?
Dados: Massas molares em g.mol-1: P = 40.
Provas
O monóxido de carbono (CO) é uma substância altamente tóxica, porque se combina com a hemoglobina com afinidade 200 vezes maior que o O2, gerando a carboxiemoglobina. A reação de transformação do monóxido de carbono no dióxido de carbono (CO2) está descrita abaixo.
CO(g) + 1/2 O2(g) → CO2(g)
A reação ocorre em etapa única e de acordo com a reação acima, com constante de velocidade (k) igual a 0,5 L1/2.mol-1/2.min-1. Em uma situação em que a concentração de CO e O2 sejam 2,0 e 4,0 mol.L-1, respectivamente, a velocidade de reação, em mol.L-1∙min-1 será igual a:
Provas
O elemento tálio é extensivamente aplicado em inovações tecnológicas, e seu isótopo 201Tl é aplicado como contraste em exames médicos. Seu tempo de meia vida é de aproximadamente 72 horas. Dada uma massa inicial 128 mg, qual a massa (em mg) esperada de 201Tl após 15 dias?
Provas
O ácido periódico é um importante reagente para reação com polissacarídeos neutros. Sua reação com o hidróxido de sódio gera o periodato de sódio e água, como produtos. Qual é a fórmula molecular do periodato de sódio?
Provas
A sílica gel é aplicada no dia a dia para absorver umidade, impedindo a proliferação de fungos, mofos e ferrugem. Para identificação da umidade, a sílica gel apresenta complexos de cobalto em sua composição. Em uma situação de equilíbrio, a sílica gel apresenta coloração azul na ausência de água, e coloração rosa na presença de água. A equação da reação está representada abaixo:
[CoCl4]2- (aq) + 6 H2O(l) !$ \rightleftharpoons !$ [Co(H2O)6]2+ (aq) + 4 Cl- (aq)
Com relação ao equilíbrio químico, entre os complexos de cobalto, foram realizadas as seguintes afirmações:
1) Ao aquecer a sílica para eliminar a água presente, o equilíbrio é deslocado para o sentido dos reagentes;
2) Ao adicionar mais íons cloreto, o equilíbrio é deslocado para o sentido da formação dos produtos;
3) A formação do [CoCl4]2- (azul) indica a presença de umidade na sílica.
Está(ão) correta(s) a(s) afirmativa(s):
Provas
Caderno Container