Foram encontradas 35.933 questões.
Na comemoração pela sua aprovação no vestibular, um estudante ingeriu um total de 1 L de néctar de frutas, que contém 18 g de glicose (C6H12O6) a cada 100 mL de néctar. A reação não-balanceada do metabolismo da glicose está representada abaixo:
C6H12O6(aq) + O2(g) → CO2(g) + H2O(l)
De acordo com as entalpias de reação descritas abaixo:
1) 6 C(s) + 6 H2(g) + 3 O2(g) → C6H12O6(aq)
(!$ Δ !$H = -1.263 kJ.mol-1)
2) H2(g) + 1/2 O2(g) → H2O(l) (!$ Δ !$H = -286 kJ.mol-1)
3) CO2 → C(s) + O2(g) (!$ Δ !$H = 394 kJ.mol-1)
Qual a energia liberada após o metabolismo da glicose ingerida pelo estudante, em kJ? Dados: Massas molares em g·mol-1: H = 1; C = 12; O = 16.
Provas
Uma forma de reduzir o impacto do gás carbônico (CO2) para a vida na terra, uma vez que é um dos maiores contribuintes para as mudanças climáticas globais, é sua captura e armazenamento. Em contato com a água, o CO2 pode reagir e formar os seguintes equilíbrios químicos:
(reação 1) CO2(g) + H2O(l)!$ \leftrightharpoons !$ H2CO3(aq)
(reação 2) H2CO3(aq) + H2O(l)!$ \leftrightharpoons !$ H3O+ (aq) + HCO3 – (aq)
(reação 3) HCO3 – (aq) + H2O(l)!$ \leftrightharpoons !$ H3O+ (aq) + CO3 2– (aq)
Acerca do caráter ácido-base das espécies envolvidas, foram realizadas as seguintes afirmações:
1) Na reação 1, a água comporta-se como um ácido de Arrhenius;
2) Na reação 2, segundo a teoria de Br⌀nsted- Lowry, a água é um ácido e o H3O+ é sua base conjugada;
3) O H2CO3 é um ácido de Br⌀nsted-Lowry.
Está(ão) correta(s) a(s) afirmativa(s):
Provas
As pilhas recarregáveis de níquel-cádmio (NiCd) foram inventadas no século 19. Entre as tecnologias de baterias recarregáveis, a de NiCd rapidamente perdeu participação no mercado para as baterias NiMH e Liion, devido à sua capacidade inferior e ao impacto ambiental causado pelo descarte deste material no meio ambiente. De acordo com os potenciais, padrões de redução descritos abaixo para as reações que ocorrem na pilha NiCd:
NiO(OH) + H2O + e− → Ni(OH)2 + OH− E° = +0,49 V
Cd(OH)2 + 2e− → Cd + 2OH − E° = -0,81 V
Qual é a variação de potencial (!$ Δ !$E°) desenvolvido por esta pilha?
Provas
A naftalina é um produto comercial tóxico, utilizado no combate a insetos, como traças, moscas, formigas etc. O seu odor é percebido à temperatura ambiente, o que possibilita o afastamento dos insetos do local em que essa substância está presente. A naftalina possui ponto de fusão de 80°C e ponto de ebulição de 218°C. É correto afirmar que o fenômeno físico que permite a aplicação da naftalina no combate a insetos é:
Provas
O óxido de titânio (IV), TiO2, apresenta uma grande variedade de aplicações. Na indústria alimentícia, é usado como corante alimentar em pastilhas, gelados brancos e até no leite. Esse óxido pode ser produzido pela reação:
TiCl4(g) + 2 H2O(g) → TiO2(s) + 4 HCl(g)
Calcule o ΔHrº para esta reação conhecendo as entalpias de formação:
ΔH fº (TiCl4,g) = –763 kJ.mol–1; ΔHfº (TiO2,s) = –945 kJ.mol–1
ΔHfº (H2O,g) = –242 kJ.mol–1; ΔHfº(HCl,g) = –92 kJ.mol–1;
Provas
As pilhas de lítio-iodo possuem o formato de moedas pequenas e foram desenvolvidas, principalmente, para serem usadas em marca-passos cardíacos, já que são bem leves, seguras (não liberam gases), têm boa durabilidade (cerca de 8 a 10 anos) e fornecem uma voltagem de 2,8 V. Os eletrodos são formados por lítio e um complexo de iodo, que ficam separados por uma camada cristalina de iodeto de lítio que permite a passagem da corrente elétrica.
A reação que ocorre numa bateria de lítio-iodo é representada pela equação:
2 Li(s) + I2(s) → 2 LiI(s)
Analisando a reação redox acima, é correto afirmar que:
Provas
A ritalina é uma anfetamina prescrita para adultos e crianças portadores de transtorno de déficit de atenção e hiperatividade. Tem o objetivo de melhorar a concentração, diminuir o cansaço e acumular mais informação em menos tempo. Sabendo que a ritalina apresenta a seguinte fórmula estrutural:
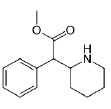
é correto afirmar que este composto possui os grupos funcionais:
Provas
A dopamina é um neurotransmissor da família das catecolaminas. Essa substância está envolvida no controle de movimentos, aprendizado, humor, emoções, cognição, sono e memória. A desregulação da dopamina no organismo está relacionada a transtornos neuropsiquiátricos, como ‘Mal de Parkinson’. Sabendo que a dopamina apresenta a seguinte fórmula estrutural:
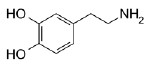
Três afirmações foram feitas:
1) Segundo a nomenclatura IUPAC, o nome da
dopamina é 3-(2-aminopropil) benzeno-1,2-diol.
2) A dopamina é um composto aromático.
3) A dopamina apresenta três ligações !$ π !$.
Está(ão) correta(s) a(s) afirmativa(s):
Provas
O ácido úrico está entre as substâncias naturalmente produzidas pelo nosso organismo. Ele é formado pela quebra das moléculas de purina (proteína contida em muitos alimentos) por ação da enzima xantina oxidase. Depois de utilizadas, as purinas são degradadas e transformadas em ácido úrico. Sabendo que o ácido úrico apresenta a seguinte fórmula estrutural:
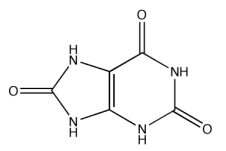
Três afirmações foram feitas:
1) Todos os carbonos da estrutura do ácido úrico têm hibridização sp2.
2) A molécula do ácido úrico possui, no total, 13 ligações !$ σ !$ e 3 ligações !$ π !$.
3) Na estrutura do ácido úrico, podemos identificar apenas um carbono terciário.
Está(ão) correta(s) a(s) afirmativa(s):
Provas
O aspartame é um adoçante muito utilizado para substituir o açúcar. No entanto, ele não deve ser utilizado em receitas de bolo, porque se decompõe em temperaturas elevadas, gerando fenilalanina, aspartato e metanol, perdendo, assim, a capacidade de adoçar. As fórmulas estruturais do aspartame, fenilalanina e aspartato são apresentadas abaixo.
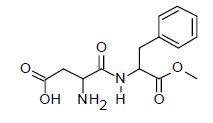
Aspartame
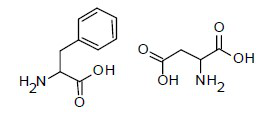
Fenilalanina Aspartato
De acordo com o texto e as fórmulas estruturais, assinale a alternativa correta.
Provas
Caderno Container