Foram encontradas 650 questões.
A reação (não balanceada) de síntese da amônia, a partir das substâncias simples H2(g) e N2(g) é representada por:
N2 + H 2 ↔ NH3
O que acontece a um equilíbrio se for aumentada a pressão através da adição de uma gás inerte?
Provas
Analisando a molécula KrF2, assinale a alternativa que apresenta corretamente o peso molecular, em números significativos, como resposta final deste composto, sabendo que o peso atômico do flúor é 18,9984032μ é do criptônio e 83,80μ
Provas
Em um laboratório de química, foi dada a seguinte ordem para a preparação de soluções: Preparar uma solução aquosa de cal viva a 1% com 50 gramas deste óxido puro para análise. Diante destes dados, pode-se afirmar que a quantidade de água utilizada neste processo foi de
Provas
Em relação às estruturas a seguir, assinale a alternativa que apresenta o conjunto de orbitais híbridos com ligações sigma (s – sp3).
Provas
Dissolveu-se 0,500g de carbonato de cálcio em um balão volumétrico de 250,0mL, completando-se o seu volume final com água até o menisco. Uma alíquota de 10,00mL dessa solução foi titulada com 20,00mL de uma solução de ácido clorídrico. Logo, a solução ácida apresentará concentração igual a
Provas
Reações entre ácidos e hidróxidos constituem reações de neutralização ou salificação. Estas reações são comuns em nosso dia-adia principalmente na neutralização do ácido clorídrico presente no estômago com hidróxidos de magnésio ou de alumínio. Seguindo o mesmo conceito, assinale a alternativa que indica os produtos de uma reação de neutralização quando reagem estequiometricamente 1mol de ácido carbônico com 1mol de hidróxido de sódio.
Provas
Ácido fosfórico ou ácido ortofosfórico é um composto químico de fórmula molecular H3PO4, sendo classificado, dentre os ácidos minerais, como um ácido fraco, oxiácido derivado do anidrido fosfórico. É o mais importante dos ácidos derivados do fósforo. Em relação à fórmula molecular indicada anteriormente no texto, assinale a alternativa correta sobre o número e tipos de ligações nesta estrutura.
Provas
Em um sistema fechado de volume igual a 1 litro, 1 mol de SO2(g) reage com 1 mol de O2(g), à temperatura constante, formando anidrido sulfúrico, de acordo com a reação (não balanceada) a seguir:
SO2(g) + O2(g) ↔ SO3(g)
Depois de estabelecido o equilíbrio químico, verifica-se a presença de 12,8g de SO2(g).
Analisando os dados acima, a constante de equilíbrio desta reação é igual a
Provas
A talidomida é um medicamento perigoso, responsável pela deformação de fetos. A droga foi desenvolvida em um laboratório alemão e lançada no mercado consumidor no final da década de 50. Considerada como calmante e ansiolítico, a talidomida foi largamente usada por gestantes para controlar as constantes náuseas e a tensão, típicas dos primeiros meses de gravidez. No entanto, o alívio que se tinha no princípio transformava-se em desespero e angústia alguns meses depois. Ao longo dos anos 60, muitos bebês nasceram deformados, sem braços ou pernas, com deficiências na estrutura vertebral, cegos ou surdos.
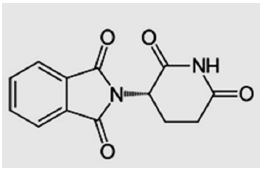
Em relação à estrutura da talidomida, assinale a alternativa que apresenta a função orgânica presente nesta espécie química.
Provas
Em relação ao método de extração denominado arraste a vapor, assinale a alternativa correta.
Provas
Caderno Container