Foram encontradas 562 questões.
No rótulo de uma embalagem de 90 g de um creme dental consta a informação de que o produto contém 1 450 ppm de flúor, que se apresenta na forma do composto Na₂SiF₆ (M = 188 g. mol–1). A massa do composto Na₂SiF₆, em gramas, no conteúdo dessa embalagem de creme dental é de, aproximadamente,
Provas
Analise as seguintes moléculas orgânicas:
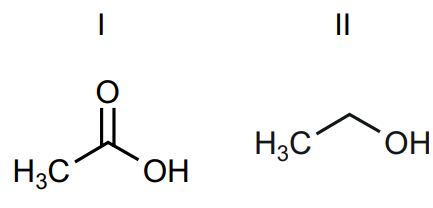
A reação entre I e II forma um composto que pertence à função orgânica ____________, por meio de uma reação de ____________.
As lacunas são preenchidas, correta e respectivamente, por:
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Considere a estrutura a seguir:
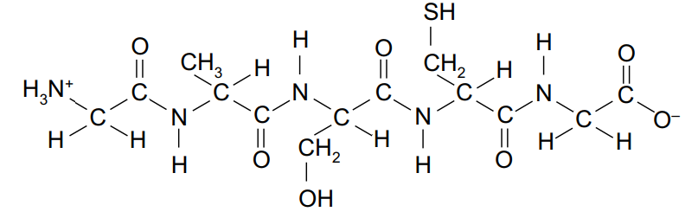
Ao sofrer reação de hidrólise, essa estrutura irá fornecer, no máximo,
Provas
O ácido sulfúrico reage com alguns metais e forma dióxido de enxofre e água. O potencial padrão de redução dessa semirreação é Eº = + 0,20V.
Sabendo que o potencial padrão de redução para Cr3+(aq) + 3e– → Cr(s) é –0,74 V,
o potencial padrão da reação global da interação entre o ácido sulfúrico e o crômio sólido, e a soma dos menores valores inteiros dos coeficientes estequiométricos dessa reação global são, respectivamente,
Provas
Examine a figura a seguir:
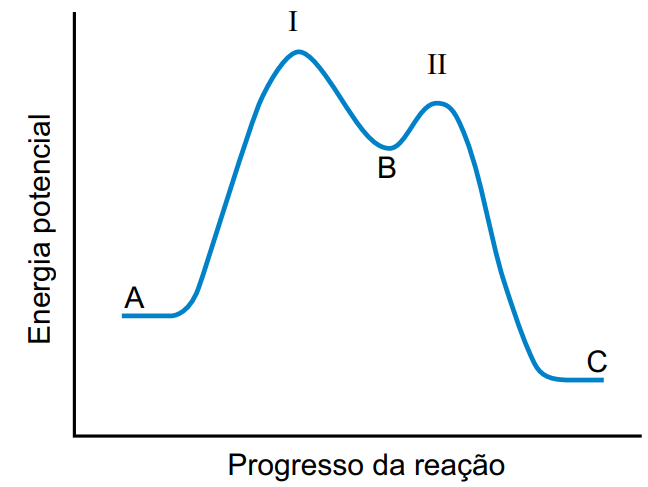
Progresso da reação I II (Brown, T. L.; LeMay Jr, H. E.; Bursten, B. E.; Burdge, J. R. Química, a ciência central, 2005. Adaptado)
A figura representa a relação da energia e o progresso da reação A → C, que ocorre em duas etapas. A reação A → C é uma reação ___________ e a velocidade da reação é determinada pela etapa ___________, a mais ___________, pois apresenta energia de ativação.
As lacunas são preenchidas, correta e respectivamente, por:
Provas
Analise as moléculas representadas a seguir:
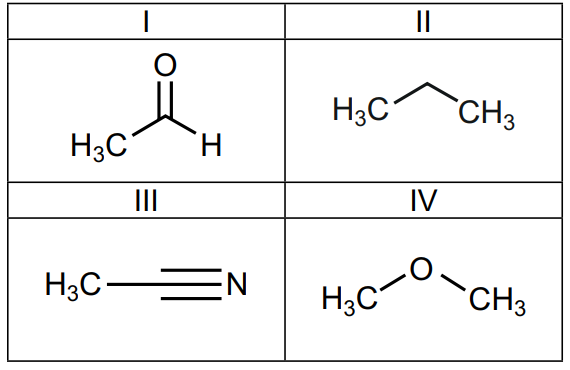
A ordem crescente das forças dipolo-dipolo para as moléculas I a IV é, respectivamente:
Provas
A partir do modelo da repulsão dos pares eletrônicos da camada de valência (VSEPR), a geometria molecular esperada para a molécula XeF4 é
Provas
Considere uma situação prática de eletrodeposição utilizada em processos industriais para recobrimento metálico, na qual se deseja calcular o tempo necessário para a deposição de uma massa conhecida de zinco sob corrente constante. Sabendo que a constante de Faraday é 9,65x104 C.mol–1, para a deposição de 2,0 mg de zinco metálico, o tempo necessário, em minutos, utilizando corrente de 10 mA, é de, aproximadamente,
Provas
Observe os dados de entalpia de formação (ΔH\( _f^º \)) da tabela a seguir:
| Composto | ΔH\( _f^º \) (kJ.mol–1) |
| C₂H₅OH(\( ℓ \)) | -278 |
| CO₂(g) | -394 |
| H₂O(\( ℓ \)) | -286 |
É correto afirmar que a entalpia padrão da reação de combustão completa do etanol (ΔH\( _f^º \)), em kJ.mol–1, é
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
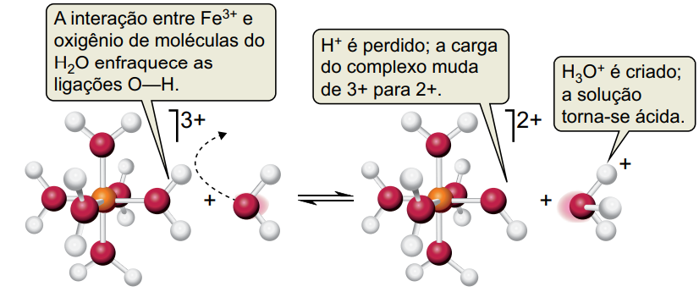
Considere a figura que mostra o mecanismo da reação de íons metálicos hidratados com a água, o exemplo é para o íon [Fe(H2O)6]3+, e a tabela de constantes de acidez (Ka) para cátions metálicos em solução aquosa, a 25 °C a seguir:
Figura
Tabela
| cátion | Ka |
|---|---|
| Zn2+ | 2,5x10–10 |
| Ni2+ | 2,5x10–11 |
| Cr2+ | 1,6x10–4 |
(Brown, T. L.; LeMay Jr, H. E.; Bursten, B. E.; Burdge, J. R. Química, a ciência central, 2005)
De acordo com a tabela e o mecanismo apresentado na figura, conclui-se que os íons metálicos hidratados se comportam como __________ e a solução que apresenta maior pH é a que contém os íons hidratados __________.
As lacunas são preenchidas, correta e respectivamente, por:
Provas
Caderno Container