Foram encontradas 90 questões.
Dispõe-se de duas lâmpadas de incandescência: L1 de 127 V – 40 W e L2 de 127 V – 60 W. Por equívoco, as lâmpadas são ligadas em série a uma fonte de tensão que mantém em seus terminais 127 V sob quaisquer condições.
Nesse caso, a potência P1 consumida pela lâmpada L1 e a potência P2 consumida pela lâmpada L2 são tais que
Provas
A figura representa, em gráfico cartesiano, como o módulo da velocidade de um projétil, lançado obliquamente do solo horizontal, varia em função do tempo entre o instante do lançamento e o instante em que retorna ao solo, supondo a resistência do ar desprezível.
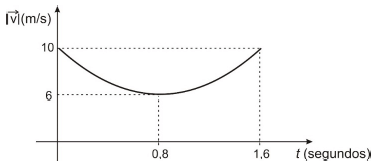
O alcance desse lançamento foi
Provas
A figura a seguir mostra um sistema de vasos comunicantes contendo água em equilíbrio hidrostático. O ramo da direita (3) é aberto. O ramo da esquerda (1) e o central (2) estão hermeticamente tampados, havendo, portanto, em ambos, ar comprimido entre as tampas e as superfícies livres da água.
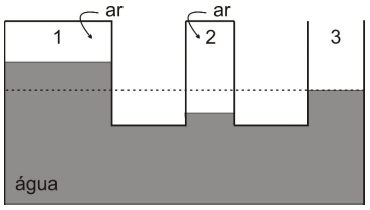
Sejam p1 a pressão do ar confinado no ramo da esquerda (1), p2 a pressão do ar confinado no ramo central (2), e p3 a pressão no ramo (3) - atmosférica local. Estas pressões são tais que
Provas
Alguns parâmetros utilizados para compor o Índice de Qualidade da Água (IQA) podem ser determinados por volumetria, como, por exemplo, o percentual de nitrogênio amoniacal.
Nesse método, resumidamente, o íon amônio presente na amostra de água analisada é transformado em amônia pela adição de base forte (equação I). O gás formado é quantitativamente separado por destilação e recolhido em solução contendo excesso de ácido bórico (equação II). O íon borato formado é, então, titulado com ácido sulfúrico (equação III).
(I) NH4+(aq) + OH– (aq) !$ \rightleftharpoons !$ NH3(g) + H2O(l)
(II) NH3(g) + H3BO3(aq) !$ \rightleftharpoons !$ NH4+(aq) + H2BO3– (aq)
(III) 2 H2BO3– (aq) + H2SO4(aq) !$ \rightleftharpoons !$ 2 H3BO3(aq) + SO4–2(aq)
Uma alíquota de 25,0 mL de uma amostra de água, com densidade 1,20 g/cm3, foi alcalinizada com excesso de hidróxido de sódio e, após destilação, toda a amônia foi recolhida em excesso de ácido bórico.
Se a titulação do borato formado consumiu 30,0 mL de ácido sulfúrico 0,50 mol.L-1, então o percentual em massa de nitrogênio amoniacal nessa amostra é
Dado: massa molar (g.mol-1): N=14,0
Provas
A análise dos parâmetros termodinâmicos de uma reação e de seus componentes é de fundamental importância para a compreensão de como e porque os fenômenos químicos ocorrem.
Observe a tabela a seguir que apresenta os valores de variação padrão de entalpia de formação !$ (\Delta H_f^0) !$e energia livre !$ (\Delta G_f^0) !$ para três hidrocarbonetos isômeros de fórmula molecular C4H8.
| Hidrocarboneto | !$ \Delta H_f^0 (KJ.mol^{-1}) !$ | !$ \Delta G_f^0 (KJ.mol^{-1}) !$ |
| cis-but-2-eno | – 6,99 | + 65,86 |
| trans-but-2-eno | – 11,17 | + 62,97 |
| metilpropeno | – 16,90 | + 58,07 |
A partir dos dados apresentados, analise as afirmativas a seguir.
I. A interconversão de cis-but-2-eno em trans-but-2-eno é um processo endotérmico.
II. O metilpropeno é termodinamicamente o mais estável dos três isômeros apresentados.
III. A interconversão de trans-but-2-eno em metilpropeno é um processo espontâneo.
Está correto o que se afirma em
Provas
Os critérios de solubilidade, assim como a acidez e basicidade dos compostos, são muito utilizados no desenho de estratégias eficientes para a separação de misturas.
Observe o fluxograma que representa uma estratégia de separação para uma mistura inicial contendo álcool benzílico e ácido benzoico nas condições padrão.
Os números I, II e III representam métodos físicos de separação distintos aplicados ao processo.
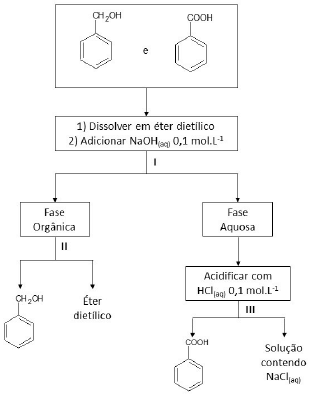
Sabendo que, nas condições padrão, o álcool benzílico é um líquido e o ácido benzoico é um sólido pouco solúvel em água, os processos I, II e III são, respectivamente, denominados
Provas
- Química InorgânicaSubstância e mistura: substância simples, substância composta e mistura. Alotropia
O grafeno é um nanomaterial composto por átomos de carbono que possui propriedades como alta condutividade térmica e elétrica, flexibilidade e elevada resistência mecânica. Essas características despertaram o interesse de diferentes setores industriais, que podem aplicar o material em uma ampla gama de produtos como baterias mais leves e com maior tempo de carga, smartphones com telas flexíveis, tintas anticorrosivas, plásticos e borrachas mais resistentes e condutores, ligas metálicas muito leves e tecidos e embalagens com barreira e dissipação térmica.
Disponível em: https://revistapesquisa.fapesp.br/grafeno-made-in-brasil/ Acesso em Jan/2021. (Adaptado)
A partir das informações do texto, o grafeno pode ser classificado como uma
Provas
Muitas das propriedades dos raios catódicos foram estudadas por J. J. Thomson. Seus estudos deram origem a descoberta da partícula denominada elétron. Mais do que isso, seus trabalhos levaram a determinação experimental da razão carga/massa dessa partícula e a proposição de um novo modelo para o átomo. Hoje é sabido que um átomo é composto também por outras partículas, como prótons e nêutrons, cerca de duas mil vezes mais pesados do que o elétron.
Dados:
- Constante de Avogrado: 6,0x1023
- Massa do próton: 1 u.
Sabendo que o módulo da carga elétrica de um elétron equivale a 1,6 x 10-19 C, é possível estimar que o valor para a razão carga/massa do elétron, em C/g, determinada por Thomson foi, aproximadamente, igual a
Provas
Várias espécies de terapia para câncer utilizam radiação para destruir células malignas. A terapia por captura de nêutrons pelo boro é diferente pelo fato do boro-10 injetado não ser radioativo. Entretanto quando esse isótopo é bombardeado com um nêutron, ele emite uma partícula alfa com alto grau de poder destrutivo.
Na terapia por captura de nêutrons pelo boro, o boro-10 é incorporado a um composto que é absorvido preferencialmente pelos tumores. O paciente é então exposto a breves períodos de bombardeamento por nêutrons. Assim que o bombardeamento cessa, o boro-10 para de gerar partículas alfa.
ATKINS, P., LORETTA J. Princípios de química: questionando a vida moderna e o meio ambiente. Porto Alegre: Bookman, 2001. (Adaptado)
No processo de captura de nêutrons pelo boro é correto afirmar que ocorre
Provas
Diversas transformações químicas na natureza ocorrem de maneira reversível, estabelecendo um estado de equilíbrio dinâmico no sistema. Entender os mecanismos moleculares envolvidos nesses processos é de fundamental importância para a Ciência, pois a partir deles é possível obter diversas informações.
Em condições reacionais específicas o fósforo (P) no estado gasoso pode reagir com gás cloro (Cl2), formando o pentacloreto de fósforo (PCl5), de acordo com a equação a seguir.
2 P(g) + 5 Cl2(g) !$ \rightleftharpoons !$ 2 PCl5(g)
Esse processo ocorre em duas etapas descritas a seguir, onde K1 e K2 representam as constantes de equilíbrio em cada etapa.
2 P(g) + 3 Cl2(g) !$ \rightleftharpoons !$ 2 PCl3(g) K1
PCl3(g) + Cl2(g) !$ \rightleftharpoons !$ PCl5(g) K2
A partir das informações apresentadas, é possível prever que, nessas mesmas condições, a constante de equilíbrio para a formação de pentacloreto de fósforo a partir de fósforo gasoso e gás cloro, em função de K1 e K2, é expressa por
Provas
Caderno Container