Foram encontradas 1.090 questões.
Com um conta-gotas determinou-se que são necessários 20 gotas para completar 1 ml. Em 1 gota de ácido clorídrico 0,0001mol/L encontramos:
Provas
Dados os números atômicos dos átomos de lítio (Li = 3), flúor (F = 9), enxofre (S = 16) e cloro (Cl = 17), assinale os tipos de Iigação química que estão presentes nos compostos LiF, SCI2 e Cl2, respectivamente.
Provas
Na bula de um frasco de dipirona sódica encontra-se:
Composição da Dipirona Sódica:
gotas com 0,5 g/ml de dipirona sódica e soluçãoinjetável com 0,5 g/ml de dipirona sódica.
Posologia e Administração da Dipirona Sódica:
gotas: adultos: 20 a 40 gotas, até 3 vezes por dia. Lactentes e crianças menores de 5 anos: 4 a 8 gotas, até 4 vezes por dia. Crianças maiores de 5 anos: 10 a 20 gotas, até 4 vezes ao dia. Solução injetável: adulto: a critério médico. Em média 1 a 4 ampolas por dia.
Indicações da Dipirona Sódica:
Analgésico e antipirético. www.bulas.med.br
O valor aproximado da concentração em mol/L para a dipirona sódica (C13H16N3O4SNa) é: ( M. atômica em g/mol: C=12, H=1, N=14, O=16, S=32 e Na=23)
Provas
Um estudante do ensino médio ao ler num pote de requeijão cremoso, verificou que era composto por: “Leite padronizado reconstituído, creme de leite, soro de leite, caseinato de cálcio, água, sal, cloreto de cálcio, fermentos lácteos, enzima protease, estabilizantes polifosfato de sódio e difosfato de sódio, conservante sorbato de potássio. Não Contém Glúten.” Curioso em saber o que era sorbato de potássio, pesquisou e encontrou a fórmula:
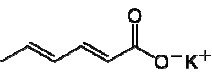
E afirmou que:
I – É um produto do reação do ácido sórbico com hidróxido de potássio.
II – Todos seus carbono são insaturados.
III – Sua fórmula molecular é C6 H7 K O2 .
Das afirmações do estudante:
Provas
Sobre radioatividade são feitas as seguintes afirmações:
I – A perda de uma partícula beta pelo átomo de 53 135 Iobtemos um isótopo do iodo.
II – Quando um núcleo emite uma partícula alfa seu número atômico diminui em duas unidades.
III – Na transformação do átomo 89 228Ac em 84 212 Po são emitidas 4 partículas alfa e 3 partículas beta.
Das afirmações:
Provas
Considere a distribuição eletrônica em níveis para os átomos:
A – K= 2, L= 8, M= 8 e N= 2.
B– K= 2, L= 8 e M= 7.
C– K= 2, L= 8, M= 12 e N= 2.
Sobre os átomos acima pode-se afirmar:
Provas
Segundo o site http://www.explicatorium.com. A valina é um aminoácido alifático primo da leucina e da isoleucina, tanto em estrutura, como em função. Estes aminoácidos são extremamente hidrofóbicos e são quase sempre encontrados no interior de proteínas. Eles raramente são úteis em reações bioquímicas normais, mas estão relegados à função de determinar a estrutura tridimensional das proteínas devido à sua natureza hidrofóbica. A valina representa cerca de 5% dos aminoácidos das proteínas do nosso organismo. O Leite e os ovos são alimentos ricos em valina. Sua fórmula estrutural é

A afirmativa incorreta sobre a valina é:
Provas
A reação de hidrogenação do but-2 eno é:
C4H8(g)+ H2(g) \( → \) C4H10(g)
A variação de entalpia em KJ / mol a 1atm e 298,15K,vale:
Dados:\( Δ \)Hfº (C4H8(g)) = −11,4; \( Δ \)Hfº (CO2(g)) = −393,5; \( Δ \)Hfº (H2O(l)) = −285,8 e\( Δ \)Hcº (C4H10(g)) = −2.877,6, em que \( Δ \)Hfºe \( Δ \)Hcº em kJ/mol, representam as variações de entalpia de formação e de combustão a 298,15 K e 1 atm, respectivamente.
Provas
A decomposição do dicromato de amônio ocorre conforme a equação não balanceada a seguir:
(NH4)2Cr2O7(s) \( → \) Cr2O3(s) + H2O (g) + N2(g)
Sobre isso, analise as afirmações:
I – É uma reação de deslocamento.
II – A soma dos menores e inteiros coeficiente é 7.
III – O cromo sofre redução.
É correto o que se afirma em
Provas
Em um cilindro de capacidade igual a 24,6 L, foram adicionados 1,0g de gás hidrogênio e 8,0g de gás oxigênio a uma pressão de 1,5 atm. A temperatura que essa mistura apresentará será de: (Dados : H = 1g/mol, O= 16g/mol e R= 0,082 atm.L/mol.K)
Provas
Caderno Container