Foram encontradas 890 questões.
A acidez e a basicidade em compostos orgânicos referem-se à capacidade dessas substâncias em doar ou aceitar prótons ou pares de elétrons, isso determina as reações e propriedades desses compostos, influenciando desde a química de biomoléculas até a síntese de medicamentos e materiais poliméricos. Sabe-se que o aumento da força do ácido está associada a maior estabilidade de sua base conjugada, portanto, qual dos ácidos abaixo será o mais forte?
Provas
Algumas propriedades físicas dos compostos orgânicos, como ponto de ebulição ou fusão e solubilidade, podem ser determinadas com base na polaridade das ligações entre os átomos formadores desses compostos e a interação entre as moléculas. Baseado nessas informações, que grupo funcional você espera que possua o ponto de ebulição mais elevado? (Considere que as moléculas possuem massa molar semelhantes).
Provas
Os métodos eletroanalíticos são uma classe de técnicas em química analítica que estudam um analito medindo a tensão elétrica e/ou a corrente elétrica em uma célula eletroquímica. Na potenciometria, é medida a diferença de potencial do eletrodo. Sabendo disso, calcule o pH de uma solução onde, numa pilha, um eletrodo de hidrogênio (p = 1 atm) é imerso na solução e interligado a um eletrodo-padrão de cobre, fornecendo uma diferença de potencial igual a 0,514 V. A alternativa que apresenta o valor obtido é:
Considere o Potencial-padrão de redução do cobre: Cu2+(aq) + 2 e– → Cu(s) E = +0,337.
Provas
Os óleos essencais de eucalipto são ricos em compostos classificados como monoterpenos e sesquiterpenos. Em uma análise do óleo essencial da espécie Eucalyptus Cinerea, a quantificação dos componentes foi realizada com equipamento Shimadzu GC-17 equipado com detector de ionização de chama (FID) e coluna capilar de sílica fundida RTX-5 (30 m x 0,25 mm, espessura de filme de 0,25 μm). Foram encontrados apenas quatro componentes, como mostra o cromatograma a seguir:
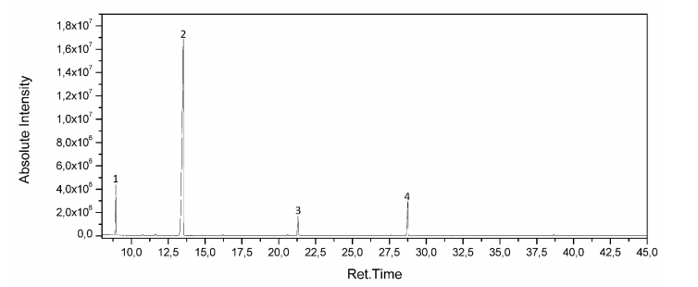
Cromatograma do óleo essencial extraído das folhas de Eucalyptus Cinerea. (Fonte: Tese de Doutorado do Prof. Claudinei Andrade Filomeno)
Esses componentes foram identificados como sendo α-terpineol, α-pineno, Acetato de α-terpinil e 1,8-cineol, cujas estruturas são mostradas a seguir:
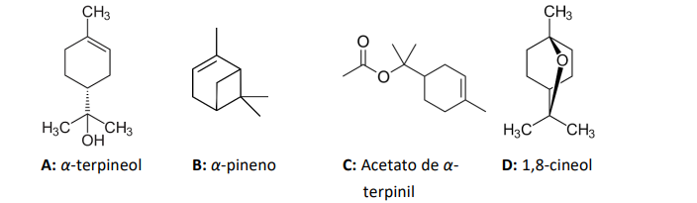
Assinale a alternativa que associa CORRETAMENTE o componente identificado e o seu tempo de retenção.
Provas
A cromatografia é uma técnica analítica que tem por finalidade a separação e/ou purificação de misturas. Sobre essa técnica, são feitas as afirmações a seguir:
I. Na cromatografia gasosa, a fase móvel pode ser um gás inerte e a fase estacionária pode ser um adsorvente sólido ou um líquido adsorvido em um suporte inerte;
II. Na cromatografia líquida, tanto a fase estacionária como a fase móvel são líquidas;
III. A cromatografia em camada delgada é uma técnica usada para separar misturas de compostos com base em diferenças de polaridade. Nessa técnica, quanto mais polar a substância, maior é o tempo de retenção, quando utilizada uma fase estacionária de sílica-gel.
Está(ão) CORRETA(S), apenas:
Provas
A análise de cálcio em uma amostra de urina foi determinada por gravimetria, onde o Ca2+ foi precipitado a oxalato de cálcio (CaC2O4), em meio básico, que, após lavagem em água fria, foi dissolvido em ácido para formar ácido oxálico e Ca2+. O ácido oxálico dissolvido foi aquecido e titulado com uma solução padrão de permanganato de potássio, segundo a reação:
2 MnO4-(aq) + 5 C2O42-(aq) + 16 H+ \( \rightarrow \) 2 Mn2+(aq) + 10 CO2(g) + 8 H2O(I)
A padronização da solução de permanganato de potássio foi realizada a partir do preparo de 100 mL de uma solução contendo 0,134 g oxalato de sódio. Na titulação de 10 mL desta solução, foram gastos 40,00 mL da solução de permanganato de potássio.
Determine a massa, em mg, de cálcio numa amostra de 5,00 mL de urina, cuja titulação com a solução padrão de permanganato de potássio foram gastos 15,00 mL.
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Fazer o estudo do comportamento de uma curva de titulação de um sistema e determinar o pH nas proximidades do ponto de equivalência é fundamental para escolher o indicador adequado em uma análise volumétrica. Considerando a faixa de pH de mudança de cor do indicador informados na tabela a seguir, qual é o indicador mais adequado numa análise volumétrica de 20,0 mL de uma solução 0,001 mol/L de ácido acético (Ka = 1,8 x 10-5) com uma solução 0,001 mol/L de hidróxido de sódio?
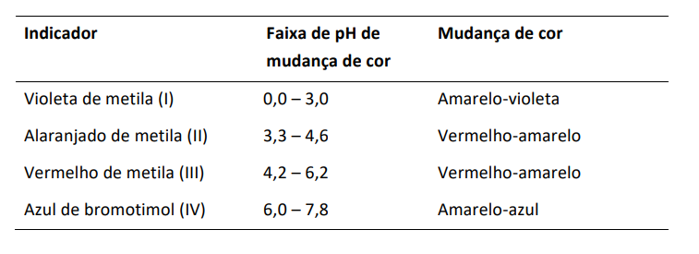
Provas
O método de Volhard, utilizado na volumetria de precipitação, consiste em precipitar o analito com um excesso de solução padrão de AgNO3 e, em seguida, titular a prata residual, em meio ácido, com uma solução padrão de tiocianato de potássio, usando Fe 3+ como indicador. Uma amostra de 20,0 mL de uma solução desconhecida de cloreto foi tratada com 50,0 mL de AgNO3 0,100 mol/L. Após remoção do precipitado por filtração, adicionou-se Fe3+ ao filtrado e titulou-se com KSCN 0,200 mol/L, onde foram necessários 15,0 mL do titulante para a solução se tornar vermelha. Qual o teor de cloreto nessa amostra?
Provas
O ácido lático (HC3H5O3) é um subproduto naturalmente produzido pelo organismo durante a realização de exercícios físicos. Sendo um ácido fraco, é pouco ionizado. Determine o valor aproximado do pH de uma solução aquosa 0,010 mol/L de ácido lático (Ka = 1,4 x 10-4 ).
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
O equilíbrio iônico é um caso particular do equilíbrio químico e estuda o comportamento dos íons em solução. Uma solução é classificada como eletrólito forte pela grande quantidade de espécies iônicas liberadas em solução. Já um eletrólito fraco tem o número de íons reduzido. O equilíbrio é medido pela constante de equilíbrio e pelo grau de equilíbrio. Para que ele ocorra, é necessário que a temperatura seja constante e o sistema não tenha trocas com o ambiente.
Considerando o equilíbrio iônico a seguir, assinale a alternativa CORRETA:
![]()
Provas
Caderno Container