Foram encontradas 890 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Numa aula prática de Química, serão utilizados 800 mL de solução de NaOH 0,5 mol/L. Porém, não foi encontrada nenhuma solução com a concentração necessária, havendo disponíveis apenas as seguintes soluções de NaOH:
Solução A: 1,0 mol/L
Solução B: 5 g/L
Solução C: 0,25 mol/L
O técnico de laboratório resolveu o problema misturando quantidades adequadas de cada solução. Sabendo que foram utilizados 100 mL da solução B, quais foram os volumes utilizados das soluções A e C, RESPECTIVAMENTE?
Provas
A emissão de óxidos de nitrogênio nos processos de combustão provoca um problema ambiental sério porque esses óxidos são poluentes primários e geram poluentes secundários através de ciclos fotoquímicos na atmosfera. Normalmente, o óxido de nitrogênio emitido em maior quantidade é o NO que se oxida a NO2 quando reage com oxigênio:
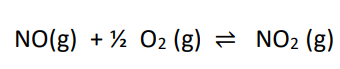
Calcule a constante de equilíbrio do sistema anterior, no estado padrão, utilizando dados termodinâmicos:
Dados: \( \Delta \)Gºf (NO2(g)) = + 52 kJ/mol ; \( \Delta \)Gºf (NO(g)) = + 87 kJ/mol; R = 8,314 J/mol.K
A opção que apresenta a alternativa CORRETA é:
Provas
As medalhas de ouro entregues aos primeiros lugares nos jogos olímpicos não são de ouro maciço. Tais medalhas são feitas de prata maciça com uma camada de ouro depositada. Nas olimpíadas de Paris, as medalhas recebidas pelas pessoas que conquistaram as primeiras colocações tinham massa total de 529 g. Desse total, além do ouro depositado, 505 g eram de prata e havia uma placa de ferro, retirada da torre Eiffel, com massa de 18 g.
Considerando que o ouro foi depositado na medalha de prata a partir da eletrólise de uma solução de nitrato auroso, calcule a intensidade de corrente necessária para que o processo demorasse 1 h para cada medalha e assinale a alternativa CORRETA.
Provas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
Uma das características dos íons complexos de metais de transição é a cor que resulta, entre outras coisas, da interação dos fótons da luz com os elétrons d do metal. A seguir, são apresentados alguns íons complexos e suas respectivas cores:

Os nomes oficiais dos íons complexos anteriores são encontrados, RESPECTIVAMENTE, na alternativa:
Provas
Outra análise importante que deve ser feita ao se propor a utilização de um novo combustível é determinar seu poder calorífico, ou seja, a quantidade de energia liberada pela sua queima. Como a queima ocorre em temperaturas elevadas, uma correção do poder calorífico com a temperatura pode ser necessária. Assinale a alternativa que indica o poder calorífico da combustão da amônia, produzindo monóxido de nitrogênio, segundo a equação não balanceada, que ocorre a 1025 ºC:

Provas
Atualmente, há várias pesquisas que buscam combustíveis alternativos para os combustíveis baseados no carbono, com o objetivo de reduzir as emissões de dióxido de carbono (CO2). Uma dessas possibilidades é usar a amônia como combustível, já que sua combustão não emite CO2. Porém, a combustão da amônia pode produzir óxidos de nitrogênio que são poluentes atmosféricos importantes, assim, deve-se olhar com cautela essa alternativa. Assinale a alternativa que indica o volume de ar, contendo 21% (v/v) de oxigênio, necessário para produzir 500 L de dióxido de nitrogênio, a 1027 ºC e 1,3 atm, durante a combustão da amônia, produzindo dióxido de nitrogênio, segundo a equação não balanceada:
NH3(g) + O2(g) → NO2(g) + H2O(g)
Provas
O conhecimento da geometria das espécies químicas permite estimar propriedades físicas e prever como cada espécie interage com outras. Qual é a alternativa que apresenta a geometria de cada espécie química a seguir, RESPECTIVAMENTE?
I. BrF3
II. ClF5
III. I3–
IV. H2Te
V. BrF4–
Provas
O iodo pode ser utilizado para fazer experimentos simples em laboratório que permitem analisar fenômenos físicos e químicos. Um desses experimentos consiste em aquecer ligeiramente cristais de iodo sólido num tubo de ensaio para se observar a formação de um vapor violeta. Uma outra possibilidade de experimento é colocar cristais de iodo num tubo de ensaio com água destilada à temperatura ambiente e observar que a solubilidade do iodo é pequena. Em seguida, acrescentando-se uma pequena quantidade de iodeto de potássio ao tubo com agitação, percebe-se que o sólido se dissolve totalmente.
Analise as afirmações a seguir, relacionadas aos experimentos descritos anteriormente, e marque a alternativa INCORRETA:
Provas
Recentemente, uma carga com material radioativo foi roubada em São Paulo e, felizmente, recuperada sem maiores problemas. Um dos elementos radioativos contidos nessa carga era um isótopo do germânio (\( G \)\( e \)) utilizado em exames na medicina nuclear. Sabendo que o ![]() é um emissor de pósitrons, seu decaimento radioativo gera:
é um emissor de pósitrons, seu decaimento radioativo gera:
Provas
A figura a seguir apresenta a redução na energia de ativação de uma reação devido à utilização de um catalisador.

Figura 2 – Energia em função do caminho da reação.
Utilizando a Lei de Arrhenius, calcule a razão entre as constantes de velocidade da reação com catalisador (k2) e sem catalisador (k1), a 27 ºC e 1 atm. A alternativa que apresenta essa razão é:
Dado: R = 8,314 J/mol.K
Provas
Caderno Container