Foram encontradas 440 questões.
Para determinar a pureza do cloreto de potássio (KCl), presente em uma amostra de fertilizante, foi empregada um método analítico no qual todo o cloreto contido na amostra foi titulado com uma solução padrão de nitrato de prata (AgNO3) 0,10 mol.L-1 , utilizando cromato de potássio (K2CrO4) como indicador. O laboratorista realizou os seguintes procedimentos:
I) Utilizando uma balança analítica, pesou-se 1,00 g da amostra do fertilizante (KCl) que foi dissolvido e transferido para a vidraria 1, com o volume definido de 100,00 mL, completando-se o volume e homogeneizando-se a solução.
II) Utilizando a vidraria 2, retirou-se uma alíquota de 10,00 mL da solução preparada no item I.
III) A alíquota foi transferida quantitativamente para a vidraria 3, juntamente com uma quantidade apropriada do indicador.
IV) A alíquota foi titulada adicionando-se nitrato de prata com o auxílio da vidraria 4. Ao longo do procedimento, observou-se inicialmente a formação de um precipitado branco (precipitado 1). No ponto final da titulação observou-se a formação e permanência de um segundo precipitado de coloração marrom avermelhado (precipitado 2).
V) Na titulação, foram gastos 13,00 mL da solução padrão de nitrato de prata 0,10 mol.L-1
Considerando essas informações, identifique as vidrarias 1, 2, 3, 4, a fórmula química dos precipitados 1 e 2, respectivamente, e a pureza do KCl. (Dados Massa Molar K= 39 g.mol-1 , Massa Molar Cl = 35,5 g.mol-1 .
Provas
Assinale a alternativa INCORRETA:
Provas
Com base nas informações e dados apresentados abaixo.
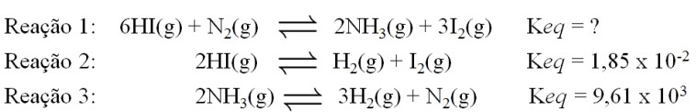
Considerando que o sistema apresentado na reação 1, esteja em equilíbrio, qual das alternativas apresenta, respectivamente, o valor da constante de equilíbrio para a reação 1 e um fator que contribui para o aumento da quantidade de amônia no sistema.
Provas
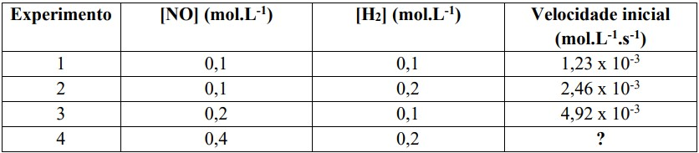
Com base nos dados experimentais apresentados abaixo. Determine a lei de velocidade para a reação entre o óxido nítrico com o hidrogênio, produzindo nitrogênio e água, bem como a velocidade inicial para o experimento 4.
2NO(g) + 2H2(g) → N2(g) + 2H2O(g)
Provas
A síntese da amônia a partir de hidrogênio e nitrogênio, utilizando ósmio como catalisador, realizada por Fritz Haber (1868-1934) e seu assistente Robert Le Rossignol (1884-1976) no laboratório da Universidade Técnica de Karlsruhe, em 2 de julho de 1909, onde demonstraram para Alwin Mittasch (18691953) e Julius Kranz, ambos da BASF (Badische Anilin und SodaFabrik), apesar das controvérsia envolvendo suas aplicações, tem sua importância reconhecida como uma das maiores descobertas da ciência.
Adaptado de: A síntese da amônia: alguns aspectos históricos.
Quim. Nova, Vol. 30, Nº . 1, 240-247, 2007.
Considere as afirmativas abaixo relativas a reação de síntese da amônia, representada pela equação abaixo, bem como as características das moléculas envolvidas e marque a alternativa em que toda(s) a(s) afirmativa(s) esteja(m) correta(s).
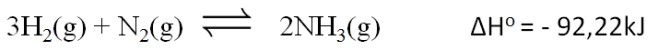
I - Segundo o modelo de repulsão dos pares de elétrons de valência a molécula da amônia apresenta uma geometria trigonal plana.
II – A molécula de nitrogênio molecular (N2) é formada por 1 ligação sigma (σ) e 2 ligações pi (π), apresentando hibridização sp2 , enquanto a amônia é formada por 3 ligações sigma (σ) e apresenta hibridização sp3 .
III – A composição da mistura de reação da síntese da amônia no equilíbrio apresenta energia livre de Gibbs (∆G) igual a zero.
IV - Considerando que a constante de equilíbrio (Keq) da reação de síntese da amônia seja igual a 1,45 x 10-5 a 500 °C, ao alterar a temperatura do sistema reacional para 600 ºC o valor da constante de equilíbrio permanecerá o mesmo.
V – Ao aumentar a pressão do sistema reacional, espera-se que o equilíbrio seja deslocado favorecendo a formação de amônia.
Provas
Um laboratorista precisava preparar 500 mL de uma solução de ácido nítrico (HNO3) com concentração de 0,3 mol.L-1 , para um determinado procedimento no laboratório. Contudo, por um equívoco, ele preparou 200 mL da solução de HNO3 com concentração de 0,1 mol.L1 . Para tanto, ele usou uma solução de ácido nítrico comercial. A fim de corrigir o seu erro, o laboratorista aproveitou toda a solução com concentração de 0,1 mol.L-1 , que havia preparado, e acrescentou a ela uma alíquota da solução comercial, completando, na sequência, o volume com água para 500 mL. Determine o volume da alíquota da solução comercial, utilizada no preparo da solução de 0,3 mol.L-1 , de interesse do laboratorista.
Dados da solução comercial: HNO3 com concentração de 58,5% (m/m); densidade 1,4 g.mL-1 ; Massa molar: H = 1 g.mol-1 ; N = 14 g.mol-1 ; O = 16 g.mol-1 .
Provas
Qual a massa de ferro metálico e de dióxido de carbono, respectivamente, produzida a partir de 12,5 toneladas de minério de ferro por redução com monóxido de carbono em alto forno, através da reação química não balanceada apresentada abaixo. Sabendo que o minério de ferro usado tem em sua composição 80% de óxido de ferro(III) e 20% de impurezas.
Fe2O3 (s) + CO(g) → Fe(s) + CO2(g)
Dados:
Massa Molar C = 12 g.mol-1 ; O = 16 g.mol-1 ; Fe = 56 g.mol-1 ; Fe2O3 = 160 g.mol-1 ; CO = 28 g.mol-1 .
Provas
Sobre as propriedades químicas do carbono e seus compostos, assinale a alternativa CORRETA.
Provas
Em um erlenmeyer foi adicionado certa quantidade de limalha de um metal M. Na sequência, foi adicionado, lentamente, uma solução de ácido nítrico até que o metal tenha sido totalmente consumido, observando-se um gás, G, de coloração vermelho-acastanhado. À solução final, obtida no erlenmeyer, de coloração verde, foi adicionado solução de amônia, observando-se o aparecimento da cor azul forte, indicando a formação de um complexo C. Sabe-se que o metal M é de transição e de configuração (n-1) d10 , na sua forma eletricamente neutra e que a valência primária de M, no complexo C, é 2+ e sua valência secundária é 4.
Sobre as espécies M, G e C e suas propriedades, analise as afirmativas abaixo e assinale a alternativa INCORRETA.
Provas
As propriedades periódicas dos elementos influenciam na natureza química de seus compostos, que por sua vez, estão relacionadas às configurações eletrônicas da camada de valência dos elementos. Baseado nas propriedades periódicas e dos compostos do grupo 13, avalie as afirmativas a seguir:
( ) O boro e o alumínio, com Nox 3+, apresentam uma alta razão carga/raio, favorecendo ligações direcionais em seus compostos.
( ) O raio do Ga é ligeiramente menor que o raio do Al devido à baixa eficiência de blindagem dos elétrons nd10 no átomo de gálio.
( ) Ao longo do grupo 13, a acidez de Lewis aumenta com o aumento do raio devido à melhor acomodação dos pares de elétrons provenientes da base de Lewis.
( ) O Boro tem uma relação diagonal com o silício. Ambos são ácidos de Lewis, e podem formar os íons complexos tetracoordenados: [Si(CH3)4]- e [B(CH3)4] - .
( ) O íon Tl+ é diamagnético e ele é mais comum que o íon Tl3+, devido ao efeito do par inerte.
Marque a opção que contenha a sequência CORRETA, de cima para baixo:
Provas
Caderno Container