Foram encontradas 574 questões.
Observe os efeitos do deslocamento do equilíbrio químico que ocorre em duas soluções, cujos sistemas apresentam as respectivas equações de equilíbrio:
Equação de Equilíbrio da Solução 1:
2 CrO4-2 (aq) + 4 H+ (aq) Cr2O7 -2(aq) + 2 H2O (l)
Cr2O7 -2(aq) + 2 H2O (l)
Equação de Equilíbrio da Solução 2:
[CoCl 4] -2 (aq) + 4H2O(l) [Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0
[Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0
Com base nas informações acima, foram feitos quatro experimentos, com as duas soluções, levando-se em conta as condições para observação do deslocamento do equilíbrio químico. Os resultados foram tabelados abaixo.
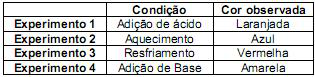
São informações corretas a respeito do estudo efetuado acima, exceto uma. Assinale a alternativa que a apresenta.
Equação de Equilíbrio da Solução 1:
2 CrO4-2 (aq) + 4 H+ (aq)
 Cr2O7 -2(aq) + 2 H2O (l)
Cr2O7 -2(aq) + 2 H2O (l) Equação de Equilíbrio da Solução 2:
[CoCl 4] -2 (aq) + 4H2O(l)
 [Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0
[Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0 Com base nas informações acima, foram feitos quatro experimentos, com as duas soluções, levando-se em conta as condições para observação do deslocamento do equilíbrio químico. Os resultados foram tabelados abaixo.

São informações corretas a respeito do estudo efetuado acima, exceto uma. Assinale a alternativa que a apresenta.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
As teorias sobre ácido-base podem explicar uma série de efeitos cotidianos e também auxiliam na otimização dos processos industriais. Com base na teoria de ácido-base de Bronsted-Lowry, são propostas as seguintes equações:
Equação 1:
NH4 + (aq) + OH- (aq) NH3(aq) +H2O(l)
NH3(aq) +H2O(l)
Equação 2:
HSO4 - (aq) + HCO3-(aq) SO4 2- (aq) + H2CO3(aq)
SO4 2- (aq) + H2CO3(aq)
São pares de base e base conjugada de Bronsted-Lowry, respectivamente, em cada equação:
Equação 1:
NH4 + (aq) + OH- (aq)
 NH3(aq) +H2O(l)
NH3(aq) +H2O(l) Equação 2:
HSO4 - (aq) + HCO3-(aq)
 SO4 2- (aq) + H2CO3(aq)
SO4 2- (aq) + H2CO3(aq) São pares de base e base conjugada de Bronsted-Lowry, respectivamente, em cada equação:
Provas
Questão presente nas seguintes provas
A quantidade de sulfato de sódio (Na2SO4) presente em uma solução pode ser determinada por uma solução de cloreto de bário (BaCl2). A equação química que representa esta determinação é a seguinte:
Na2SO4(aq) + BaCl2 (aq) → NaCl(aq) + BaSO4 (s)
(Dados de massas atômicas (u): Na = 23; S = 32; O = 16; Ba = 137; Cl = 35,5)
Se 50,00mL da solução de sulfato de sódio consome 12,25mL de uma solução a 0,02mol/L de cloreto de bário, assinale a alternativa que apresenta a massa de sulfato de sódio presente.
Na2SO4(aq) + BaCl2 (aq) → NaCl(aq) + BaSO4 (s)
(Dados de massas atômicas (u): Na = 23; S = 32; O = 16; Ba = 137; Cl = 35,5)
Se 50,00mL da solução de sulfato de sódio consome 12,25mL de uma solução a 0,02mol/L de cloreto de bário, assinale a alternativa que apresenta a massa de sulfato de sódio presente.
Provas
Questão presente nas seguintes provas
1,5225g de um sólido com a fórmula genérica MgCl2.X H2O a 100°C perde todas as moléculas de água, formando um sólido branco de massa 0,7125g. Sendo assim, é correto afirmar que o número de moléculas de água (X) presentes na fórmula genérica é
(Dados: massas molares (g/mol): Mg = 24; Cl = 35,5; H = 1; O = 16)
(Dados: massas molares (g/mol): Mg = 24; Cl = 35,5; H = 1; O = 16)
Provas
Questão presente nas seguintes provas
Uma amostra impura de chumbo (IV) e água tem a massa total de 10,00g. Com a finalidade de determinar a quantidade total de chumbo, foi retirada uma alíquota de 2,50g da amostra que foi decomposta por aquecimento a temperatura acima de 470°C e foi obtido 0,91g de sólido. Observe a equação química que representa a decomposição.
Pb(NO3)4(s) → Pb(s) + N2O4(g) + O2(g)
(Dado de massas molares (g/mol): Pb(NO3)4 = 455; Pb = 207; N2O4 = 92, O2 = 16)
Então, é correto afirmar que a massa total de nitrato de chumbo (IV) presente na amostra é de, aproximadamente,
Pb(NO3)4(s) → Pb(s) + N2O4(g) + O2(g)
(Dado de massas molares (g/mol): Pb(NO3)4 = 455; Pb = 207; N2O4 = 92, O2 = 16)
Então, é correto afirmar que a massa total de nitrato de chumbo (IV) presente na amostra é de, aproximadamente,
Provas
Questão presente nas seguintes provas
É possível extrair o álcool isopropílico (ou 2-propanol, C3H8O), que foi misturado em um óleo mineral (mistura de hidrocarbonetos), colocando 2mL deste sistema em 25mL de água; após agitação, deixa-se repousar e observa-se a formação de duas fases, conforme desenho abaixo.
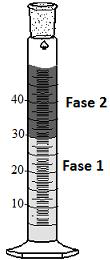
(Densidade(g/ml) a 25°C: óleo mineral = 0,81; água = 1,0)
É correto afirmar que o aumento do volume da fase 1 se deve às interações intermoleculares

(Densidade(g/ml) a 25°C: óleo mineral = 0,81; água = 1,0)
É correto afirmar que o aumento do volume da fase 1 se deve às interações intermoleculares
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaHidrocarbonetos
Os triazóis são uma classe de substâncias de grande importância no tratamento de doenças infecciosas emergentes, tais como candidíases. Essa classe de compostos apresenta, em sua estrutura, um ciclo composto por três átomos nitrogênios. São dadas a seguir as estruturas de alguns triazóis:
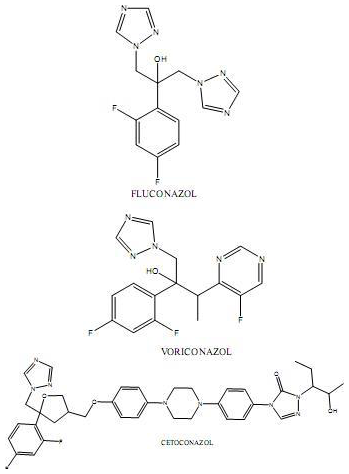
Diante do exposto, assinale a alternativa incorreta.

Diante do exposto, assinale a alternativa incorreta.
Provas
Questão presente nas seguintes provas
A tabela de uma reação química em função do tempo foi determinada a partir da concentração dos reagentes (A e B) e do produto formado (C), conforme as informações abaixo.
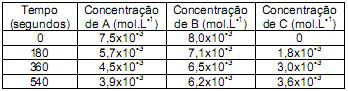
Segundo os dados obtidos acima, é correto afirmar que os módulos das velocidades médias (mol.L-1 .min-1 ) da reação em função da concentração de A, B e C, respectivamente, entre os intervalos de tempo de 3 minutos e 6 minutos, são:

Segundo os dados obtidos acima, é correto afirmar que os módulos das velocidades médias (mol.L-1 .min-1 ) da reação em função da concentração de A, B e C, respectivamente, entre os intervalos de tempo de 3 minutos e 6 minutos, são:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A bula de um frasco de 15,0mL de paracetamol em gotas indica que cada gota contém 13,0mg de paracetamol. Sabendo que cada gota tem 0,0500mL, assinale a alternativa que apresenta a porcentagem de paracetamol (% m/v) neste frasco.
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Considere uma solução de etilenodiamina (C2H8N2), cuja densidade é 0,900 g/cm3 . (Dados de massas atômicas (u): C = 12; H = 1,0; N = 14). A partir destes dados, analise as assertivas abaixo.
I. A densidade também pode ser considerada como sendo 9,00.102 g/L.
II. Se um rótulo informa que tem 50,0Kg de etilenodiamina, então, o volume da embalagem tem que ser maior do que 100L.
III. É possível considerar que o teor de etilenodiamina é 90,0%(m/v).
IV. A concentração da solução de etilenodiamina pode ser considerada como sendo 15,0mol/L.
É correto o que se afirma em
I. A densidade também pode ser considerada como sendo 9,00.102 g/L.
II. Se um rótulo informa que tem 50,0Kg de etilenodiamina, então, o volume da embalagem tem que ser maior do que 100L.
III. É possível considerar que o teor de etilenodiamina é 90,0%(m/v).
IV. A concentração da solução de etilenodiamina pode ser considerada como sendo 15,0mol/L.
É correto o que se afirma em
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container