Foram encontradas 1.513 questões.
Os íons Mn2+ reagem em meio aquoso ácido com os íons BiO3− formando íons permanganato, íons Bi3+ e água. A soma dos menores valores inteiros dos coeficientes estequiométricos da equação corretamente balanceada dessa reação é:
Provas
O biodiesel pode ser obtido por reação de transesterificação de óleos vegetais ou de gordura animal (trialcilglicerol). Esta reação se processa com o aquecimento do trialcilglicerol e um álcool de cadeia curta, empregando-se um ácido forte como catalisador. Forma-se como produtos o éster, que é o biodiesel, e um triálcool, o glicerol. Cuidados são tomados para que a reação se processe na ausência de água para evitar a hidrólise do biodiesel no meio reacional.
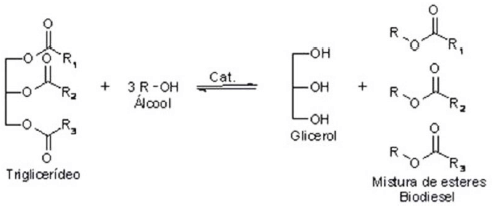
Considerando-se a síntese do biodiesel a partir do óleo de coco (R1 = R2 = R3 = C11H23) com metanol, a reação indesejada de hidrólise do biodiesel geraria com um dos produtos um composto com fórmula molecular
Provas
Atendendo às regras de segurança no laboratório químico, todos os frascos devem possuir rótulos que indiquem claramente seu conteúdo. Uma forma de representar os perigos associados ao conteúdo do frasco é a inclusão no rótulo do diamante de Hommel.
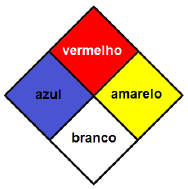
Risco para a saúde, perigo de incêndio e perigo de instabilidade são classificados em uma escala que abrange valores de 0 (mínimo) a 4 (máximo) e são correta e respectivamente representados no Diamante de Hommel nos campos de cores:
Provas
Um estudo cinético da reação de síntese do composto Z foi feito a partir da reação dos compostos X e T.
X(g) + T (g) → Z(g)
Três experimentos, I, II e III, de medida de velocidade de reação foram feitos em condições de temperatura e pressão controladas e constantes. Os resultados são expressos na tabela a seguir.
|
Experimento |
[X] mol.L-1 | [T] mol.L-1 |
Velocidade de formação de Z mol.L-1s-1. |
| I | x | t | v |
| II | x | 3t | v |
| III | 9x | t | 3v |
Com base nos resultados dos experimentos é possível concluir corretamente que os valores de ordem de reação para consumo das substâncias X e T são, respectivamente:
Provas
Um composto orgânico formado apenas por carbono, hidrogênio e oxigênio foi analisado por combustão. Uma amostra de 90 mg desse composto foi queimada adequadamente em um equipamento apropriado e como resultado da combustão completa formaram-se 176 mg de CO2 e 90 mg de H2O. A fórmula mínima do composto orgânico analisado é corretamente representada por
Provas
As ligações químicas nos compostos !$ C \ell F_3 !$ e !$ IF_5 !$ são corretamente representadas empregando-se para os átomos centrais dessas moléculas, respectivamente, os conjuntos de orbitais híbridos
Provas
Considere a teoria cinético-molecular dos gases para analisar as informações a seguir:
I – Os gases são constituídos por moléculas ou átomos que estão em movimento constante e aleatório.
II – Quando as moléculas de um gás colidem entre si, não há perda energia individual.
III – Há uma relação entre a energia cinética média das moléculas do gás e a temperatura absoluta.
IV – A colisão entre as moléculas de um gás dentro de um recipiente isolado não causa alteração na energia total.
São corretas somente as afirmações:
Provas
A equação de estado cúbica a seguir é uma forma simples para representar comportamentos de gases reais. Considere que dentro de um recipiente fechado de formato cúbico com arestas de 40cm há 32g de metano à temperatura de 50ºC. Caso se trate de um sistema isotérmico perfeitamente isolado, poderemos dizer que:
!$ P = { \large n R .T \over V - b} - { \large a \over V^2} !$
Dados: R = 0,082 atm.L/mol.K; a = 5,7 x 10-7 atm/cm6; b = 1,35 x 104 cm3; MMC = 12 g/mol; MMH = 1 g/mol
Provas
Uma cápsula de certo medicamento para dores de cabeça possui um fármaco que se degrada no organismo de acordo com uma cinética de primeira ordem e com uma constante de velocidade, k = 3,5 d-1. Este composto, após ser ingerido, perde a sua eficiência no organismo quando sua concentração chega à metade da concentração inicial. Em quanto tempo o medicamente deixa de fazer efeito? Use ln !$ 2 \approx 0,7 !$.
Provas
O elemento fósforo natural tem abundância isotópica de 100% fósforo-31. Entretanto pode-se produzir sinteticamente o radioisótopo fósforo-32 que decai para enxofre-32. Qual é a partícula emitida nesse processo de decaimento radioativo?
Provas
Caderno Container