Foram encontradas 1.513 questões.
As geometrias da molécula de metano e dos íons CH3+ e CH3- são, respectivamente:
Provas
O desenvolvimento dos catalisadores de Grubbs de primeira e segunda geração revolucionaram a área de síntese orgânica. Assinale a alternativa que contenha a reação química na qual esses catalisadores são empregados.
Provas
A respeito do estudo cinético de reações químicas, pode-se afirmar que:
Provas
De acordo com as definições ácido-base, é correto afirmar que:
Provas
Solução tampão é uma solução que atenua as variações de pH quando ocorre a adição de uma base ou de um ácido. É preparada a partir de um par ácido-base conjugado. Um químico pretende preparar uma solução tampão misturando 500 mL de NH3 0,2 molL-1 com 500 mL de NH4Cl 0,02 molL-1. Qual é o valor do pH da solução tampão? Use !$ pK_b \approx 4,7 !$.
Provas
“A localização de um elétron no átomo é descrita por uma função de onda conhecida como orbital atômico. Os orbitais atômicos são designados pelos números quânticos n (principal), !$ \ell !$ (momento angular), !$ m\ell !$ (magnético), e organizam-se em camadas e subcamadas. O elétron possui um número quântico intrínseco a ele, chamado de número quântico magnético de spin (ms)”. Dentre os estados quânticos a seguir, qual é permitido?
Provas
“São eletropositivos, de coloração cinza-prateada e os menos densos da tabela periódica. Reagem vigorosamente em água. A configuração eletrônica da camada de valência é terminada em ns1. São encontrados em compostos na natureza na forma de cátions com estado de oxidação unitário”. Dentre os elementos do grupo da tabela periódica que possuem tais características, podemos citar:
Provas
Em 1911, dois alunos do Prof. Ernest Rutherford realizaram o seguinte experimento para testar o modelo atômico de Thomson: bombardearam uma lâmina de ouro com um feixe de radiação alfa, como mostra a Figura 1.
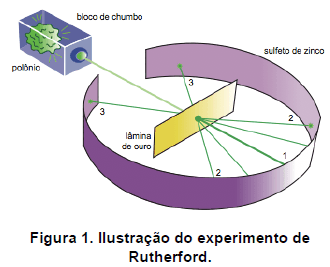
Apenas uma a cada 20 mil partículas alfa (núcleos de hélio) era ricocheteada com ângulos maiores de 90 graus. Nesse experimento, foi utilizada uma lâmina de ouro que é um metal representado por !$ ^{197}_{79} Au !$ . Porém, Rutherford usou também lâminas de outros metais como platina !$ (^{195}_{78} Pt) !$ e alumínio !$ (^{27}_{13} Al) !$. A lâmina de platina apresentou o mesmo resultado observado para a lâmina de ouro. No entanto, não foi possível observar tal fenômeno de deflexão usando uma lâmina de alumínio. Isso se deve ao fato de que:
Provas
Soluções aquosas dos seguintes sais foram preparadas separadamente: Fe2(SO4)3, NaF, Ca(CH3CO2)2 e NH4Cl. O pH de cada solução será, respectivamente:
Provas
Um gás pode apresentar dois comportamentos dependendo das condições de temperatura e pressão, ou seja, ele pode se comportar como um gás ideal ou como um gás real. Esses comportamentos estão relacionados a diferentes modelos utilizados para explicar observações experimentais, e são importantes na indústria para estimar corretamente a pressão que um gás irá exercer dentro do reator. Suponha, como exemplo, o uso de 1500 mols de gás nitrogênio (N2) a 800 K na produção da amônia pelo processo Haber-Bosch. O reator apresenta um volume de 600 L, e suporta uma pressão de até 175 atm. Adotando o modelo do gás real, a pressão exercida no reator pelo gás será de aproximadamente 173 atm. Se o modelo do gás ideal fosse adotado, a pressão exercida seria maior ou menor e com qual diferença numérica em relação à pressão real?
(Dado: R = 0,082 atm.L.mol-1.K-1)
Provas
Caderno Container