Foram encontradas 80 questões.
Considere a representação simplificada dos seguintes decaimentos radioativos conhecidos:
!$ ^{238}_{92} U \xrightarrow {x_1} ^{234}_{90}Th !$
!$ ^{234}_{90} Th \xrightarrow {x_2} ^{234}_{91}Pa !$
!$ ^{222}_{86} Rn \xrightarrow {x_3} ^{218}_{84}Po !$
!$ ^{218}_{84} Po \xrightarrow {x_4} ^{214}_{82}Pb !$
!$ ^{214}_{82} Pb \xrightarrow {x_5} ^{214}_{83}Bi !$
Com relação aos decaimentos acima, é possível afirmar que:
Provas
Uma amostra de 390 g de sulfito de cálcio com 25% de impurezas, em massa, é atacada por ácido clorídrico concentrado em um meio reacional a 2 atm e 300 K. Considere comportamento ideal de gases.
Dados:
• massa molar do enxofre = 32 g.mol-1;
• massa molar do cálcio = 40 g.mol-1; e
• massa molar do oxigênio = 16 g.mol-1.
Pode-se afirmar que o volume, em litros, de anidrido sulforoso obtido pelo consumo completo do sulfito é:
Provas
Considere a célula eletroquímica abaixo:
!$ Pt(s)|H_2(g)|HCl(aq)||Hg_2Cl_2(s)|Hg(l) !$
Admita, ainda, a reação a seguir:
!$ Hg_2Cl_2(s) + H_2(g) \rightarrow 2Hg(l) + 2HCl(aq) !$
O potencial-padrão da célula acima a 294,5 K é +0,2678 V e a 302,5 K é +0,2638 V. Considere que tanto a entalpia, quanto a entropia de reação mudam muito pouco para variações de temperatura não muito amplas. A constante de Faraday é 96500 C.mol-1. A entropia-padrão da reação acima, a 298,15 K, em J.(K.mol)-1, será aproximadamente:
Provas
Bicarbonato de sódio reage estequiometricamente, em processo isotérmico a 300 K, com 50 mL de uma solução aquosa de um ácido monoprótico forte, em um recipiente rígido e fechado que, quando vazio, apresenta um volume útil de 74,9 mL, conforme o esboço abaixo:

O cristal piezoelétrico tem espessura (t) de 2 mm e suscetibilidade voltaica !$ (\Phi) !$ de 0,050 V.(m.Pa)-1 e, quando a reação atinge o equilíbrio, fornece um potencial elétrico (U) de 1,0 V. Considere a solubilidade molar de gases na água desprezível e a constante universal dos gases R = 8,3 J.(mol.K)-1. Se o volume reacional é constante e igual ao volume da solução ácida inicial, a concentração molar inicial da solução do ácido monoprótico, em mol.L-1, é:
Provas
É correto afirmar que:
Provas
Assinale a afirmativa correta sobre as propriedades e características dos polímeros.
Provas
O gráfico qualitativo abaixo ilustra a relação da energia livre de Gibbs molar !$ (G_m) !$ de uma substância pura com a temperatura !$ (T) !$ em seus estados sólido, líquido e gasoso.
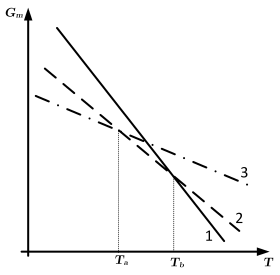
Considere as afirmativas abaixo:
I. As três retas são decrescentes, pois a expressão !$ G_m = H_m - TS_m !$ é representada por uma reta com inclinação definida pelo termo !$ (-S_m) !$.
II. As retas 1, 2 e 3 representam a substância nos estados sólido, líquido e gasoso, respectivamente.
III. A temperatura !$ T_a !$ indica o ponto de fusão da substância nas condições em que o gráfico foi obtido.
IV. Em temperaturas mais altas do que !$ T_b !$, a fase 1 da substância é a mais estável.
Assinale as alternativas que são verdadeiras.
Provas
Na desidratação a alta temperatura de uma mistura reacional composta pelos ácidos fórmico, acético e propiônico, qual a quantidade máxima de diferentes anidridos que poderá ser obtidos?
Provas
Uma reação entre dois líquidos !$ A !$ e !$ B !$ produz dois compostos gasosos !$ C !$ e !$ D !$, de acordo com a estequiometria!$ A + B \rightarrow C + D !$. Se conduzida a pressão e temperatura constantes, pode-se afirmar que:
Provas
Considere a seguinte reação em equilíbrio:
!$ 2SO_2(g) + O_2(g) \rightleftharpoons 2SO_3(g) !$
Dados:
• R = 8,3 J.(K.mol)-1;
• ln 1,6 = 0,47; e
• ln 10 = 2,3.
Sabe-se que a constante de equilíbrio dessa reação é 4,0.1024, a 27 ºC e 2,5.1010, a 227 ºC.
Qual a variação de entalpia padrão da reação, em kJ.mol-1, considerando que ela seja constante nessa faixa de temperatura?
Provas
Caderno Container