Foram encontradas 700 questões.
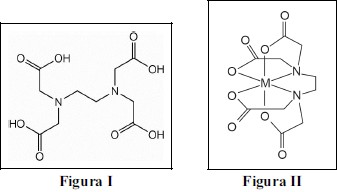
O ácido etilenodiaminotetracético (EDTA), cuja fórmula estrutural é mostrada na figura I acima, é um excelente agente quelante e forma complexos com quase todos os metais. O complexo metal-ligante resultante, no qual a estrutura do EDTA tem forma de gaiola em torno do metal, é mostrado na figura II. O EDTA é um ácido hexaprótico que apresenta os seguintes valores sucessivos de pKa.
pKa1 = 0,0; pKa2 = 1,5; pKa3 = 2,0; pKa4 = 2,68; pKa5 = 6,11; pKa6 = 10,17
Considere que a forma totalmente desprotonada do EDTA seja, para efeito de simplificação, representada pela letra Y.
No que se refere à estrutura do complexo metal-EDTA, mostrada na figura II, assinale a opção correta.
Provas

O ácido etilenodiaminotetracético (EDTA), cuja fórmula estrutural é mostrada na figura I acima, é um excelente agente quelante e forma complexos com quase todos os metais. O complexo metal-ligante resultante, no qual a estrutura do EDTA tem forma de gaiola em torno do metal, é mostrado na figura II. O EDTA é um ácido hexaprótico que apresenta os seguintes valores sucessivos de pKa.
pKa1 = 0,0; pKa2 = 1,5; pKa3 = 2,0; pKa4 = 2,68; pKa5 = 6,11; pKa6 = 10,17
Considere que a forma totalmente desprotonada do EDTA seja, para efeito de simplificação, representada pela letra Y.
Com base nas informações acima, assinale a opção correta.
Provas
A emissão radioativa tem sido usada para a cura de doenças, a obtenção de energia para as naves espaciais, a preservação de alimentos, o acompanhamento de mecanismos de reações etc.
Considerando o decaimento radioativo do !$ ^{22}_{11} \text{ Na} !$ produzindo !$ ^{22}_{10} \text{ Ne} !$, assinale a opção que apresenta a partícula emitida diretamente por esse decaimento.
Provas
O processo industrial mais importante de obtenção de amônia é o processo de Haber, no qual o hidrogênio e o nitrogênio se combinam diretamente, em uma única etapa, segundo a equação a seguir,
N2(g) + 3H2(g) !$ \rightleftharpoons !$ 2NH3(g) + calor.
Para que seja atingido um rendimento de 20% de NH3, essa reação é mantida a alta pressão, aproximadamente 300 atm, e a alta temperatura, cerca de 450 ºC. Ferro e molibdênio são empregados como catalisadores dessa reação.
Assinale a opção correta, considerando as informações fornecidas acima.
Provas
O processo industrial mais importante de obtenção de amônia é o processo de Haber, no qual o hidrogênio e o nitrogênio se combinam diretamente, em uma única etapa, segundo a equação a seguir,
N2(g) + 3H2(g) !$ \rightleftharpoons !$ 2NH3(g) + calor.
Para que seja atingido um rendimento de 20% de NH3, essa reação é mantida a alta pressão, aproximadamente 300 atm, e a alta temperatura, cerca de 450 ºC. Ferro e molibdênio são empregados como catalisadores dessa reação.
Acerca da espontaneidade da reação de obtenção de amônia apresentada acima, assinale a opção correta.
Provas
O processo industrial mais importante de obtenção de amônia é o processo de Haber, no qual o hidrogênio e o nitrogênio se combinam diretamente, em uma única etapa, segundo a equação a seguir,
N2(g) + 3H2(g) !$ \rightleftharpoons !$ 2NH3(g) + calor.
Para que seja atingido um rendimento de 20% de NH3, essa reação é mantida a alta pressão, aproximadamente 300 atm, e a alta temperatura, cerca de 450 ºC. Ferro e molibdênio são empregados como catalisadores dessa reação.
Considerando-se que !$ t !$ representa o tempo, a velocidade !$ v !$ da reação apresentada acima é corretamente descrita por
Provas
O processo industrial mais importante de obtenção de amônia é o processo de Haber, no qual o hidrogênio e o nitrogênio se combinam diretamente, em uma única etapa, segundo a equação a seguir,
N2(g) + 3H2(g) !$ \rightleftharpoons !$ 2NH3(g) + calor.
Para que seja atingido um rendimento de 20% de NH3, essa reação é mantida a alta pressão, aproximadamente 300 atm, e a alta temperatura, cerca de 450 ºC. Ferro e molibdênio são empregados como catalisadores dessa reação.
Na situação acima, considere que as energias de Gibbs molar padrão de formação do NH3, N2 e H2, a 300 K, sejam, respectivamente, -15,6 kJ/mol, 0 kJ/mol e 0 kJ/mol, que R = 8 J/K mol e que !$ \Delta !$G = !$ \Delta !$G0 + RT !$ \ell !$n (Q). Nesse caso, à temperatura de 300 K, o logaritmo neperiano da constante de equilíbrio — !$ \ell !$n (K) — da reação para obtenção de amônia pelo método de Haber é igual a
Provas
O processo industrial mais importante de obtenção de amônia é o processo de Haber, no qual o hidrogênio e o nitrogênio se combinam diretamente, em uma única etapa, segundo a equação a seguir,
N2(g) + 3H2(g) !$ \rightleftharpoons !$ 2NH3(g) + calor.
Para que seja atingido um rendimento de 20% de NH3, essa reação é mantida a alta pressão, aproximadamente 300 atm, e a alta temperatura, cerca de 450 ºC. Ferro e molibdênio são empregados como catalisadores dessa reação.
Com relação à termoquímica envolvida na reação apresentada acima, assinale a opção correta.
Provas
Vários gases produzidos pelas indústrias, quando não são tratados, causam poluição atmosférica. Esses gases, em contato com os gases atmosféricos, formam uma mistura gasosa. A respeito desses gases e de mistura de gases, julgue os seguintes itens, considerando que os gases comportam-se idealmente e que estão a 1 atm e 25 ºC.
Provas
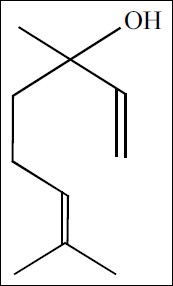
Muitos óleos essenciais são usados em produtos farmacêuticos e de limpeza em alimentos e em bebidas. O linalol, cuja estrutura molecular encontra-se ilustrada na figura acima, é um desses óleos, sendo empregado, principalmente, na preparação de perfumes e cosméticos e, também, na síntese de bactericidas e fungicidas. Na medicina, o linalol tem sido utilizado como sedativo.
Considerando a molécula do linalol apresentada acima, assinale a opção correta com relação à classificação periódica dos elementos.
Provas
Caderno Container