Foram encontradas 50 questões.
O cloreto de lítio é um importante material utilizado na indústria como precursor de lítio metálico e outros sais e óxidos
empregados na fabricação de baterias para veículos elétricos, smartphones etc. A energia de rede é um parâmetro
fundamental que define várias das propriedades químicas de sais. Esse parâmetro pode ser calculado indiretamente
por meio de valores de entalpia experimentais de reações auxiliares. A seguir, são fornecidos alguns dados
termodinâmicos de reações auxiliares para se determinar a energia de rede do cloreto de lítio.
Entalpia de formação do cloreto de lítio: −408 kJ mol–1 Entalpia de formação do cloreto gasoso: −233 kJ mol–1 Entalpia de formação do cloreto aquoso: −167 kJ mol–1 Entalpia de formação do Li+ aquoso: −278 kJ mol–1 1ª Energia de ionização do lítio: 513 kJ mol–1 Afinidade eletrônica do cloro: 348 kJ mol–1 Entalpia de atomização do lítio: 159 kJ mol–1 Entalpia de atomização do cloro: 121 kJ mol–1
Conforme os dados fornecidos, o valor de energia de rede do sal mencionado é mais próximo de:
Entalpia de formação do cloreto de lítio: −408 kJ mol–1 Entalpia de formação do cloreto gasoso: −233 kJ mol–1 Entalpia de formação do cloreto aquoso: −167 kJ mol–1 Entalpia de formação do Li+ aquoso: −278 kJ mol–1 1ª Energia de ionização do lítio: 513 kJ mol–1 Afinidade eletrônica do cloro: 348 kJ mol–1 Entalpia de atomização do lítio: 159 kJ mol–1 Entalpia de atomização do cloro: 121 kJ mol–1
Conforme os dados fornecidos, o valor de energia de rede do sal mencionado é mais próximo de:
Provas
Questão presente nas seguintes provas
A manutenção de aquários e lagos ornamentais requer cuidados com a qualidade da água. Para o uso de água da rede
de saneamento, muitas vezes é necessária a remoção de cloro e cloraminas, que podem levar à morte de peixes e
outros animais, ou mesmo prejudicar o desenvolvimento da biota. Essa remoção pode ser realizada com o uso de
condicionadores baseados em tiossulfato de sódio (Na2S2O3), que reage de forma espontânea com cloro e cloroaminas
para gerar espécies químicas inofensivas. No caso da reação com cloroaminas, esses condicionadores possuem
também aditivos que neutralizam a amônia produzida na reação. Considere a remoção de cloro de uma amostra e os
diagramas de Latimer a seguir.
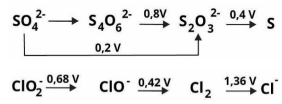
A reação, que provoca o condicionamento da água da rede de saneamento própria para uso, possui a diferença de potencial padrão de:

A reação, que provoca o condicionamento da água da rede de saneamento própria para uso, possui a diferença de potencial padrão de:
Provas
Questão presente nas seguintes provas
Atualmente, existe uma grande procura por novas tecnologias de conversão de energia. As células a combustível de
metanol direto (DMFCs) são uma promissora tecnologia em que a principal vantagem é a operação em baixa
temperatura e a facilidade de transporte do combustível. Essas células utilizam uma solução de metanol (3 mol L–1)
que reage em uma camada catalítica para formar dióxido de carbono. A água é consumida no ânodo, e os íons H+ são
transportados através da membrana de troca de prótons até o cátodo, onde reagem com o oxigênio para produzir água.
A seguir são mostradas as equações das semirreações desse processo. Os elétrons são transportados por meio de
um circuito externo do ânodo para o cátodo, fornecendo energia aos dispositivos conectados.
CH3OH + H2O → 6 H+ + 6 e− + CO2 (ânodo) O2 + 4 H+ + 4 e− → 2 H2O (cátodo)
Devido às características de operação e restrições, essas células operam com potências de saída da ordem de 0,3 kW. Para um sistema projetado para fornecer 24 V, a corrente que passa pelo circuito é de 12,5 A.
Dado: ℱ = 96.500 C mol–1.
Considerando que o sistema acima descrito opere por um período de 100 horas, qual é o valor mais próximo do volume, em litros, de solução de metanol consumido?
CH3OH + H2O → 6 H+ + 6 e− + CO2 (ânodo) O2 + 4 H+ + 4 e− → 2 H2O (cátodo)
Devido às características de operação e restrições, essas células operam com potências de saída da ordem de 0,3 kW. Para um sistema projetado para fornecer 24 V, a corrente que passa pelo circuito é de 12,5 A.
Dado: ℱ = 96.500 C mol–1.
Considerando que o sistema acima descrito opere por um período de 100 horas, qual é o valor mais próximo do volume, em litros, de solução de metanol consumido?
Provas
Questão presente nas seguintes provas
O éster diisononílico do ácido 1,2-ciclohexanodicarboxílico (DINC) é um importante plastificante não baseado em ftalatos, usado na
fabricação de artigos de plástico flexíveis em áreas de aplicação sensíveis, como brinquedos, dispositivos médicos e embalagens
de alimentos. Esse composto pode ser obtido por uma sequência de reações, que parte do ácido fumárico (ácido 2-butenodióico,
M = 116 g mol–1) para formar um derivado do ciclohexeno na etapa I, cujo rendimento é de 80%, seguida de hidrogenação obtida de
forma quantitativa e, por fim, esterificação com 1-nonanol (M = 144 g mol–1), com rendimento de 90%, conforme mostrado no
esquema a seguir.
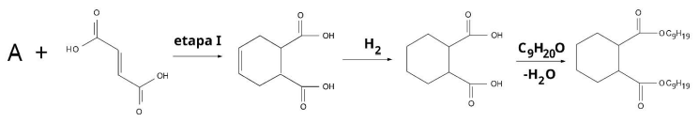
Dados: Massa molar (g mol–1): C = 12, O = 16, H = 1.
Provas
Questão presente nas seguintes provas
O éster diisononílico do ácido 1,2-ciclohexanodicarboxílico (DINC) é um importante plastificante não baseado em ftalatos, usado na
fabricação de artigos de plástico flexíveis em áreas de aplicação sensíveis, como brinquedos, dispositivos médicos e embalagens
de alimentos. Esse composto pode ser obtido por uma sequência de reações, que parte do ácido fumárico (ácido 2-butenodióico,
M = 116 g mol–1) para formar um derivado do ciclohexeno na etapa I, cujo rendimento é de 80%, seguida de hidrogenação obtida de
forma quantitativa e, por fim, esterificação com 1-nonanol (M = 144 g mol–1), com rendimento de 90%, conforme mostrado no
esquema a seguir.

Dados: Massa molar (g mol–1): C = 12, O = 16, H = 1.
Provas
Questão presente nas seguintes provas
O eletrodo de referência prata-cloreto de prata é amplamente usado em medidas eletroquímicas, por exemplo, em
sistemas de controle de corrosão por proteção catódica em ambientes costeiros, e é uma alternativa aos eletrodos de
calomelano, que têm riscos ambientais. Ele consiste em um fio de prata recoberto por uma fina camada de cloreto de
prata mergulhado numa solução eletrolítica. Para que o potencial de eletrodo não varie, a concentração de íons prata
deve ser constante. Considere que um fio é recoberto por uma camada de 1,0 mg de cloreto de prata e está imerso
em 0,1 mL de uma solução 3 mol L–1 de cloreto de sódio.
Dados: Massas molares (g mol–1): Ag = 107; Cl = 35,5. KPS (AgCl) = 1,8 x 10–10.
Na situação descrita, a concentração de prata, em mol L–1, na solução é de:
Dados: Massas molares (g mol–1): Ag = 107; Cl = 35,5. KPS (AgCl) = 1,8 x 10–10.
Na situação descrita, a concentração de prata, em mol L–1, na solução é de:
Provas
Questão presente nas seguintes provas
O diagrama de Hommel (NFPA 704) é constituído de quatro regiões identificadas pelas cores vermelho
(inflamabilidade), azul (risco à saúde), amarelo (reatividade) e branco (riscos específicos) e números que variam
de 0 (nenhum risco) a 4 (risco extremo). Esse código é usado para informar de maneira simples e objetiva os riscos
oferecidos pelos materiais. Desse modo, o profissional define quais precauções deve tomar e os EPIs que deve usar,
além de quais procedimentos devem ser realizados em um acidente. Considere o manuseio de acetona, ácido sulfúrico
e tolueno.
Os valores associados às regiões vermelha e azul nos diagramas desses três materiais são, respectivamente:
Os valores associados às regiões vermelha e azul nos diagramas desses três materiais são, respectivamente:
Provas
Questão presente nas seguintes provas
Para análise da qualidade de águas, um dos mais importantes parâmetros é a dureza total (GH). Os testes comerciais se baseiam
na análise colorimétrica, e a maioria deles utiliza o método de titulação complexométrica empregando negro de eriocromo T, que
atua também como indicador, e edta (H4edta = ácido etilenodiaminatetraacético, M = 292 g mol–1) em meio de tampão pH 10. A
solução do ânion do eriocromo T possui cor azul quando livre e se converte em rosa/vermelho ao ser complexada com Ca2+. Já o
complexo metálico com edta é mais estável que com o eriocromo T. Assim, ao adicionar este ligante, o ânion eriocromo T é
deslocado, conforme ilustrado nas duas equações de equilíbrio a seguir. No ponto de viragem, o excesso de edta promove a
conversão da cor da solução em azul.
(eriocromo T)2– + Ca2+ ⇌ [Ca(eriocromo T)] (I)
[Ca(eriocromo T)] + edta4– ⇌ [Ca(edta)]2– + (eriocromo T)2– (II)
Os testes de dureza são ajustados para que o operador separe uma amostra de 5 mL da água a ser analisada, adicione uma
quantidade certa de indicador e tampão e, por fim, adicione gota a gota a solução de edta até o ponto de viragem. A quantidade de
gotas corresponde a quantas unidades de dGH a amostra possui. Cada gota possui um volume de 0,05 mL. Águas moles apresentam
valores de até 70 dGH, enquanto acima de 200 dGH são consideradas águas duras. Cada unidade de dGH corresponde a 17,9 ppm
de carbonato de cálcio (M = 100 g mol–1).
Provas
Questão presente nas seguintes provas
Para análise da qualidade de águas, um dos mais importantes parâmetros é a dureza total (GH). Os testes comerciais se baseiam
na análise colorimétrica, e a maioria deles utiliza o método de titulação complexométrica empregando negro de eriocromo T, que
atua também como indicador, e edta (H4edta = ácido etilenodiaminatetraacético, M = 292 g mol–1) em meio de tampão pH 10. A
solução do ânion do eriocromo T possui cor azul quando livre e se converte em rosa/vermelho ao ser complexada com Ca2+. Já o
complexo metálico com edta é mais estável que com o eriocromo T. Assim, ao adicionar este ligante, o ânion eriocromo T é
deslocado, conforme ilustrado nas duas equações de equilíbrio a seguir. No ponto de viragem, o excesso de edta promove a
conversão da cor da solução em azul.
(eriocromo T)2– + Ca2+ ⇌ [Ca(eriocromo T)] (I)
[Ca(eriocromo T)] + edta4– ⇌ [Ca(edta)]2– + (eriocromo T)2– (II)
Os testes de dureza são ajustados para que o operador separe uma amostra de 5 mL da água a ser analisada, adicione uma
quantidade certa de indicador e tampão e, por fim, adicione gota a gota a solução de edta até o ponto de viragem. A quantidade de
gotas corresponde a quantas unidades de dGH a amostra possui. Cada gota possui um volume de 0,05 mL. Águas moles apresentam
valores de até 70 dGH, enquanto acima de 200 dGH são consideradas águas duras. Cada unidade de dGH corresponde a 17,9 ppm
de carbonato de cálcio (M = 100 g mol–1).
Provas
Questão presente nas seguintes provas
Recentemente, cientistas identificaram na Antártida as mais antigas bolhas de ar já descobertas, presas no gelo a
profundidades entre 100 e 200 metros. A datação dessas amostras foi realizada por meio de medidas de isótopos de
argônio. O argônio possui 26 isótopos conhecidos. Na atmosfera, o 40Ar compõe 99,6% do argônio natural. O isótopo
radioativo de maior tempo de meia-vida é o 39Ar, com aproximadamente 300 anos.
Uma amostra, que foi datada de 3000 anos, deve apresentar, em relação à quantidade inicial (m0), uma quantidade desse isótopo radioativo de maior tempo de meia-vida igual a:
Uma amostra, que foi datada de 3000 anos, deve apresentar, em relação à quantidade inicial (m0), uma quantidade desse isótopo radioativo de maior tempo de meia-vida igual a:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container