Foram encontradas 50 questões.
Em 1999, o Laboratório Nacional Lawrence Berkeley (EUA) anunciou a descoberta dos elementos superpesados de
números atômicos 116 e 118. Porém, mais tarde, descobriu-se que as evidências haviam sido forjadas por um de seus
cientistas, e o trabalho científico teve que ser retratado. Um ano depois, pesquisadores do Centro Conjunto
Internacional de Pesquisa Nuclear, na Rússia, liderados por Yuri Oganessian, em parceria com Laboratório Nacional
Lawrence Livermore nos EUA, descobriram esses dois novos elementos, os quais foram nomeados livermório (116Lv)
e oganésson (118Og), em homenagem ao laboratório e ao pesquisador líder, respectivamente. Og é atualmente o último
elemento da tabela periódica. Ambos os elementos superpesados foram sintetizados por meio do bombardeamento
de elementos actinídeos (An) por íons do isótopo Ca-48, conforme esquemas I e II. O Og também decai radioativamente
e produz Lv, como mostrado no esquema III.
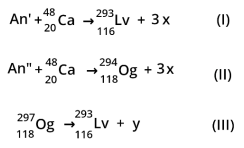
Nos esquemas, os actinídeos An’ e An” e as partículas x e y são, respectivamente:
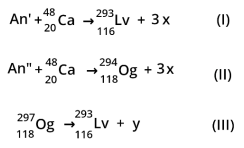
Nos esquemas, os actinídeos An’ e An” e as partículas x e y são, respectivamente:
Provas
Questão presente nas seguintes provas
Um químico recém-contratado em uma empresa encontrou no laboratório balões volumétricos de 250 mL, os quais
estavam rotulados como: i) resíduo contendo acetona; ii) resíduo contendo ácido acético; iii) resíduo contendo ácido
nítrico; iv) resíduo contendo cloreto férrico; v) resíduo contendo peróxido de hidrogênio. A fim de encaminhar esses
resíduos de maneira correta (separando aquosos, metais pesados, organoclorados etc.) e segura, o profissional irá
transferir os conteúdos para bombonas plásticas de modo a descartá-los e liberar os balões volumétricos para uso.
Para tanto, o profissional decidiu usar quatro bombonas diferentes:
Provas
Questão presente nas seguintes provas
Pesquisadores do Instituto de Química da Unesp criaram um método prático, rápido e barato para identificar
falsificação de combustíveis e bebidas. Esse teste foi amplamente divulgado pela imprensa em função dos casos de
intoxicação por metanol em bebidas e da adulteração de combustível em postos. O teste se baseia no método
colorimétrico, em que um sal é adicionado à amostra. Caso haja metanol, o sal converte o metanol em formol. Em
seguida, é adicionado o revelador, ácido cromotrópico, que reage com formol para formar um composto de cor
púrpura. Um sistema baseado nesse método gerou a paleta de cores em função do teor de metanol, mostrada no
quadro a seguir.
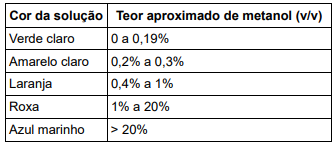
Para simular uma contaminação, um investigador usou uma garrafa de vidro vazia e seca, de 750 mL, com massa de 348,0 g. Essa garrafa foi enxaguada por dentro com etanol combustível adulterado com 50% de metanol. Após verter o conteúdo do enxágue, a massa da garrafa molhada foi de 350,4 g. A garrafa foi então preenchida com etanol de laboratório padrão para análise até completar 750 mL. Por fim, uma alíquota do conteúdo da garrafa foi submetida ao teste.
Dados: Densidade etanol = densidade metanol = 0,79 g mol–1.
Considerando a simulação descrita no texto, o teste de análise deve resultar em qual cor?

Para simular uma contaminação, um investigador usou uma garrafa de vidro vazia e seca, de 750 mL, com massa de 348,0 g. Essa garrafa foi enxaguada por dentro com etanol combustível adulterado com 50% de metanol. Após verter o conteúdo do enxágue, a massa da garrafa molhada foi de 350,4 g. A garrafa foi então preenchida com etanol de laboratório padrão para análise até completar 750 mL. Por fim, uma alíquota do conteúdo da garrafa foi submetida ao teste.
Dados: Densidade etanol = densidade metanol = 0,79 g mol–1.
Considerando a simulação descrita no texto, o teste de análise deve resultar em qual cor?
Provas
Questão presente nas seguintes provas
Em 2025 houve um aumento muito grande de casos de intoxicação por metanol, especialmente no estado de São Paulo.
Os sintomas da intoxicação aparecem em até 12 horas, e a substância age na medula e no cérebro, causando confusão
mental, lesão no nervo óptico, acidose no sangue e respiratória. Com a ingestão do metanol, em vez de metabolizá-lo
em substâncias facilmente processadas, o fígado o converte em compostos ainda mais perigosos, capazes de
provocar cegueira e de levar à morte, como o formaldeído e o ácido fórmico.
A qual classe pertence a reação mencionada no texto, que converte o metanol em compostos mais perigosos?
A qual classe pertence a reação mencionada no texto, que converte o metanol em compostos mais perigosos?
Provas
Questão presente nas seguintes provas
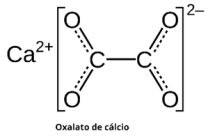
Além de alcaloides, muitas plantas são tóxicas por conter oxalato de cálcio (M = 128 g mol–1). As beladonas e a
comigo-ninguém-pode são altamente tóxicas devido à presença desse composto na forma cristalina de ráfides (agulhas), que são
perfurantes. Quando em contato com a pele e/ou mucosas, podem causar lesões e, em casos mais sérios, asfixia, podendo levar a
óbito devido à obstrução das vias aéreas. No entanto, outras folhas, como espinafre, são ricas em oxalato, mas nesse caso o
composto se encontra na forma cristalina de drusas e prismas pequenos, que não são tóxicos.
5 C2O4 2−(aq) + 2 MnO4 −(aq) + 16 H+(aq) → 10 CO2(g) + 2 Mn2+(aq) + 8H2O(l)
Considerando os dados descritos da análise, a quantidade de oxalato, em miligramas, por 100 g de folha seca, é mais próxima de:
Provas
Questão presente nas seguintes provas
Além de alcaloides, muitas plantas são tóxicas por conter oxalato de cálcio (M = 128 g mol–1). As beladonas e a
comigo-ninguém-pode são altamente tóxicas devido à presença desse composto na forma cristalina de ráfides (agulhas), que são
perfurantes. Quando em contato com a pele e/ou mucosas, podem causar lesões e, em casos mais sérios, asfixia, podendo levar a
óbito devido à obstrução das vias aéreas. No entanto, outras folhas, como espinafre, são ricas em oxalato, mas nesse caso o
composto se encontra na forma cristalina de drusas e prismas pequenos, que não são tóxicos.
Provas
Questão presente nas seguintes provas
Conhecido como “falsa couve”, o caso recente de pessoas que ingeriram uma espécie venenosa de folha de seu jardim
reacendeu o alerta sobre os perigos de plantas comuns de jardim. As pessoas foram intoxicadas por ingerir folhas
de Nicotiana glauca, que são similares às da couve, mas que contêm alcaloides tóxicos, que atacam o sistema nervoso,
dentre os quais se destaca a anabasina. Outras plantas ornamentais comuns em jardim, como beladonas e lírio
trombeta, também contêm alcaloides, como a atropina, e sua ingestão pode provocar convulsões e até parada
respiratória. As estruturas da anabasina e da atropina são:
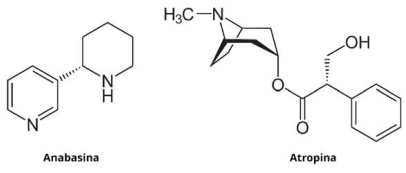
Qual função orgânica é comum nos compostos tóxicos mencionados no texto?

Qual função orgânica é comum nos compostos tóxicos mencionados no texto?
Provas
Questão presente nas seguintes provas
Os lantanídeos (Ln) estão sendo considerados estratégicos para as economias, devido às diversas aplicações em tecnologias
aeroespaciais, de defesa, energia, telecomunicações, eletrônica e transporte. Esses elementos estão contidos no bloco f da tabela
periódica e localizados na coluna do grupo 3, na família dos metais de transição junto com escândio e ítrio, apesar de haver
divergências entre os cientistas sobre a presença dos lantanídeos nesse grupo. De todo modo, esse grupo da tabela corresponde
ao das terras raras, uma vez que escândio e ítrio são encontrados nos mesmos minérios que os lantanídeos. Quando formam
compostos minerais, os cátions de todos elementos do grupo 3 possuem o estado de oxidação +3. O Brasil possui a segunda maior
reserva de minérios de terras raras e, para alcançar maior valor agregado, necessita desenvolver tecnologias de processamento dos
minérios para a separação e purificação desses metais. Geralmente e de modo simplificado, o processamento ocorre em etapas em
que o minério é triturado e tratado em altas temperaturas com ácido sulfúrico para alterar as fases minerais e torná-las solúveis. Em
seguida, com resfriamento, vão se formando os óxidos dos metais separadamente. Para obtenção do metal, esses óxidos são
fundidos e colocados em células onde são submetidos a corrente e potencial elétricos.
Provas
Questão presente nas seguintes provas
Os lantanídeos (Ln) estão sendo considerados estratégicos para as economias, devido às diversas aplicações em tecnologias
aeroespaciais, de defesa, energia, telecomunicações, eletrônica e transporte. Esses elementos estão contidos no bloco f da tabela
periódica e localizados na coluna do grupo 3, na família dos metais de transição junto com escândio e ítrio, apesar de haver
divergências entre os cientistas sobre a presença dos lantanídeos nesse grupo. De todo modo, esse grupo da tabela corresponde
ao das terras raras, uma vez que escândio e ítrio são encontrados nos mesmos minérios que os lantanídeos. Quando formam
compostos minerais, os cátions de todos elementos do grupo 3 possuem o estado de oxidação +3. O Brasil possui a segunda maior
reserva de minérios de terras raras e, para alcançar maior valor agregado, necessita desenvolver tecnologias de processamento dos
minérios para a separação e purificação desses metais. Geralmente e de modo simplificado, o processamento ocorre em etapas em
que o minério é triturado e tratado em altas temperaturas com ácido sulfúrico para alterar as fases minerais e torná-las solúveis. Em
seguida, com resfriamento, vão se formando os óxidos dos metais separadamente. Para obtenção do metal, esses óxidos são
fundidos e colocados em células onde são submetidos a corrente e potencial elétricos.
Provas
Questão presente nas seguintes provas
Os lantanídeos (Ln) estão sendo considerados estratégicos para as economias, devido às diversas aplicações em tecnologias
aeroespaciais, de defesa, energia, telecomunicações, eletrônica e transporte. Esses elementos estão contidos no bloco f da tabela
periódica e localizados na coluna do grupo 3, na família dos metais de transição junto com escândio e ítrio, apesar de haver
divergências entre os cientistas sobre a presença dos lantanídeos nesse grupo. De todo modo, esse grupo da tabela corresponde
ao das terras raras, uma vez que escândio e ítrio são encontrados nos mesmos minérios que os lantanídeos. Quando formam
compostos minerais, os cátions de todos elementos do grupo 3 possuem o estado de oxidação +3. O Brasil possui a segunda maior
reserva de minérios de terras raras e, para alcançar maior valor agregado, necessita desenvolver tecnologias de processamento dos
minérios para a separação e purificação desses metais. Geralmente e de modo simplificado, o processamento ocorre em etapas em
que o minério é triturado e tratado em altas temperaturas com ácido sulfúrico para alterar as fases minerais e torná-las solúveis. Em
seguida, com resfriamento, vão se formando os óxidos dos metais separadamente. Para obtenção do metal, esses óxidos são
fundidos e colocados em células onde são submetidos a corrente e potencial elétricos.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container