Foram encontradas 115 questões.
O ferro é um dos elementos mais abundantes da crosta terrestre, e sua distribuição eletrônica pode ser descrita como [Ar] 3d6 4s2 . Entretanto, este elemento ocorre mais frequentemente na forma de dois íons: o Fe2+ e o Fe3+. As estruturas eletrônicas destes dois íons são descritas, respectivamente, como:
Provas
Questão presente nas seguintes provas
Observe os valores de pKa para os ácidos conjugados dos compostos abaixo.
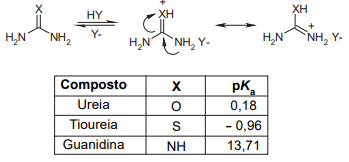
A partir destes dados, conclui-se que a
Provas
Questão presente nas seguintes provas
As baterias de Ag/Zn são formadas por óxido de prata, zinco metálico e uma solução aquosa de um hidróxido de metal alcalino, como o KOH. A esse respeito, analise as semirreações abaixo.
!$ Zn^{2+} + 2 e^- \rightleftharpoons Zn \ E'^o= - 0,76V \\ Ag^+ e^- \rightleftharpoons \ E'^o= 0,80V !$
Com base nessas semirreações, pode-se afirmar, corretamente, que
Provas
Questão presente nas seguintes provas
Diversos compostos organometálicos são empregados em síntese orgânica, sendo muito úteis em metodologias de construção de ligações carbono-carbono. Nestes compostos, o átomo de carbono tem caráter nucleofílico, e a ligação carbono-metal pode ter maior caráter covalente ou iônico. Organolitiados (ligação C-Li) e organomagnesianos (ligação C-MgX) são muito empregados, enquanto o uso de organosódios (C-Na) é raro. A partir desses dados, está correto afirmar que o(s)
Provas
Questão presente nas seguintes provas
A rancificação hidrolítica (formação de ácidos graxos a partir da hidrólise de triglicerídeos) em alimentos pode ser avaliada por titulometria de neutralização, empregando uma solução básica de concentração conhecida, sendo que o teor máximo de acidez aceitável para consumo humano é de 3 mmol% (3 mmol em 100 g de material). Uma amostra de manteiga foi analisada da seguinte forma: 100 g deste alimento foram fundidos e, após a separação das fases, 5 g da camada gordurosa foram transferidos para um erlenmeyer e dissolvidos em 40 mL de uma mistura etanoléter etílico (1:2) previamente neutralizada com solução de NaOH 0,1 mol/L. Após essa etapa, adicionaram-se algumas gotas de solução de fenolftaleína e gotejou-se, através de uma bureta, solução de NaOH 0,12 mol/L até o surgimento de coloração rósea persistente, sendo que, para isso, foram gastos 0,85 mL dessa solução. Com base neste experimento, pode-se afirmar, corretamente, que a(o)
Provas
Questão presente nas seguintes provas
Observe o esquema abaixo.
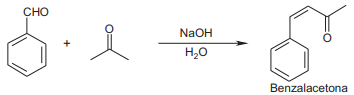
Esta reação é uma condensação aldólica, em que o meio básico gera um carbânion a partir da acetona, que, por sua vez, reage preferencialmente com o benzaldeído. Isto acontece porque o(a)
Provas
Questão presente nas seguintes provas
A redução de 2-isopropilciclo-hexanona pelo complexo borana-THF, empregando tetra-hidrofurano (THF) como solvente, gera dois produtos, sendo um deles denominado principal por ser formado em maior proporção que o outro.
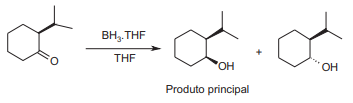
Analisando esta reação, considere as afirmações a seguir. O produto principal tem estereoquímica relativa cis, devido ao ataque nucleofílico do agente redutor pela face do anel ciclo-hexano oposta àquela onde se localiza a cadeia isopropila.
PORQUE
esta cadeia exerce um impedimento estereoeletrônico desta face, favorecendo a aproximação do nucleófilo pela face oposta. A esse repeito, conclui-se que
Provas
Questão presente nas seguintes provas
O ângulo de ligação H-C-H no metano é de 109,5°, enquanto que o ângulo H-N-H na amônia é de 108° e o ângulo H-O-H na água é de 104,5°. Esta variação pode ser explicada pelo(a )
Provas
Questão presente nas seguintes provas
Um aluno de Química, durante o desenvolvimento de seu projeto de curso, precisa acompanhar a formação de álcool 4-nitrobenzílico a partir da redução de 4-nitrobenzaldeído, com hidreto de boro e sódio em metanol.
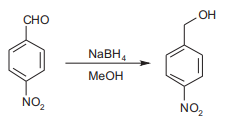
Como método para este acompanhamento, ele escolheu a cromatografia líquida de alta eficiência (CLAE ), empregando uma coluna de fase reversa (octadecilsilano) como fase estacionária, uma mistura de acetonitrila e água como fase móvel e detector de absorção de luz ultravioleta (254 nm). Após quinze minutos de reação, o aluno injetou uma alíquota da reação, obtendo o seguinte cromatograma:
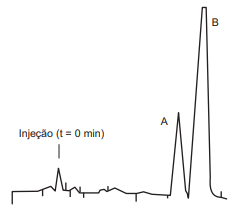
Após interpretar o cromatograma, o aluno levantou as hipóteses a seguir.
I – O pico A corresponde ao 4-nitrobenzaldeído, já que, por ser mais polar que o álcool 4-nitrobenzílico, terá menor tempo de retenção em uma coluna de fase reversa.
II – Apesar de a reação não estar finalizada, ela está próxima do final, já que há dois picos no cromatograma, e a concentração do produto é maior que a do reagente.
III – A escolha do comprimento de onda de 254 nm pode ser justificada pelo fato de o cromóforo principal, nos dois compostos em questão, ser o mesmo, possibilitando a análise em um único comprimento de onda.
É(São) correta(s) APENAS a(s) hipótese(s)
Provas
Questão presente nas seguintes provas
A cadeia respiratória e a fermentação lática são dois processos metabólicos que dependem da produção de piruvato a partir da glicose. Ao longo destes processos, são sintetizadas moléculas de ATP, que atuam como reservatório de energia química para os processos celulares, e espécies redutoras como NADH2+ e FADH. Na cadeia respiratória, o oxigênio molecular (O2 ) é convertido em água, enquanto que, na fermentação lática, o piruvato dá origem ao lactato.
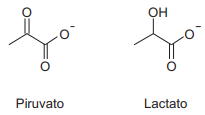
Em relação a estes processos bioquímicos, são feitas as afirmativas a seguir.
I – O piruvato e o oxigênio são aceptores finais de elétrons na fermentação lática e na cadeia respiratória, respectivamente, sendo reduzidos por NADH2 + e/ou FADH.
II – A redução do piruvato e do O2 permite a continuidade dos ciclos intracelulares de produção de energia, já que regeneram NAD+ e FAD, cofatores de disponibilidade limitada na célula.
III – Na ausência de O2 , a célula pode utilizar piruvato como aceptor final de elétrons na cadeia respiratória, mantendo ativo o ciclo de produção celular de ATP.
É(São) correta(s) APENAS a(s) afirmativa(s)
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container