Foram encontradas 2.648 questões.
O gráfico abaixo representa a velocidade de um paraquedista desde um instante t0 até um instante t3
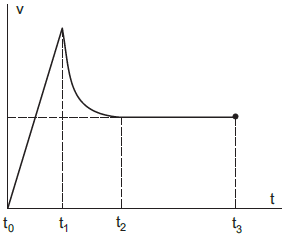
O instante de abertura do paraquedas e os dois intervalos de tempo em que, no movimento, há aceleração não nula são, respectivamente,
Provas
Questão presente nas seguintes provas
Um jovem brasileiro que passava seis meses na cidade de Toronto, no Canadá, em um programa de intercâmbio estudantil, decide aprender a esquiar. Para tal, comprou equipamentos e roupas a fim de se preparar para o rigoroso inverno da cidade. Dentre os itens, adquiriu uma roupa especial que possui 2,7 m2 de área total e 9 mm de espessura. Sabendo que tal roupa foi confeccionada com um material de condutibilidade térmica igual a 6, 0 x 10–5 cal.s–1.cm–1. °C–1, que a temperatura corporal, no dia da atividade esportiva, era 37°C e a temperatura ambiente era –13 °C, a quantidade de calor, em calorias, conduzida através do tecido durante 5 minutos, nesse dia, foi de
Provas
Questão presente nas seguintes provas
O gráfico abaixo representa a potência de uma fonte térmica em função da temperatura de um bloco de 200 g de massa, inicialmente a 20 ºC, que fica exposto a essa fonte durante 40 s, e, ao final, atinge a temperatura de 70ºC.
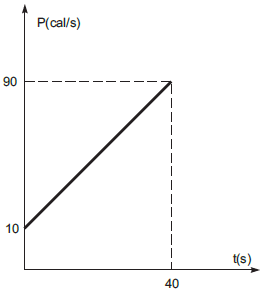
Sabe-se que, durante o intervalo de tempo representado no gráfico, todo o calor produzido pela fonte térmica é utilizado no aquecimento do bloco. Com base nessas informações, o calor específico da substância que constitui o referido corpo, em cal/g.ºC, vale
Provas
Questão presente nas seguintes provas
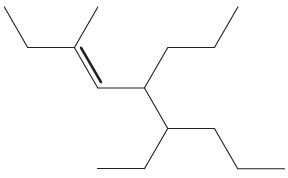
Segundo a IUPAC, a nomenclatura do hidrocarboneto acima é
Provas
Questão presente nas seguintes provas

Analisando os monoterpenos I, II e III ilustrados acima, conclui-se que
Provas
Questão presente nas seguintes provas
O gás natural possui uma quantidade variável de gás carbônico e gás sulfídrico. O CO2 é indesejável, já que reduz o poder calorífico do gás natural e dificulta o transporte do mesmo sob baixas temperaturas e alta pressão, pois solidifica. Já o gás sulfídrico é extremamente venenoso e corrosivo frente aos equipamentos metálicos. Uma das técnicas utilizadas para retirar esses contaminates gasosos é a absorção física, onde o gás natural passa pelo solvente polietilenoglicol sob altas pressões e baixa temperatura, sendo seletivamente absorvido pelo polímero. O polímero absorvente é sintetizado a partir do óxido de etileno em meio ácido, de acordo com a reação abaixo.
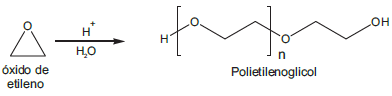
O polietilenoglicol é
Provas
Questão presente nas seguintes provas
Três cubas eletrolíticas ligadas em série, munidas de eletrodos de platina, contêm, respectivamente, soluções aquosas de sulfato cúprico, ácido sulfúrico e nitrato de prata. Após certo tempo de passagem de corrente elétrica, a eletrólise foi interrompida. Sabendo-se que 1,35 g de cobre foi depositado na primeira cuba, analise as afirmativas a seguir.
I – A quantidade de prata depositada na terceira cuba é 4,59 g.
II – Há produção de gás oxigênio apenas na segunda cuba.
III – A quantidade de ácido sulfúrico permanece constante na segunda cuba.
IV – O volume de oxigênio produzido, nas CNTP, na segunda cuba, é de 0,24 L.
Dado: Volume molar dos gases na CNTP = 22,4 L.mol–1
Estão corretas APENAS as afirmativas
Provas
Questão presente nas seguintes provas
O besouro-bombardeiro, cujo nome científico é Brachynus crepitans, possui, no seu abdômen, dois compartimentos distintos que armazenam hidroquinona e peróxido de hidrogênio. Quando ele se sente ameaçado, essas substâncias se misturam e, através de uma catálise enzimática, há a formação de p-benzoquinona, que é expelida sob a forma de uma solução quente, de acordo com a reação abaixo.
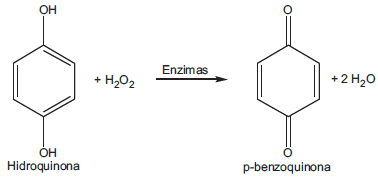
Nessa reação de oxirredução,
Provas
Questão presente nas seguintes provas
Considere que uma solução aquosa de ácido clorídrico reagiu com os seguintes reagentes:
• solução de tiossulfato de sódio;
• dióxido de manganês;
• carbonato de cálcio;
• zinco metálico.
Sobre essas reações, analise as afirmativas a seguir.
I – O ácido clorídrico atua como agente oxidante do tiossulfato na reação Na2S2O3(aq)+2 HCl(aq) !$ \rightarrow !$ 2 NaCl(aq)+ SO2(g)+H2O(!$ \ell !$)+S(s)
II – O dióxido de manganês atua como agente oxidante do cloreto na reação MnO2(s) + 4 HCl(aq) !$ \rightarrow !$ MnCl2(aq) + Cl2(g) + 2 H2O(!$ \ell !$)
III – O carbonato de cálcio é oxidado pelo ácido clorídrico na reação CaCO3 (s) + 2 HCl(aq) !$ \rightarrow !$ CaCl2 (aq) + CO2(g) + H2O(!$ \ell !$)
IV – O zinco metálico é oxidado pelo ácido clorídrico na reação Zn(s) + 2 HCl(aq) !$ \rightarrow !$ ZnCl2(aq) + H2(g)
Estão corretas APENAS as afirmativas
Provas
Questão presente nas seguintes provas
O peróxido de hidrogênio, sob o ponto de vista de reações de oxidação e redução, é um composto bastante versátil já que pode atuar como agente redutor ou oxidante. A reação entre soluções de peróxido de hidrogênio e de dicromato de potássio em meio ácido pode ser utilizada para caracterização do peróxido de hidrogênio.
O teste envolve a observação do composto CrO5 em fase orgânica, uma vez que esse composto é altamente instável em meio aquoso. Caso o solvente orgânico não seja adicionado, observam-se a coloração característica dos íons cromo III e a liberação de gás oxigênio.
A equação devidamente balanceada da reação entre as soluções de peróxido de hidrogênio e de dicromato de potássio em meio ácido, sem adição de solvente orgânico, é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container