Foram encontradas 2.000 questões.
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em uma bancada de laboratório há dois frascos: um deles contém 50 mL de uma solução aquosa 2 mol/L de hidróxido de sódio, e o outro contém 200 mL de uma solução aquosa 0,4 g/L hidróxido de sódio. Ao se misturarem as duas soluções, o volume final é de 250 mL e o valor aproximado da concentração de NaOH, em mol/L, da solução resultante é
Dado MM(NaOH) = 40 g/mol
Dado MM(NaOH) = 40 g/mol
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
Considere um experimento em que, no meio aquoso, o NaOH reage por completo com o H2SO4 , segundo a equação:
2NaOH(aq) + H2 SO4(aq) → 2H2 O(l) + Na2 SO4(aq)
Nesse experimento, a massa, em gramas, de NaOH que reage por completo com 2,94 g de H2 SO4 é
2NaOH(aq) + H2 SO4(aq) → 2H2 O(l) + Na2 SO4(aq)
Nesse experimento, a massa, em gramas, de NaOH que reage por completo com 2,94 g de H2 SO4 é
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Considere as equações I, II e III apresentadas abaixo, que traduzem o comportamento do H3 PO4 como ácido triprótico na água.

De acordo com o conceito ácido-base de Bronsted e Lowry, na equação

De acordo com o conceito ácido-base de Bronsted e Lowry, na equação
Provas
Questão presente nas seguintes provas
Sulfato de bário é um sal muito pouco solúvel em água. Esse sal, em solução saturada, encontra-se na seguinte situação de equilíbrio:

Sendo o seu produto de solubilidade a 25 º C igual a 1,0 x 10-10 , em solução saturada, a concentração de Ba 2+ , em mol/L, é

Sendo o seu produto de solubilidade a 25 º C igual a 1,0 x 10-10 , em solução saturada, a concentração de Ba 2+ , em mol/L, é
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Transformações Químicas e EnergiaTermoquímica
A reação de queima do enxofre em atmosfera de oxigênio é indicada na equação abaixo.
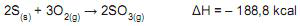
Considerando-se que há excesso de oxigênio e que ocorre reação completa, o valor do calor, em kcal, liberado na formação de 10 mol de SO 3(g) é
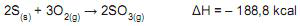
Considerando-se que há excesso de oxigênio e que ocorre reação completa, o valor do calor, em kcal, liberado na formação de 10 mol de SO 3(g) é
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Transformações Químicas e EnergiaEletroquímica
A 60 mL de solução aquosa de SnCl2 0,10 mol/L juntamos 40 mL de solução FeCl3 0,80 mol/L e água suficiente para levar a solução a 500 mL. Considere que se trata de uma reação de oxirredução representada pela equação abaixo e que um dos reagentes está em excesso.
SnCl2(aq) + 2 FeCl3(aq) → SnCl4(aq)+ 2 FeCl2(aq)
Qual a concentração, em quantidade de matéria (mol/L), da espécie Sn 4+ formada?
SnCl2(aq) + 2 FeCl3(aq) → SnCl4(aq)+ 2 FeCl2(aq)
Qual a concentração, em quantidade de matéria (mol/L), da espécie Sn 4+ formada?
Provas
Questão presente nas seguintes provas
Um hidrocarboneto cuja fórmula geral é CnH2n é um
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
A substância orgânica representada na Figura a seguir pertence à classe dos bioflavonoides e apresenta atividade biológica.
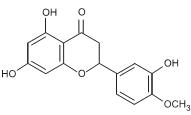
Na sua estrutura estão presentes as funções orgânicas
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Considere uma solução preparada pela adição de 0,01mol do ácido carboxílico indicado como HA, em água, formando 1,0 L de solução.
HA ⇌ A- + H+ ; Ka = 1,0 x 10-4
A alternativa que indica, com melhor aproximação, a concentração, em mol L-1 , de íons H+ na solução é:
HA ⇌ A- + H+ ; Ka = 1,0 x 10-4
A alternativa que indica, com melhor aproximação, a concentração, em mol L-1 , de íons H+ na solução é:
Provas
Questão presente nas seguintes provas
A posição dos elementos na tabela periódica se dá em função da ordem crescente dos números atômicos, em períodos e grupos e de acordo com a quantidade de camadas eletrônicas e a distribuição dos elétrons nos seus níveis de energia. As propriedades dos elementos se relacionam com as respectivas posições na tabela.
Levando em conta as posições num mesmo período ou num mesmo grupo, o
Levando em conta as posições num mesmo período ou num mesmo grupo, o
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container