Foram encontradas 2.000 questões.
Propano é queimado completamente com 60% de excesso de ar. Considerando a composição do ar 80% N2 e 20% O2 em base molar, a razão entre o número de mols de N2 /CO2 no gás de exaustão é, aproximadamente, igual a
Provas
Questão presente nas seguintes provas
Em um dado momento de uma titulação potenciométrica, usando um eletrodo de Pt como indicador, a concentração de Fe2+ é dez vezes a concentração de Fe3+.
O potencial medido em volts, numa certa temperatura T e em relação ao eletrodo padrão de hidrogênio (EPH), é
Dados Da equação de Nernst: RT/F = 0,06 V
Fe 3+ + e → Fe 2+ E0 = +0,77 V
E0EPH = 0V
O potencial medido em volts, numa certa temperatura T e em relação ao eletrodo padrão de hidrogênio (EPH), é
Dados Da equação de Nernst: RT/F = 0,06 V
Fe 3+ + e → Fe 2+ E0 = +0,77 V
E0EPH = 0V
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Transformações Químicas e EnergiaEletroquímica
Considere a eletrólise de uma solução aquosa contendo íons K+, Pt ++, Cu++, e Mn++.
Os íons de maior e de menor prioridade de descarga são, respectivamente,
Os íons de maior e de menor prioridade de descarga são, respectivamente,
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
A diferenciação entre os conceitos de ácido e base, estabelecidos pela teoria de Lewis, prediz que, para qualquer espécie química, ácidos e bases são, respectivamente,
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água

Sabendo-se que o produto iônico da água na mesma tem- peratura é Kw, a concentração de H+, é dada por:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Considerando 6,0 x 1023 como a quantidade de unidades referente a 1 mol, e sendo “massa molar” a massa, em gramas, de 1 mol de matéria, a quantidade, em mols, de íons Na+ e a quantidade de íons Cl- que há em 117 g de NaCl dissolvidos em água e totalmente dissociados nos seus íons são, respectivamente,
Provas
Questão presente nas seguintes provas
A medição de pH com eletrodo de membrana de vidro é um exemplo de determinação potenciométrica. No método potenciométrico,
Provas
Questão presente nas seguintes provas
Num laboratório foi realizado um experimento em que o magnésio reagiu com ácido clorídrico dando origem a 56 mL de gás hidrogênio, medido na pressão de 770 mm de Hg e temperatura de 27 ºC.
Mg(s)+ 2HCl(aq) → MgCl2(aq) + H 2(g)
A quantidade máxima de H2 obtida no experimento, em miligrama, considerando comportamento de gás ideal, é, aproximadamente, igual a:
Dados:
constante dos gases = 62,3 mmHg L K-1 mol -1
Mg(s)+ 2HCl(aq) → MgCl2(aq) + H 2(g)
A quantidade máxima de H2 obtida no experimento, em miligrama, considerando comportamento de gás ideal, é, aproximadamente, igual a:
Dados:
constante dos gases = 62,3 mmHg L K-1 mol -1
Provas
Questão presente nas seguintes provas
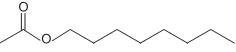
A substância representada na Figura acima é um flavorizante obtido sinteticamente (a partir de um ácido carboxílico e um álcool) utilizado em diversos alimentos e bebidas.
De acordo com as regras da IUPAC, sua nomenclatura é
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um padrão primário usado em titulações volumétricas em sistemas aquosos possui diversas características.
NÃO constitui uma dessas características:
NÃO constitui uma dessas características:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container