Foram encontradas 2.000 questões.
No alto forno de uma siderúrgica, uma das reações que ocorre para a produção do redutor metalúrgico monóxido de carbono é a do coque com o gás carbônico. Em condições específicas, essa reação apresenta o seguinte equilíbrio:
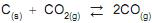
Para esse equilíbrio, a expressão da constante de equilíbrio Kc em função das concentrações das espécies, em quantidade de matéria, é:
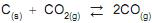
Para esse equilíbrio, a expressão da constante de equilíbrio Kc em função das concentrações das espécies, em quantidade de matéria, é:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
As funções da química inorgânica reúnem compostos que apresentam comportamento químico semelhante.
É uma propriedade da função química inorgânica:
É uma propriedade da função química inorgânica:
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Na volumetria ácido-base, a escolha do indicador de neutralização leva em conta a curva de titulação e a faixa de viragem do indicador:
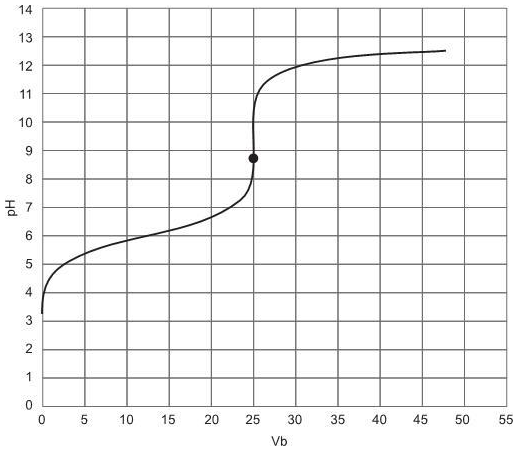
O gráfico acima refere-se à variação do pH na titulação de um ácido em função do volume de base (Vb), em mL, adicionado. O ponto estequiométrico se dá com a adição de 25 mL de base. 
Um indicador do ponto final da titulação apropriado para uso nessa análise é o(a)
Provas
Questão presente nas seguintes provas
A soda cáustica (NaOH) pode ser fabricada numa cuba eletrolítica dotada de eletrodos de platina, através da eletrólise do NaCl do tipo
Provas
Questão presente nas seguintes provas
A solubilidade do cloreto de amônio em água, a 20 º C é de 37,5 g por 100 mL. No processo de dissolução em água, o cloreto de amônio absorve energia da sua vizinhança.
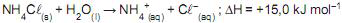
A adição de 1.000 g de cloreto de amônio a 1.000 mL de água, a 20 º C, envolve a variação de entalpia, em kJ, igual a
Dado
MNH4Cl = 53,5g mol -1
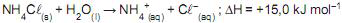
A adição de 1.000 g de cloreto de amônio a 1.000 mL de água, a 20 º C, envolve a variação de entalpia, em kJ, igual a
Dado
MNH4Cl = 53,5g mol -1
Provas
Questão presente nas seguintes provas
No equilíbrio indicado na equação abaixo, o rendimento de formação do SO3 é aumentado, por exemplo, pela adição de O2 ao sistema. Esse é um exemplo de que, quando um sistema em equilíbrio é perturbado, a composição do mesmo se ajusta de modo a contrapor a ação de perturbação.
2 SO 2(g) + O 2(g) ⇌ 2 SO 3(g)
Esse comportamento segue a(o)
2 SO 2(g) + O 2(g) ⇌ 2 SO 3(g)
Esse comportamento segue a(o)
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
Uma mistura foi preparada em duas etapas e a 25 º C: na Etapa I, foram misturados 50 mL de água e 50 mL de etanol; na Etapa II, uma massa igual a 0,05 g de glicose (soluto não volátil) foi totalmente dissolvida no sistema de solventes.
A pressão de vapor das soluções e dos componentes que as formaram é maior na(o)
Dados
ponto de ebulição da água a 1 atm = 100 ºC
ponto de ebulição do etanol a 1 atm = 78 º C
A pressão de vapor das soluções e dos componentes que as formaram é maior na(o)
Dados
ponto de ebulição da água a 1 atm = 100 ºC
ponto de ebulição do etanol a 1 atm = 78 º C
Provas
Questão presente nas seguintes provas
As massas, em gramas, de cálcio, fósforo e oxigênio, presentes em 100 gramas do ortofosfato de cálcio, são, respectivamente, as seguintes:
Dados
Massa atômica do cálcio = 40 g
Massa atômica do fósforo = 31 g
Massa atômica do oxigênio = 16 g
Dados
Massa atômica do cálcio = 40 g
Massa atômica do fósforo = 31 g
Massa atômica do oxigênio = 16 g
Provas
Questão presente nas seguintes provas
O gás sulfídrico (H2 S) é um produto formado em corpos de água poluídos. A ionização do H2 S em água se dá em duas etapas, como mostrado abaixo.
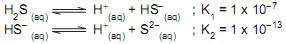
Considere as afirmações a seguir referentes a esses equilíbrios e à solução onde eles ocorrem.
I - O valor da constante de equilíbrio global do processo de ionização do H2 S é dado por K1+ K2
II - A expressão da constante de equilíbrio da primeira equação é K1 =[H+ ] [HS- ]
III - A adição de NaOH na solução diminui a concentração de H2 S na solução.
Está correto o que se afirma em
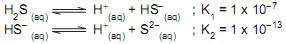
Considere as afirmações a seguir referentes a esses equilíbrios e à solução onde eles ocorrem.
I - O valor da constante de equilíbrio global do processo de ionização do H2 S é dado por K1+ K2
II - A expressão da constante de equilíbrio da primeira equação é K1 =[H+ ] [HS- ]
III - A adição de NaOH na solução diminui a concentração de H2 S na solução.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
Abaixo está representada a estrutura de uma substância.
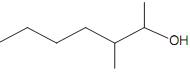
A função orgânica oxigenada e a nomenclatura de acordo com as regras da IUPAC dessa substância são, respectivamente,

A função orgânica oxigenada e a nomenclatura de acordo com as regras da IUPAC dessa substância são, respectivamente,
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container