Foram encontradas 1.190 questões.
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A concentração de vitamina C (C6 H8 O6 ) foi determinada por coulometria usando eletrodo de platina. No processo, aplicou-se uma diferença de potencial para formar I- , a partir de um excesso de I2 presente na solução onde a amostra foi adicionada. A espécie I3- (formada a partir de I- e I2 ) reagiu com a vitamina C, oxidando-a (ver equações a seguir).
C6 H8 O6 + I3 - → C6 H6 O6 + 3I- + 2 H+
Em que I3 - + 2e → 3I-
Sabe-se que 25,00 mL de solução de amostra foram adicionadas à célula coulométrica, e que foram requeridos 12 min e
52 s da aplicação de 25 mA de corrente para oxidar quantitativamente a vitamina C.
Com base nessa informação, a concentração de vitamina C (em mol L-1 ) na solução de amostra é de
Dado
Carga de 1 mol de elétrons = 96500 C
C = A s
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Pode-se fazer passar um feixe de luz por dois recipientes A e B, um deles contendo uma solução atômica (SA), e o outro contendo uma mistura coloidal (MC), como ilustrado na Figura abaixo.
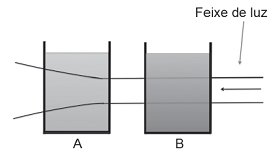
Observe as afirmações a seguir.
I – O recipiente A contém um MC, pois os coloides são suficientemente grandes para espalhar a luz.
II – O recipiente A contém uma SA, pois as moléculas são suficientemente grandes para espalhar a luz.
III – O recipiente B contém uma MC, pois os coloides não são suficientemente grandes para espalhar a luz.
Está correto o que se afirma em:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma solução aquosa foi preparada pela dissolução de 0,020 mol de hidroxilamina (HO-NH2 ) em 250,00 mL de água pura. A equação do equilíbrio de ionização do HO-NH2 em água e sua constante, a 25°C, estão apresentadas abaixo.
HO-NH2 (aq) + H2O(ℓ) = HO-NH3 + (aq) + OH- (aq) Kb = 5 x 10-9
A concentração, em mol L-1 , de OH- na solução é
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaHidrocarbonetos
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
O captopril, cuja estrutura está representada a seguir, é um medicamento usado para o controle da pressão arterial.
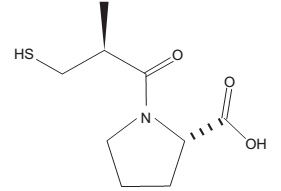
Sobre o captopril, verifica-se que ele
Provas
O nióbio é um elemento usado para produção de aços com propriedades especiais. Na natureza, ele ocorre na forma de pentóxido de nióbio, de onde se pode obter o nióbio metálico por um processo térmico, usando uma mistura de alumínio e óxido de ferro (III), como mostrado na equação química a seguir.
3 Nb2O5(s) + Fe2O3(s) + 12 Al(s) → 6 Nb(s) + 2 Fe(s) + 6 Al2O3(s)
O processo térmico em questão produz o nióbio metálico com rendimento de 80%.
O valor aproximado da massa de Nb, em tonelada, que seria obtida a partir de 1,6 toneladas de Nb2O5 é
Dados
M (Nb) = 93 g mol-1
M (Nb2O5 ) = 266 g mol-1
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A concentração da solução preparada, em mol L-1, corresponde a, aproximadamente,
Dado Massa molar do etanol: 46 g mol-1
Provas
Uma solução padrão de um corante foi colocada na cubeta de quartzo (1,00 cm de caminho óptico) de um espectrofotômetro. O percentual de radiação (em 550 nm) transmitida através da solução foi de 10%, valor já corrigido em relação à contribuição do solvente. A absortividade molar, em 550 nm, do corante é 10.000 L mol-1 cm-1 , e o resultado experimental se encontrava na faixa linear regida pela Lei de Beer-Lambert.
A concentração, em mol L-1 , do corante na solução é
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
Um volume de 500 mL de uma solução aquosa, contendo 0,0040 mol L-1 de Ba2+ foi misturada com 500 mL de uma solução 0,0060 mol L-1 de ácido sulfúrico, promovendo a reação conforme ilustrado na Equação I a seguir:
Ba2+ (aq) + H2SO4 (aq) → BaSO4 (s) + 2 H+ (aq) (Equação I)
O BaSO4 produzido se dissocia, estabelecendo um equilíbrio de solubilidade como indicado na Equação II a seguir:
BaSO4(aq) ⇋ Ba2+ (aq) + SO42- (aq) ; Kps = 1 x 10-9 (Equação II)
A solução resultante (de volume igual a 1000 mL) se encontra a 25°C. Conforme as condições indicadas, e ignorando a influência da força iônica no equilíbrio de solubilidade, mas considerando o excesso de SO42- em solução, a concentração aproximada de Ba2+ residual na solução, em mol L-1 , é
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
Uma solução foi preparada com a mistura de 360 g de água pura com 160 g de um solvente orgânico. Em uma certa temperatura, a pressão de vapor da mistura foi 4,3 kPa. Com base no valor da pressão de vapor da mistura, e nas opções abaixo, pode-se concluir que o solvente orgânico usado foi
Dados:
• Pressão de vapor da água pura: 2,0 kPa
• Pressão de vapor do solvente orgânico: 13,5 kPa
• M (água) = 18,00 g mol-1
Provas
Uma amostra de minério (20,00 g) foi previamente solubilizada com uma mistura de ácidos inorgânicos e posteriormente diluída com água para ajustar seu volume para 1,00 L. Dessa solução, separam-se 250,00 mL que foram colocados em uma célula de um sistema eletrogravimétrico. Após a aplicação de um potencial adequado, o cobre da solução foi depositado, seletivamente, na superfície de um eletrodo de platina (em forma de rede para se ter elevada área superficial).
Se a massa de cobre depositada no eletrodo foi igual a 1,55 g, a percentagem (m/m) no minério é
Provas
Caderno Container