Foram encontradas 1.190 questões.
O acetaldeído ou etanal é um aldeído que se decompõe segundo a equação abaixo:
CH3 CHO(g) → CH4(g) + CO (g)
A reação tem cinética de segunda ordem, e o valor da constante de velocidade, numa dada temperatura, é 9,0 × 10-5 L mol-1 s-1 .
O valor mais próximo da velocidade inicial de decomposição de 200 g de acetaldeído, dentro de um reator de 10 L, é
Dado
M(CH3 CHO) = 44 gmol-1
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Na titulação fotométrica, com monitoramento da absorvância da solução em 330 nm, o analito A, em solução, reage com o reagente titulante T para formar o produto P de acordo com a equação a seguir:
A(aq) + T(aq) → P(aq)
A curva de titulação obtida é mostrada abaixo.
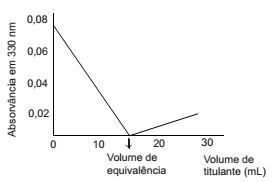
Com base nas informações acima, conclui-se que
Provas
Uma mistura gasosa denominada de ARGOMETA P10 contém 10%, em massa, de metano e argônio em quantidade para fechar o balanço da composição. Considere que um recipiente, de volume igual a 100 L, está preenchido somente com 100 g de ARGOMETA P10.
Considerando condições ideais, a pressão parcial do metano no recipiente, em atm e a 298 K, é, aproximadamente, igual à
Dados
M (CH4 ) = 16 g mol-1
M (Ar) = 40 g mol-1
R = 0,082 atm L mol-1 K-1
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma solução de NaCℓ foi feita dissolvendo, totalmente, 0,100 g do sal em água antes de transferir essa mistura para um balão volumétrico de 100,00 mL onde a solução teve seu volume ajustado. A incerteza da massa de NaCℓ é 0,001 g (calculada considerando duas etapas: a tara e a pesagem propriamente dita do sal), e a incerteza do balão é 0,10 mL.
Assim, essa solução teria uma incerteza de concentração, em gL-1 , de
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um volume igual a 25,00 mL de solução aquosa 1,0 x 10-2 mol L-1 de um pesticida foi transferido para um balão volumétrico que teve seu volume ajustado, com água, para 100,00 mL. Dessa solução, 20,00 mL foram coletados e passados numa coluna de extração em fase sólida onde o pesticida foi totalmente retido. Utilizaram-se 5 mL de solvente adequado para eluir 90,0% do pesticida (em mol) para um balão volumétrico onde se ajustou o volume para 10,00 mL. A fração complementar de 10,0% ficou retida na coluna sem chance de recuperação.
A concentração, em mol L-1 , do pesticida no balão de 10,00 mL é
Provas
O potencial padrão de redução do Fe3+ (ver equação I) é +0,77 V em relação ao eletrodo padrão de hidrogênio (EPH). O eletrodo de referência de calomelano, ou Hg/Hg2Cℓ2 (KCℓsat), tem potencial de redução (ver equação II) igual a +0,24 V em relação ao EPH.
I - Fe3+ (aq) + e → Fe2+ (aq) E° = +0,77 V
II - Hg2Cℓ2(s) + e → 2 Hg(ℓ) + 2 Cℓ- (aq) E° = +0,24 V
Assim sendo, o potencial de redução padrão do Fe3+, em V, em relação ao eletrodo de referência de calomelano é
Provas
Uma amostra de minério (5,00 g) foi completamente dissolvida em ácido e o volume ajustado para 100,00 mL. Uma alíquota de 10,00 mL dessa solução aquosa foi misturada, de forma lenta e sob agitação constante, com excesso de solução aquosa de hidróxido de amônio, suficiente para promover a precipitação completa de ferro na forma de Fe(OH)3 .
Fe3+ (aq) + 3OH- (aq) → Fe(OH)3 (s)
Após envelhecer, em sua água mãe, filtrar e lavar, o precipitado foi calcinado em forno mufla para formar Fe2O3 , que depois foi deixado para resfriar, em dessecador, até massa constante.
2 Fe(OH)3(s) → Fe2O3(s) + 3H2O(g)
Sendo a massa de Fe2O3(s), obtida após a calcinação, igual a 3,84 g, o valor mais próximo da percentagem (massa/ massa) de ferro no minério é
Dado
M (Fe) = 56 g mol-1
M (Fe2O3 ) = 160 g mol-1
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
É muito comum encontrar as substâncias KNO3 , NaOH, e HCℓ em produtos comercializados e de uso cotidiano.
Observe as afirmações a seguir concernentes a propriedades dessas substâncias
I - NaNO3 , ao ser dissolvido em água, altera significantemente o pH.
II - NaOH se dissocia parcialmente quando dissolvido em água, sendo, por isso, uma base fraca.
III - HCℓ é um gás muito solúvel em água, onde se dissocia diminuindo o pH.
Está correto APENAS o que se afirma em
Provas
O enxofre do H2S dissolvido em água pode ser precipitado por um processo eletrolítico, como indicado na equação a seguir.
H2 S(aq) + I2(aq) → S(s) + 2H+ (aq) + 2I- (aq)
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma massa igual a 5,5 g de cloreto de cálcio (CaCl2 ) foi totalmente dissolvida em um balão volumétrico de 250,00 mL. Dessa solução, preparou-se uma solução de trabalho transferindo-se uma alíquota de 10,00 mL para um balão volumétrico de 100,00 mL, onde se ajustou o volume final com água pura.
O valor mais aproximado da concentração de cloreto, em quantidade de matéria (mol L-1 ), na solução de trabalho é
Dado
M (CaCl2) = 111,0 g mol-1
Provas
Caderno Container