Foram encontradas 2.005 questões.
- Eletrônica AnalógicaAmplificadores, diodos, transistores, tiristores e dispositivos correlatos
- Eletrônica AnalógicaCircuitosModelos equivalentes e realimentação
Julgue os itens abaixo, relativos à aplicação de realimentação negativa em circuitos amplificadores lineares.
A largura de banda do amplificador pode aumentar com o uso da realimentação negativa.
Provas
Julgue o item seguinte quanto ao fator de atrito, à dinâmica de fluidos e à perda de carga.
Ao operar uma bomba com pequeno valor de NPSH, há risco de ocorrer cavitação.
Provas
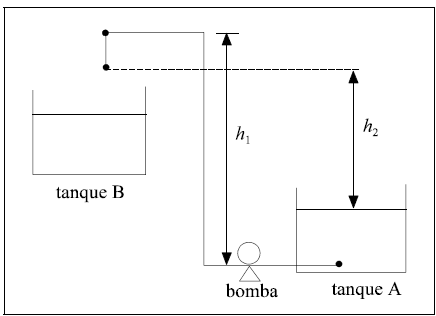
O esquema acima mostra o arranjo de dois tanques, A e B. Deseja-se transferir um líquido incompressível do tanque A para o tanque B. Com base nessa situação, julgue o item que se segue.
Uma bomba que opere com grande valor de NPSH tem pequena possibilidade de apresentar cavitação.
Provas
Plataformas de produção de petróleo são estruturas flutuantes destinadas a receber o petróleo de vários poços submarinos e transferilo a navios ou oleodutos. O equilíbrio dessas estruturas pode ser analisado de forma simplificada com o modelo abaixo.
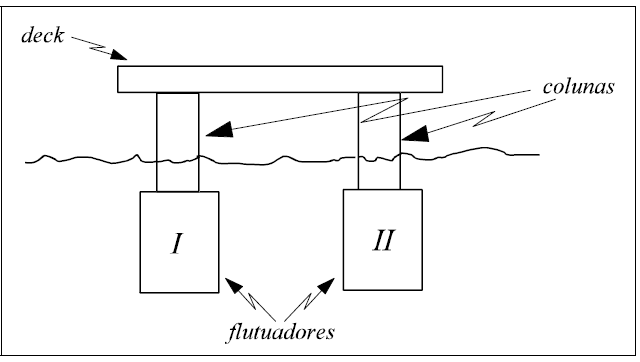
Considerando que a densidade da água seja igual a 103 kg/m3 e que a aceleração gravitacional seja de 10 m/s2, julgue o item a seguir, a respeito da flutuabilidade e estabilidade da estrutura modelada.
Considerando a hipótese de ocorrer um rompimento na parte inferior do flutuador I, localizada a 20 m de profundidade, então, se ar fosse injetado no flutuador a uma pressão superior a 200 kPa, a água não adentraria o flutuador.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
A acumulação de sujeiras em superfícies dificulta o acesso de oxigênio, formando um anodo, e contribui para acelerar a corrosão.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
Pode ocorrer corrosão em mecanismos hidráulicos de aço-carbono apoiados em mancais de latão, pois ele pode formar uma célula galvânica de composição tendo o aço como catodo.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
A presença de tensões em componentes estruturais que estejam operando em ambientes corrosivos não afeta a velocidade da corrosão, pois tensões não têminfluência no mecanismo de funcionamento das células galvânicas.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
O mecanismo de eletrodeposição de um metal sobre outro (cromagem, niquelagem etc.) é o mesmo da corrosão. A peça que vai receber a deposição é usada como catodo e uma fonte externa força os elétrons para o catodo, fazendo que os íons liberados pelo anodo, feito do metal a ser depositado, se depositem no catodo.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
A umidade do ar atmosférico é insuficiente para permitir a formação de uma célula galvânica na superfície de uma peça de aço-carbono e enferrujá-la.
Provas
Considerando a teoria linear de ondas aplicada às ondas de gravidade na superfície do mar, julgue o item a seguir.
Em ondas estacionárias, a velocidade do fluido e a elevação da superfície apresentam uma diferença de fase de 180 graus.
Provas
Caderno Container