Foram encontradas 50 questões.
O gráfico abaixo mostra o perfil energético de uma reação exotérmica em duas condições experimentais: A (linha cheia) e B (linha tracejada).
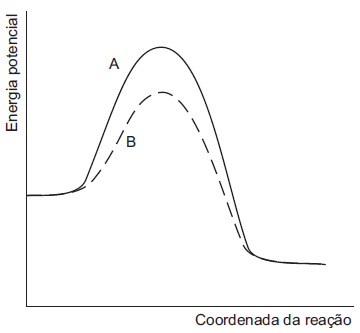
A análise do gráfico mostra que a velocidade da reação é
Provas
Alguns processos químicos e bioquímicos são muito sensíveis à variação do valor de pH do meio. Para evitar grandes variações do pH, recorre-se ao uso de soluções tampões. A tabela abaixo mostra os valores de pKa para alguns ácidos.
|
Ácido |
pKa1 | pKa2 |
pKa3 |
|
Carbônico |
6,4 |
10,3 |
– |
|
Fosfórico |
2,1 | 7,2 |
11,7 |
|
Sulfúrico |
< 0 | 1,9 |
– |
Considere um processo em que o máximo rendimento se dá em pH 11,0 e no qual estão disponíveis apenas os ácidos mostrados na tabela acima e os sais de seus ânions com o cátion sódio. A solução tampão de pH 11,0, com máxima eficiência, é formada por
Provas
Uma das últimas fases do tratamento da água nas Estações de Tratamento de Água (ETA) é a desinfecção com o uso de cloro. A reação do cloro com a água em pH básico forma os íons hipoclorito e o cloreto, conforme a reação abaixo.
!$ C\ell_2+2 \, OH^- \rightleftharpoons C \ell O ^-+C \ell^-+H_2O !$
Nessa reação, o
Provas
Ao se dissolver um soluto em água, o pH da solução pode diferir do encontrado para a água quando pura, que possui pH = 7. Dentre os solutos abaixo, aquele cuja solução apresentará pH menor que sete é
Provas
A padronização de uma solução de hidróxido de sódio utilizou como padrão primário o biftalato de potássio (KHC8H4O4). A tabela abaixo mostra os resultados da titulação.
|
Titulação |
Massa de biftalato de NaOH |
Volume de NaOH |
| 1 |
0,5502 g |
23,12 mL |
| 2 | 0,5328 g |
22,32 mL |
A concentração média encontrada para a solução de hidróxido de sódio, em mol/L, é
Provas
Em um reator de 5,0 L, misturaram-se os reagentes Z e X para produzir Y, segundo a seguinte equação química:
2 Z(g) + X(g) !$ \longrightarrow !$ 2 Y(g)
Após o equilíbrio ser estabelecido, detectou-se, no interior do reator, 0,400 mol de Z; 0,200 mol de X e 2,400 mol de Y. O valor da constante de equilíbrio para essa reação é
Provas
Misturou-se, em um béquer, 20,0 mL de uma solução aquosa de ácido clorídrico 0,500 mol/L com 30,0 mL de uma solução aquosa de metilamina 1,00 mol/L. O pH da solução resultante é de, aproximadamente,
Dados: Kb metilamina = 4,4x10–4; log 2 = 0,30; log 11 = 1,04
Provas
O teor da solução de ácido clorídrico concentrada, também chamada de ácido clorídrico P.A., é de 37,0 % (m/m) e a massa específica dessa solução é de 1,19 g/cm3. O volume de ácido clorídrico P.A. necessário para preparar 250,0 mL de uma solução de concentração 0,500 mol/ L é de, em mL, aproximadamente,
Provas
A ferrugem é o exemplo mais conhecido de um fenômeno comum a muitos materiais: a oxidação. Dentre os compostos abaixo, aquele que apresenta o elemento no maior estado de oxidação é o
Provas
Uma solução aquosa de cloreto de sódio com concentração de 0,010 mol/L foi transferida para um béquer, onde se mergulhou um aparelho para medir a condutividade elétrica de tal solução.
Dividiu-se a solução original em três partes denominadas P, Q e R, onde foram adicionados:
Parte P: 200 mL de água deionizada
Parte Q: 1,00 g de cloreto de sódio
Parte R: 1,00 g de carbonato de amônio
Sabendo-se que a fração do volume da solução original dividido entre as partes era o mesmo, qual é o efeito da adição das substâncias indicadas na condutividade elétrica nas partes P, Q e R, em relação à medida da solução inicial?
| Parte P |
Parte Q | Parte R |
Provas
Caderno Container