Foram encontradas 3.243 questões.
Considere as seguintes situações.
I: estado inicial é gelo a 0ºC; estado final é água pura a 0ºC
II: água pura a 100ºC
Considerando esses sistemas, julgue os itens que se seguem.
Se o estado descrito na situação II for convertido a gás a 100ºC, uma vez que a temperatura é constante, não haverá variação de pressão do sistema.
Provas
Considere as seguintes situações.
I: estado inicial é gelo a 0ºC; estado final é água pura a 0ºC
II: água pura a 100ºC
Considerando esses sistemas, julgue os itens que se seguem.
Sabendo que o calor específico da água é igual a 1,0 cal/(g × ºC) e que M(H) = 1,0 g/mol e M(O) = 16,0 g/mol, é correto concluir que para cada mol de água que sai do estado na situação I e chega ao estado na situação II, são consumidas 1.800 calorias de calor.
Provas
Considere as seguintes situações.
I: estado inicial é gelo a 0ºC; estado final é água pura a 0ºC
II: água pura a 100ºC
Considerando esses sistemas, julgue os itens que se seguem.
Durante o processo na situação I, não há variação de energia potencial, apenas de energia cinética.
Provas
Considere as seguintes situações.
I: estado inicial é gelo a 0ºC; estado final é água pura a 0ºC
II: água pura a 100ºC
Considerando esses sistemas, julgue os itens que se seguem.
Para o processo na situação I, é correto afirmar que a variação de entalpia é menor que o produto da variação de entropia pela temperatura em Kelvin.
Provas
Considere as seguintes situações.
I: estado inicial é gelo a 0ºC; estado final é água pura a 0ºC
II: água pura a 100ºC
Considerando esses sistemas, julgue os itens que se seguem.
Na situação I, o processo é endotérmico.
Provas
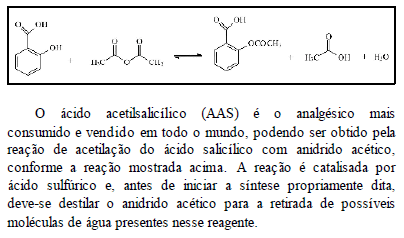
Considerando essas informações, julgue os itens subseqüentes.
Sabendo que a reação mencionada é endotérmica, é correto afirmar que o aquecimento do meio reacional favorece a formação de AAS.
Provas

Considerando essas informações, julgue os itens subseqüentes.
O ácido sulfúrico aumenta a energia de ativação e, conseqüentemente, torna a reação mais rápida.
Provas

Considerando essas informações, julgue os itens subseqüentes.
O mecanismo da reação é o mesmo com ou sem catalisador. Apenas a energia de ativação é alterada.
Provas

Considerando essas informações, julgue os itens subseqüentes.
A presença de água diminui o rendimento da reação, daí a necessidade de se destilar o anidrido acético.
Provas
Acerca dos métodos espectroscópicos de análise, de potenciometria e volumetria, julgue os itens que se seguem.
A espectroscopia de ultravioleta não permite análises quantitativas das amostras.
Provas
Caderno Container