Foram encontradas 845 questões.
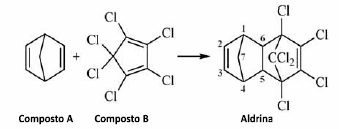
A figura acima apresenta a reação de formação do pesticida aldrina. Considerando a reação apresentada e as estruturas dos compostos envolvidos, julgue o item subsequente.
A estrutura molecular da molécula de aldrina pode ser determinada por microscopia de varredura eletrônica.
Provas

A figura acima apresenta a reação de formação do pesticida aldrina. Considerando a reação apresentada e as estruturas dos compostos envolvidos, julgue o item subsequente.
No espectro de ressonância magnética nuclear de prótons da aldrina, o sinal que aparece em campo mais baixo (maior deslocamento químico em relação aos prótons do tetrametilsilano) corresponde aos hidrogênios ligados aos carbonos marcados com os número 1 e 4 na figura apresentada.
Provas

A figura acima apresenta a reação de formação do pesticida aldrina. Considerando a reação apresentada e as estruturas dos compostos envolvidos, julgue o item subsequente.
O espectro de ressonância magnética nuclear de prótons da molécula de aldrina deve apresentar quatro sinais distintos.
Provas
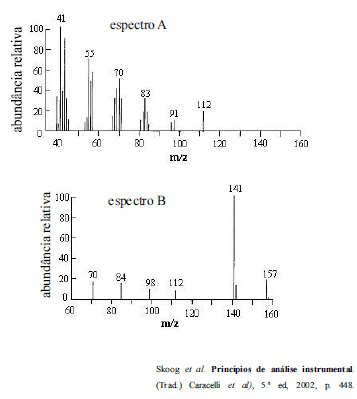
A espectrometria de massa é uma ferramenta de análise de grande utilidade, tanto na identificação de elementos quanto de compostos orgânicos. A figura abaixo apresenta dois espectros de massa obtidos para a molécula de 1-decanol, sendo que um dos espectros foi obtido utilizando-se a técnica da ionização por impacto de elétrons, e o outro, utilizando-se a ionização química (os espectros não são apresentados, necessariamente, nessa ordem).
Com base na técnica em questão, nos espectros e nas informações acima, julgue o seguinte item.
Na identificação de elementos em solução, o uso da espectroscopia de massa com plasma indutivamente acoplado fornece, usualmente, espectros mais complexos e difíceis de interpretar do que os espectros óticos correspondentes, principalmente em análises envolvendo elementos de maior número atômico.
Provas

A espectrometria de massa é uma ferramenta de análise de grande utilidade, tanto na identificação de elementos quanto de compostos orgânicos. A figura abaixo apresenta dois espectros de massa obtidos para a molécula de 1-decanol, sendo que um dos espectros foi obtido utilizando-se a técnica da ionização por impacto de elétrons, e o outro, utilizando-se a ionização química (os espectros não são apresentados, necessariamente, nessa ordem).
Com base na técnica em questão, nos espectros e nas informações acima, julgue o seguinte item.
Na figura apresentada, o espectro A corresponde à ionização por impacto de elétrons e o espectro B, à ionização química.
Provas

A espectrometria de massa é uma ferramenta de análise de grande utilidade, tanto na identificação de elementos quanto de compostos orgânicos. A figura abaixo apresenta dois espectros de massa obtidos para a molécula de 1-decanol, sendo que um dos espectros foi obtido utilizando-se a técnica da ionização por impacto de elétrons, e o outro, utilizando-se a ionização química (os espectros não são apresentados, necessariamente, nessa ordem).
Com base na técnica em questão, nos espectros e nas informações acima, julgue o seguinte item.
O raio de curvatura do movimento de um íon no analisador de um espectrômetro com setor magnético (r) está relacionado ao potencial elétrico de aceleração do íon (V), à intensidade do campo magnético do analisador (!$ \beta !$), à massa do íon (m) e à diferença entre o número de prótons e elétrons no íon (z) por meio da expressão !$ r = \sqrt{\dfrac{2.V}{\beta}\cdot (\dfrac{m}{z})} !$
Provas
Um volume Va de uma solução aquosa de ácido acético foi titulado com uma solução aquosa de NaOH com concentração mb, em mol/L. No ponto final da titulação, um volume Vb da base havia sido adicionado. Considerando os fundamentos dos métodos de análise titulométrica e a situação descrita, julgue o item subsequente.
O emprego, como titulante, de uma solução aquosa de NH3, em lugar da solução de NaOH, possibilitaria uma identificação mais precisa do ponto de equivalência.
Provas
Um volume Va de uma solução aquosa de ácido acético foi titulado com uma solução aquosa de NaOH com concentração mb, em mol/L. No ponto final da titulação, um volume Vb da base havia sido adicionado. Considerando os fundamentos dos métodos de análise titulométrica e a situação descrita, julgue o item subsequente.
Em qualquer titulação, o ponto final corresponde exatamente ao ponto de equivalência.
Provas
Considere que 20,0 mL de uma solução de FeSO4 a 0,100 mol/L tenha sido titulada, a 25 ºC, com uma solução contendo íons Ce+4 na concentração 0,100 mol/L. Para isso, mediu-se o potencial da célula eletroquímica em que o cátodo é um eletrodo de platina mergulhado na mistura reacional, e o ânodo, um eletrodo de referência de calomelano, com potencial E (cal). A reação de oxirredução que se passa no cátodo é: Ce+4 + Fe2+ → Ce3+ + Fe3+. Com base nessas informações e considerando que todas as soluções envolvidas apresentam comportamentos ideais, julgue o próximo item.
Após o ponto de equivalência, o potencial da célula permanecerá constante.
Provas
O teor de enxofre em uma amostra de querosene foi determinado por um método que apresenta um desvio padrão (!$ \sigma !$) já conhecido de 0,0010%. Foram realizadas quatro medidas, sendo encontrados os valores: 0,114; 0,112; 0,120; 0,118.
A tabela a seguir apresenta os níveis de confiança para diferentes valores de , em uma distribuição normal de !$ \dfrac{x-\mu}{\sigma} !$ erros, sendo !$ \mu !$ a média da população.
| nível de | !$ \dfrac{x-\mu}{\sigma} !$ | nível de confiança (%) | !$ \dfrac{x-\mu}{\sigma} !$ |
| 50 | 0,67 | 95 | 1,96 |
| 68 | 1,00 | 96 | 2,00 |
| 80 | 1,29 | 99 | 2,58 |
| 90 | 1,64 | 99,9 | 3,29 |
Com base nessas informações e considerando a inexistência de erros determinados, julgue o item que se segue.
A probabilidade de que o valor verdadeiro da concentração de enxofre na amostra esteja no intervalo 0,116 !$ \pm !$ 0,001 é de 96%.
Provas
Caderno Container