Foram encontradas 370 questões.
Para representação de números muito grandes e números muito pequenos, emprega-se a notação científica, utilizando potências de 10.
Julgue os itens a seguir, a respeito de notação científica.
I 9,2 × 10-9 km > 2,9 × 109 mm
II 2,3 kg > 320 g
III 5,5 × 10-3 s > 4,4 ms
Assinale a opção correta.
Provas
Assinale a opção que apresenta o(s) produto(s) correto(s) da respectiva reação química.
Provas
A Tabela Periódica é um dos conceitos mais importantes em química. Seu desenvolvimento é um exemplo de como descobertas científicas podem ser feitas pelo uso do talento para organizar dados coletados por um grande número de cientistas em um período de muitos anos. No que concerne a essa temática, assinale a opção correta.
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaIsomeria Plana e Espacial
Os ácidos graxos insaturados, de ocorrência na natureza, contêm um número par de carbonos com uma dupla ligação ou mais duplas ligações. Geralmente, as duplas ligações ocorrem nos carbonos C9-C10 e C12-C13 e são designadas por C\( n \):1 ou C\( n \):2, com \( n \) igual ao número de carbonos da cadeia.
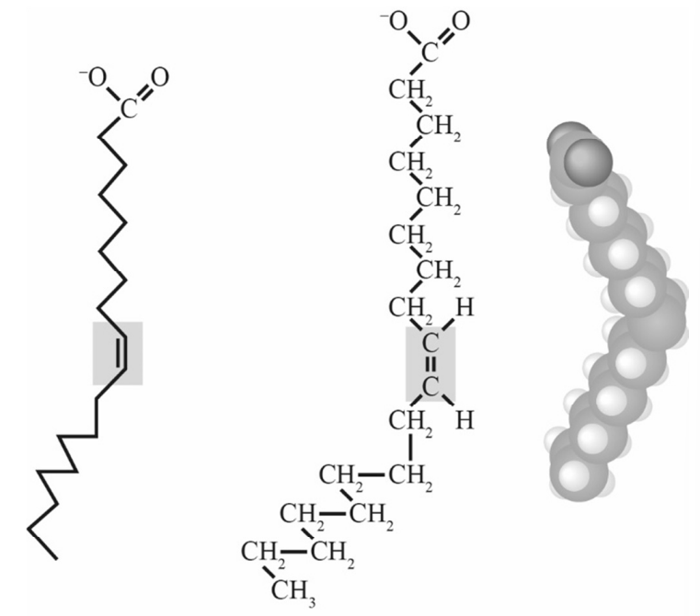
A partir das informações anteriores e das figuras (a), (b) e (c) apresentadas, assinale a opção correta.
Provas
A distinção original entre ácidos e bases foi baseada, perigosamente, nos critérios de gosto e de tato: os ácidos eram azedos e as bases lembravam o sabão. As definições modernas são baseadas em uma ampla variedade de reações químicas. Sabendo que ZAg = 47 e ZNa = 11 são os números atômicos da prata e do sódio, respectivamente, assinale a opção correta com relação a esse tema.
Provas
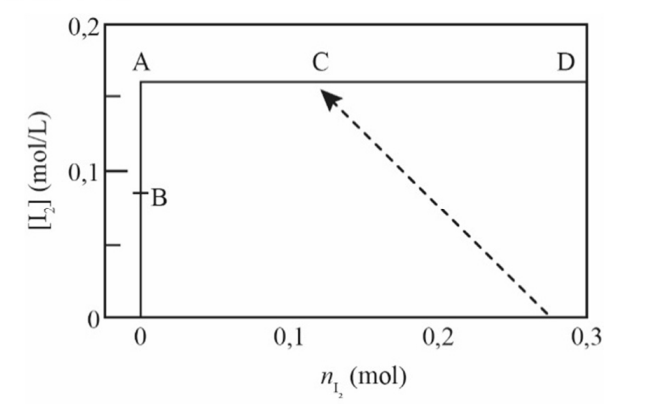
A figura anterior representa um gráfico da variação da concentração de I2 — [I2] — em uma solução aquosa em função da quantidade de matéria de I2 sólido — \( n_{I_2} \) — em contato com essa solução. Tendo o gráfico precedente como referência e considerando que K representa a constante de equilíbrio da reação I2 (s) ⇌ I2 (org), em que o solvente orgânico é CCl₄, assinale a opção correta.
Provas
2HgCl2(aq) + C2O4 2−(aq) → 2Cl− (aq) + 2CO2(g) + Hg2Cl2(s)
experimento | [HgCl2] M | [C2O4-2] M | Vinicial M/min |
1 | 0,105 | 0,150 | 1,78 × 10−5 |
2 | 0,105 | 0,300 | 7,12 × 10−5 |
3 | 0,0525 | 0,300 | 3,56 × 10−5 |
Considerando a reação e a tabela apresentadas, assinale a opção correta.
Provas
Os elementos X e Y reagem entre si, produzindo, em cada experimento, um produto distinto. As massas utilizadas de X e Y, designadas respectivamente por \( m_X \) e \( m_Y \), em cinco experimentos realizados estão dispostas na seguinte tabela.
|
experimento |
\( m_X (g) \) |
\( m_Y (g) \) |
|
1 |
1 |
3 |
|
2 |
1 |
6 |
|
3 |
1 |
9 |
|
4 |
2 |
3 |
|
5 |
2 |
9 |
Com relação à situação hipotética precedente, assumindo-se que o primeiro experimento resultou na formação do composto XY, é correto afirmar que os compostos obtidos exemplificam a aplicação da Lei de
Provas
O clorato de potássio (KClO₃) é uma substância bastante utilizada nos laboratórios didáticos para obtenção de gás oxigênio a partir da sua decomposição térmica, que gera como resíduo sólido o cloreto de potássio, de acordo com a equação que se segue.
2 KClO₃ (s) → 2 KCl (s) + 3 O₂ (g)
Considerando-se que tenham sido utilizados na reação em apreço 735 g de KClO₃ e assumindo-se que todo o oxigênio gerado pela decomposição do KClO₃ tenha sido consumido na combustão completa do buteno (C4H8) e sabendo-se que M\( O_2 \) = 32,0 g/mol, M\( C_4H_8 \) = 56,0 g/mol e M\( KClO_3 \) = 122,5 g/mol, é correto afirmar que a massa de C4H8 consumida na reação de combustão é igual a
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaTermoquímica
A determinação do abaixamento crioscópico é bastante didática para a verificação das propriedades coligativas em disciplinas experimentais de físico-química. Em um experimento, foram realizadas duas leituras do ponto de congelamento de uma amostra de 5 mL de terc-butanol, uma antes e outra após a adição de hexano (M = 86 g/mol). O abaixamento crioscópico (∆Tf) observado após a adição de hexano foi de 4 K. Admita que a constante crioscópica do terc-butanol (Kf) seja 8,3 K ∙ kg ∙ mol−1, que a densidade do terc-butanol seja 790 g/L, que a densidade do hexano seja 660 g/L e que ∆Tf = Kfb, em que b representa a molalidade do hexano no solvente terc-butanol.
Considerando-se o experimento descrito na situação hipotética em tela, é correto afirmar que o volume utilizado de hexano foi
Provas
Caderno Container