Foram encontradas 447 questões.
Princípio de incêndio em subestação deixa um funcionário ferido
Um homem ficou ferido em um princípio de incêndio
em uma subestação de energia de uma companhia de
água, em São Cristóvão.
Segundo testemunhas houve uma explosão, e pou-
co depois começou o fogo e muita fumaça. Um funcionário
da companhia de água que estava de plantão teve 50% do
corpo queimado.
De acordo com a companhia de água, o incêndio foi
provocado pelo superaquecimento na subestação de ener-
gia da elevatória, que desligou dois disjuntores. O fogo foi
controlado pelos bombeiros e, logo em seguida, técnicos
da empresa começaram o conserto.
O funcionário foi levado para o Hospital do
Andaraí, onde permanece internado em estado grave, no
CTI
Disponível em: http://www.g1.globo.com. Acesso em: 03 ago. 2009. (Adaptado).
I – Se o acidentado estiver inconsciente, pôr seu corpo de barriga para baixo antes de proceder à avaliação do seu estado geral.
II – Evitar o pânico e procurar a colaboração de outras pessoas, dando ordens breves, claras, objetivas e concisas.
III – Manter afastados os curiosos, para evitar confusão e para ter espaço em que se possa trabalhar da melhor maneira possível.
IV – Ser ágil e decidido, observando rapidamente se existem perigos para o acidentado e para quem estiver prestando o socorro.
É(São) correto(s) APENAS o(s) procedimento(s)
Provas
Os trabalhos pioneiros de químicos e físicos dos séculos XVII, XVIII e XIX permitiram a elaboração de diversas equações relacionadas às propriedades dos gases, que mais tarde foram combinadas, formando a lei geral dos gases ideais, que explica diferentes fenômenos envolvendo gases.
Com base nesta lei, analise as afirmativas a seguir.
I – Um balão cheio com 1 L de gás carbônico (CO2) não flutua, mas murcha, porque o CO2 é mais denso do que o ar.
II – Um balão cheio com hélio flutua porque este gás, apesar de ser mais denso do que o ar, possui menor volume molar, devido ao seu menor raio atômico.
III – Dois balões contendo 1 L de gás carbônico ou de hélio terão massas iguais destes gases, já que um mol de qualquer gás, nas condições ideais, ocupa 22,4 L.
(Dados: massa molar do CO2 = 44 g/mol
massa molar do He = 4 g/mol
massa molar média do ar = 29 g/mol)
É(São) correta(s) APENAS a(s) afirmativa(s)
Provas
Uma forma de detectar motoristas alcoolizados é utilizar um bafômetro baseado na oxidação do etanol a ácido acético por ação do íon dicromato em meio ácido.
A equação não balanceada pode ser descrita da seguinte forma:
CH3CH2OH (g) + K2Cr2O7 (aq) + H2SO4 (aq) \( \rightarrow \) CH3CO2H (aq) + K2SO4 (aq)+ Cr2(SO4)3 (aq)+ H2O (\( \ell \))
Se um indivíduo apresentar 0,08 mg de etanol no volume de ar exalado dos pulmões, a quantidade de dicromato de potássio, em miligramas, consumida nesta reação será
(Dados:1 mol de etanol = 46 g
1 mol de K2Cr2O7 = 294)
Provas
Catalisadores são compostos adicionados a um processo químico, mas que não são consumidos durante o processo, embora afetem sua cinética.
Assim, os catalisadores
Provas
A oxidação de materiais ferrosos pelo oxigênio atmosférico é um processo de corrosão muito comum em indústrias e residências.
As semirreações envolvidas neste processo são:
Fe2+ + 2 e \( \rightarrow \) Fe Eº = -0,409 V
O2 + H2O + 4e \( \rightarrow \) 4 HO- Eº = 0,401 V
Considerando que a variação de energia livre de uma reação de oxidorredução pode ser calculada pela fórmula \( \Delta G \, = \, -n F \Delta E, \) na qual n é o número de elétrons transferidos, F é a Constante de Faraday (96,5 kJ V-1 mol-1) e \( \Delta E, \) a diferença entre os potenciais padrão das reações de oxidação e de redução, conclui-se que a(o)
Provas
Existem diversas metodologias analíticas para a determinação dos teores de espécies químicas específicas.
Relacione as metodologias apresentadas à esquerda com os processos relacionados à direita.
Metodologia
I – Volumetria de neutralização.
II – Complexometria.
III – Turbidimetria.
IV – Absorção atômica.
Processo analítico
(P) Análise de dureza de água.
(Q) Determinação de acidez em óleos.
(R) Determinação dos teores de Fe, Cr e Hg em resíduos industriais.
Estão corretas as associações:
Provas
A Empresa Campina Grande Ltda. recebeu antecipadamente, em janeiro de 2008, por meio de depósito realizado em sua conta corrente bancária, o valor de R$ 12.000,00, referentes ao aluguel de seis meses de um imóvel de sua propriedade.
Que lançamento contábil caracteriza esta operação?
Provas
Provas
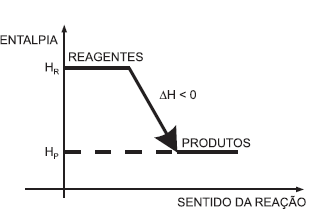
Com base no diagrama acima e considerando a variação de energia nas reações químicas, analise as afirmativas a seguir.
I – A quantidade de calor necessária para que 1 grama de água passe de 14,5 oC para 15,5 oC define o conceito da unidade Caloria (cal).
II – Um elemento químico apresenta entalpia igual a zero, quando, a 25 oC e 1 atm, está em seu estado físico usual e na forma alotrópica mais estável.
III – O diagrama representa uma reação exotérmica que, ao ocorrer, libera calor para o meio.
IV – A Lei de Hess estabelece que a variação de entalpia ( H) em uma reação química depende apenas dos estados inicial e final da reação.
Estão corretas as afirmativas
Provas
Os sistemas de tratamento de efluentes industriais são constituídos por processos e operações que empregam princípios físicos, químicos e biológicos para a remoção dos contaminantes. Os processos biológicos utilizam reações bioquímicas para remover contaminantes orgânicos solúveis ou coloidais e podem ser aeróbios ou anaeróbios. Um exemplo de processo que emprega os princípios biológicos descritos é
Provas
Caderno Container