Foram encontradas 308 questões.
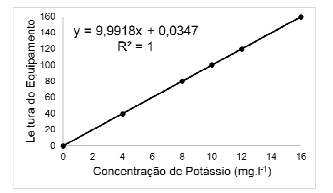
Provas
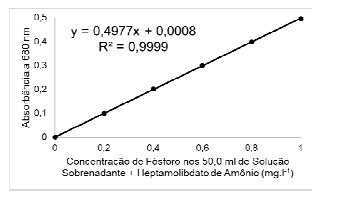
Provas
Provas
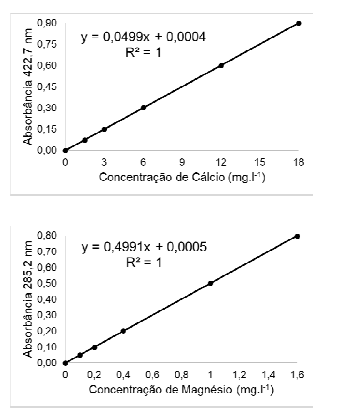
Provas
Reação: H+ + Na0H → Na+ + H20
Provas
Dentro da agronomia, uma medida de fundamental importância para garantir um bom desenvolvimento das plantas em uma lavoura é a medida de acidez do solo. Uma medida consagrada dentro dessa ciência agrária é o chamado pH SMP, que recebe esse nome com base nas iniciais dos três principais cientistas que desenvolveram o tampão em pH 7,5 utilizado na execução dessa medida (Shoemaker, McClean e Pratt). Com base no resultado do pH SMP, consegue-se ter uma boa estimativa da acidez no solo devido à presença dos íons H+ e Al3+, em centimols de carga equivalentes por decímetro cúbico (“litro”) de solo. Abaixo encontra-se o gráfico que apresenta a relação entre essas duas variáveis:
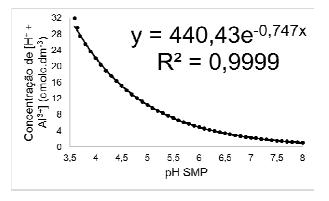
Provas
Provas
Reação: C8H5KO4 + K0H → C8H4K204 + H20
Provas
Reação: Na2B4O7 + 2 HCl → H2B4O7 + 2 NaCl
Provas
Provas
Caderno Container