Foram encontradas 308 questões.
- Biossegurança Técnica em Laboratório
- Identificação dos Diversos Equipamentos de um Laboratório, sua Utilização e Conservação
Considere as seguintes cores e os tipos de tubulações a seguir:
I) Amarelo
II) Azul
III) Vermelho
IV) Branco
V) Verde
a) Vapor.
b) Água Líquida (Extinção de Incêndio).
c) Água Líquida (Fornecimento para o Laboratório).
d) Ar comprimido.
e) Gases Não-Liquefeitos.
A associação correta das cores dos tubos pintados com os respectivos fluidos que se deslocam por dentro destes em um laboratório é
Provas
I) A filtração é um processo de separação utilizado quando se deseja separar um sólido solúvel de um líquido onde ele está imerso. Quando a separação é muito lenta ou inviável somente pela gravidade, a filtração à vácuo, onde um frasco Kitasato é ligado a uma bomba de vácuo logo abaixo do funil de filtragem, torna-se uma alternativa visando a agilizar ou tornar possível o processo.
II) O dessecador é um instrumento de laboratório importante para permitir que amostras retiradas da estufa resfriem sem reabsorver umidade. É um instrumento geralmente de vidro grosso, com saída que permite criar vácuo em seu interior quando necessário. Os dessecadores costumam possuir em seu fundo sílica, que apresenta em si íons complexos de cobalto, que quando apresenta coloração avermelhada, indica que o dessecador está em condições de uso, enquanto que, quando está azulada, é necessário levar a sílica para estufa a 1050C por 24 horas para que desidrate e possa tornar o dessecador novamente operante.
III) O pHmetro é um equipamento que permite realizar aferições de medida do pH, variável capaz de aferir quantitativamente a acidez ou basicidade de uma solução. Para isso, ele dispõe de um eletrodo de vidro que é permeável à passagem de íons H+ , onde geralmente uma célula galvânica de prata e cloreto de prata (Ag | AgCl) gera um sinal elétrico na presença desses íons, que é detectado pelo equipamento eletrônico. Nesse equipamento, é importante manter o eletrodo sempre imerso em uma solução, geralmente de cloreto de potássio 3 mol.l-1 (KCl), saturada com cloreto de prata (AgCl), de forma a preservar a integridade do eletrodo permeável e da célula galvânica.
Dessa(s) afirmativa(s),
Provas
Provas
Provas
I) Não se deve utilizar água tratada da rede de saneamento para o preparo de soluções analíticas, uma vez que impurezas e moléculas e íons contendo cloro, flúor e outros compostos químicos presentes nela, podem acabar por interferir nas análises que serão realizadas com essa solução posteriormente.
II) A água destilada é obtida a partir da água tratada, após esta ser submetida a ebulição e posterior recondensação. Apresenta altíssimo grau de pureza, podendo ser utilizada em equipamentos e processos de ponta, como a Cromatografia em Fase Líquida de Alta Eficiência (Sigla HPLC, em inglês).
III) A água deionizada é obtida após submetê-la a tratamentos com resinas capazes de retirar íons que diminuem a pureza dela, sendo mais pura que a água destilada, sendo adequada em qualidade para ser utilizada no preparo de soluções de uso comum em laboratório.
Está/estão correta(s)
Provas
Considere as moléculas a seguir:
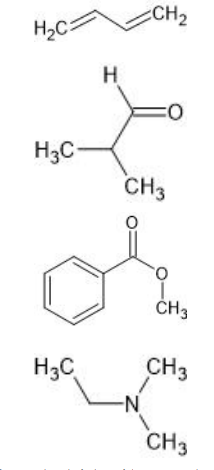
Os nomes das substâncias orgânicas representadas por essas moléculas são, respectivamente,
Provas
Considere a molécula orgânica representada a seguir:
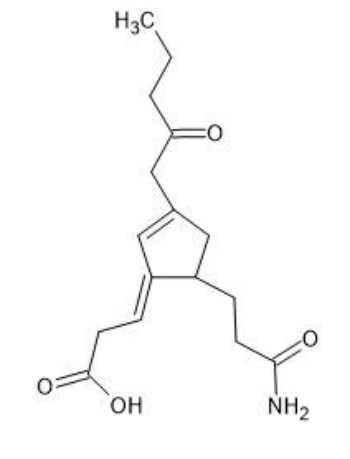
Considere as seguintes afirmações a respeito da molécula:
I) Não existem carbonos terciários na molécula.
II) Todas as cadeias carbônicas da molécula são homogêneas.
III) Existem, na molécula, as funções orgânicas: amida, ácido carboxílico e cetona.
IV) A molécula possui um total de três carbonilas.
Dessas afirmativas, estão corretas
Provas
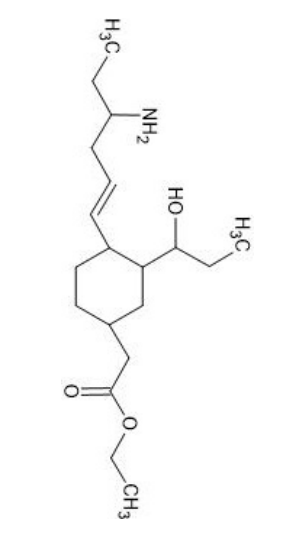
Considere as seguintes afirmações a respeito da molécula:
I) Não se trata de um composto aromático.
II) Todas as cadeias carbônicas da molécula são saturadas.
III) Existem, na molécula, as funções orgânicas: amina, éster e álcool.
IV) A molécula possui um total de 22 carbonos.
Dessas afirmações, estão corretas
Provas
Combustão Completa da Sacarose:
2 C12H22 O11 + a O2 → bCO2 + CH2O (1)
Reação Ácido-Base:
dHNO3 + 2 Ca(OH)2 → e Ca(NO3)2 + ƒH2O (2)
Reação de Haber-Bosch:
1 N2 + g H2 → h NH3 (3)
Tem-se as seguintes afirmações:
I) Os coeficientes a, b, c e d são, respectivamente, 35, 24, 22 e 4.
II) Os coeficientes e, f, g e h são, respectivamente, 1, 2, 3 e 2.
III) As reações cujas equações (1), (2) e (3) estão representando são, respectivamente, de decomposição, de dupla troca e de síntese.
IV) Na reação da equação (1), a sacarose sofreu oxidação, e na reação da equação (3) o nitrogênio sofreu redução.
Dessas afirmações,
Provas
Provas
Caderno Container