Foram encontradas 85 questões.
HCl(aq)
Ácido Clorídrico
220g. !$ \ell !$-1
d = 1,10g.cm-3
A interpretação correta dos dados apresentados indica que 25,0ml de solução aquosa do ácido clorídrico contém 5,5g de HCl.
Provas
4C3H5N3O9(!$ \ell !$) !$ \rightarrow !$ 6N2(g) + 12CO2(g) + 10H2O + O2(g) !$ \Delta !$H < zero
Substâncias, como a nitroglicerina, C3H5N3O9(!$ \ell !$), devem ser armazenadas com cuidado, porque sua decomposição, representada pela equação química, é muito rápida, exotérmica e explosiva.
Provas
O peróxido de hidrogênio, H2O2(aq), é um óxido ácido, estável na presença de água e da luz e, por isso, pode ser armazenado em frascos de vidro transparente.
Provas
O conhecimento das propriedades dos materiais, o planejamento adequado e o controle de estocagem de produtos químicos minimizam os riscos potenciais associados à utilização e ao armazenamento das diversas substâncias químicas utilizadas em um laboratório.
Provas
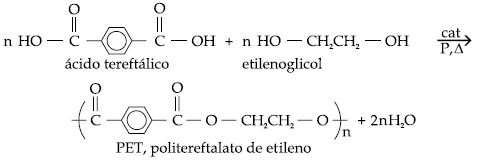
O politereftalato de etileno, PET, é um polímero de condensação resistente à corrosão por ácidos e bases, sendo utilizado como embalagem de água e de refrigerantes.
Provas
O petróleo é uma fonte renovável de hidrocarbonetos, e o craqueamento catalítico de moléculas desses compostos é realizado sob resfriamento constante e uso de catalisadores com propriedades ácidas.
Provas
A conversão de energia química em elétrica, com o uso de pilhas que utilizam eletrodos de mercúrio, cádmio ou zinco, é um processo sustentável de obtenção de energia, porque o consumo desses materiais diminui a extração de matéria-prima e não provoca impactos ambientais, quando descartados no ambiente.
Provas
| Equação da semirreação | Potencial padrão de redução, Eº (V) |
| Au3+(aq) + 3e- !$ \leftrightarrows !$ Au(s) | +1,42 |
| MnO4(aq) + 8H+(aq) + 5e- !$ \leftrightarrows !$ Mn2+(aq) + 4H2O(!$ \ell !$) | +1,49 |
De acordo com os potenciais padrão de redução apresentados na tabela, a reação entre o ouro e o íon permanganato, em meio ácido, é espontânea, e o !$ \Delta !$Eº desse processo é igual a +0,07V.
Provas
I. HNO2(aq) !$ \leftrightarrows !$ H+(aq) + NO-2 (aq) Ka = 5,0.10-4
II. H2CO3(aq) !$ \leftrightarrows !$ H+(aq) + HCO-3 (aq) Ka = 4,3.10-7
As constantes de equilíbrio dos sistemas químicos representados em I e II indicam que, em soluções aquosas 1,0mol.!$ \ell !$-1 dos ácidos nitroso e carbônico, a concentração de cátions e de ânions é maior no sistema I que no sistema II.
Provas
Fe2O3(s) + 3CO(g) !$ \leftrightarrows !$ 2Fe(s) + 3CO2(g)
Nas indústrias siderúrgicas, o ferro metálico é obtido nos altos-fornos, em determinadas condições, de acordo com o equilíbrio heterogêneo representado pela equação química, cuja constante de equilíbrio, Kc, é determinada pela expressão matemática
!$ Kc \, = \, \dfrac { [Fe]^2. \, [CO_2]^3} { [Fe_2O_3].[CO]^3} !$
Provas
Caderno Container