Foram encontradas 85 questões.
A filtração simples consiste na utilização de um funil de Büchner e um kitassato, com saída lateral, acoplada a uma bomba de vácuo.
Provas
A solução aquosa de cianeto de sódio, NaCN(aq), tem pH > 7 porque o íon cianeto se hidrolisa de acordo com a reação representada por CN-(aq) + H2O(!$ \ell !$) !$ \leftrightarrows !$ HCN(aq) + OH-(aq).
Provas
A calcinação de uma amostra com 40g de mármore resultou em 20g de óxido de cálcio, CaO(s), o que permite concluir que o mármore analisado apresenta 80% de carbonato de cálcio, CaCO3(s).
Provas
O princípio das técnicas eletroanalíticas se fundamenta nos processos de oxirredução espontânea, que ocorrem na eletrólise, sistema reacional em que o agente oxidante ganha elétrons do agente redutor.
Provas
A cromatografia pode ser utilizada para a identificação de compostos, por comparação com padrões existentes, e na purificação de substâncias.
Provas
Uma coluna cromatográfica é constituída, basicamente, por uma fase estacionária, o eluente e uma fase móvel, empacotada em um tubo, de modo que o processo de separação dos componentes de uma mistura nesse sistema independe das interações entre esses componentes e a fase estacionária ou móvel.
Provas
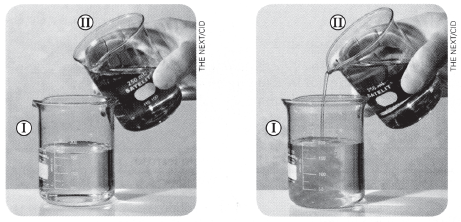
Considerando-se que o béquer I contém iodeto de potássio em solução aquosa, KI(aq), e o béquer II, a solução aquosa de nitrato de chumbo (II), Pb(NO3)2(aq), é correto afirmar que a reação entre o iodeto de potássio e o nitrato de chumbo (II), em solução aquosa e à temperatura ambiente, produz o iodeto de chumbo (II) sólido, insolúvel em água, se [Pb2+] [I-]2 !$ \ge !$ Kps.
Provas
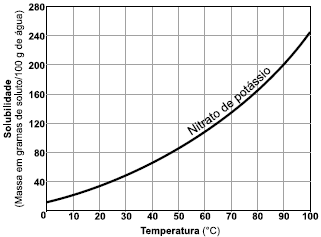
Com base na análise do gráfico de solubilidade do nitrato de potássio e admitindo-se que a densidade da água é 1,0g.cm-3, pode-se afirmar que o resfriamento de 60oC para 25ºC, de uma solução que apresenta 80g de nitrato de potássio, KNO3, dissolvido em 100m!$ \ell !$ de água, resulta na precipitação de, aproximadamente, metade da massa do sal que estava dissolvida.
Provas
A armazenagem de soluções de hidróxido de sódio em recipientes de vidro, como balões volumétricos, não é aconselhável, devido à reação entre a base e o dióxido de silício do vidro, utilizado na fabricação de objetos de uso volumétricos.
Provas
Ag+(aq) + Cl-(aq) !$ \rightarrow !$ AgCl(s)
A quantidade de íons Cl-(aq) presente em um reservatório de água pode ser determinada titulando-se uma amostra dessa água com Ag+(aq), de acordo com a reação representada pela equação química em evidência, e, desse modo, considerando-se que, para a titulação de 50,0m!$ \ell !$ de amostra, o volume gasto foi de 25,0m!$ \ell !$ de solução 0,3mol.!$ \ell !$-1 de Ag+, a concentração de cloreto presente na amostra é de 0,6mol.!$ \ell !$-1.
Provas
Caderno Container