Foram encontradas 1.980 questões.
Julgue o item a seguir.
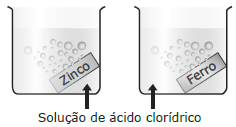
Os experimentos demonstrados na figura não requerem cuidados especiais porque o ácido clorídrico está diluído e o gás obtido no processo é pouco reativo.
Provas
Julgue o item a seguir.
O ácido fluorídrico, HF(aq), é guardado em garrafas de vidro porque não reage com os silicatos presentes nesses recipientes.
Provas
Julgue o item a seguir.
O ácido nítrico concentrado, HNO3(conc.), por ser muito oxidante e corrosivo, deve ser estocado separadamente de outros ácidos e de outras substâncias inorgânicas e disponibilizado em pequenas quantidades no laboratório.
Provas
Julgue o item a seguir.
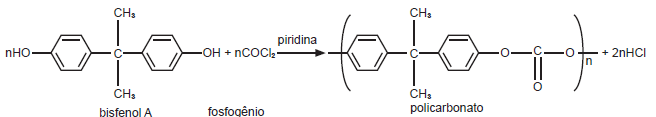
O policarbonato, representado pela estrutura química acima, por ser resistente ao calor e ao impacto, é um polímero usado na fabricação de lentes, copos, CDs e DVDs entre outros objetos. O problema desse polímero é que, com o tempo ou pelo contato com produtos de limpeza, ele libera unidades de bisfenol A, que contamina o ambiente, inclusive alimentos.
Considerando-se as informações e a estrutura química do polímero, pode-se afirmar que o policarbonato é um polímero de adição que apresenta anéis do ciclohexatrieno ligados ao grupo funcional das cetonas o que favorece a contaminação do ambiente.
Provas
Julgue o item a seguir.
O produto formado na reação entre o 2-metilpropeno e o cloreto de hidrogênio, em meio aquoso, é o 1-cloro-2-metilproprano de acordo com a regra de Markovnikov.
Provas
Julgue o item a seguir.

O etileno, C2H4(g), produzido a partir da desidratação do etanol, é um hidrocarboneto saturado utilizado como matéria-prima para a produção de polímeros usados na fabricação de embalagens biodegradáveis.
Provas
Julgue o item a seguir.

A decomposição da água por eletrólise, representada na figura, resulta na produção de um volume de hidrogênio, H2(g), no tubo II, duas vezes superior ao volume de oxigênio, O2(g), no tubo I.
Provas
Julgue o item a seguir.
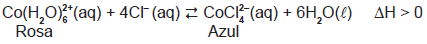
Aplicando-se o princípio de Le Chatêlier ao equilíbrio químico representado pela equação química, pode-se afirmar que o aquecimento da solução em equilíbrio favorece a intensificação da coloração azul devido ao deslocamento do equilíbrio químico, com formação de íons CoCl2– 4 (aq), e ao aumento do valor da constante de equilíbrio, Kc.
Provas
Julgue o item a segujr.
2ClO2(aq) + 2OH–(aq) → ClO–3 (aq) + ClO–2 (aq) + H2O(!$ \ell !$)
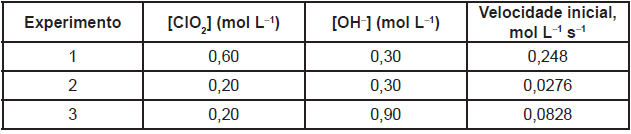
A equação de velocidade de uma reação representa a lei de velocidade e relaciona as concentrações dos reagentes elevadas a expoentes determinados experimentalmente.
Analisando-se a equação química e os dados experimentais que constam na tabela, é correto afimar que a velocidade da reação representada é dada pela equação v = k [ClO2]2. [OH–].
Provas
Julgue o item a seguir.
2NaI(s) + MnO2(s) + 3H2SO4(aq) 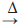 2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
O iodo gasoso, I2(g), pode ser obtido em laboratório pelo aquecimento da mistura de iodeto de sódio, NaI(s), e dióxido de manganês, MnO2(s), com gotejamento contínuo de ácido sulfúrico concentrado, H2SO4(aq), de acordo com a reação representada, de maneira simplificada, pela equação química.
A equação de oxirredução representada revela que o iodeto de sódio atua como agente oxidante porque cada átomo de iodo do iodeto de sódio transfere um elétron para o átomo de manganês do dióxido de manganês.
Provas
Caderno Container