Foram encontradas 100 questões.
Em um recipiente de 1 litro, foram misturados 12 mols de X2 e 13 mols de Y2. Depois de algum
tempo, o sistema atingiu o equilíbrio e o número de mols de XY3 medido foi 8.
Considerando a seguinte reação: X2 + 3Y2 ⇆ 2XY3, o valor da constante de equilíbrio Kc (mol-2 .L2 ) da reação é:
Considerando a seguinte reação: X2 + 3Y2 ⇆ 2XY3, o valor da constante de equilíbrio Kc (mol-2 .L2 ) da reação é:
Provas
Questão presente nas seguintes provas
Em relação aos Modelos Atômicos, analise as informações:
I Com a descoberta do elétron, Thomson verificou a existência de partículas menores que o átomo, isto é, existem partículas subatômicas. Para Thomson, o átomo era uma esfera positiva com elétrons negativos incrustados, ou seja, não havia núcleo nem níveis de energia.
II Uma importante contribuição do modelo de Rutherford foi considerar o átomo constituído de uma estrutura altamente compactada de prótons e elétrons.
III Supondo que 1 nêutron apresenta massa 1 kg, a massa de um átomo com 11 prótons, 12 nêutrons e 11 elétrons seria de 34 kg.
IV No modelo atômico atual, os elétrons têm caráter corpuscular e de onda simultaneamente.
As informações corretas são apenas:
I Com a descoberta do elétron, Thomson verificou a existência de partículas menores que o átomo, isto é, existem partículas subatômicas. Para Thomson, o átomo era uma esfera positiva com elétrons negativos incrustados, ou seja, não havia núcleo nem níveis de energia.
II Uma importante contribuição do modelo de Rutherford foi considerar o átomo constituído de uma estrutura altamente compactada de prótons e elétrons.
III Supondo que 1 nêutron apresenta massa 1 kg, a massa de um átomo com 11 prótons, 12 nêutrons e 11 elétrons seria de 34 kg.
IV No modelo atômico atual, os elétrons têm caráter corpuscular e de onda simultaneamente.
As informações corretas são apenas:
Provas
Questão presente nas seguintes provas
50.0 mL de solução de NaCl 0.10 M são titulados com AgNO3 0.10 M. Considerando que para
o AgCl tem-se que Kps = 1.0x10-10
, o valor da [Cl-
] e o de pAg, quando o volume titulante (VT) for
igual a 50.0 mL, são respectivamente:
Provas
Questão presente nas seguintes provas
Considere um sistema alimentado por uma fonte de corrente contínua, contendo duas células
eletrolíticas ligadas em série, através de um fio condutor, durante um determinado intervalo de
tempo. Uma das células contém o eletrodo de níquel e uma solução aquosa de Ni(NO3)2 e a outra
contém um eletrodo de ouro e uma solução aquosa de AuCl3. Nesse intervalo de tempo, o eletrodo
de níquel teve um incremento de massa de 1.18 g.
O incremento de massa no eletrodo da outra célula deve ter sido de:
O incremento de massa no eletrodo da outra célula deve ter sido de:
Provas
Questão presente nas seguintes provas
A variação da entalpia padrão para a oxidação da substância NH3(g), conforme a equação não
balanceada: NH3(g) + O2(g) ⮕ NO(g) + H2O(g), pode ser determinada.
Considere os seguintes dados:
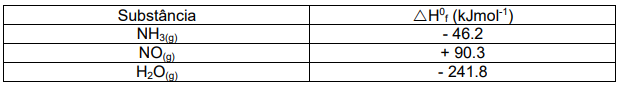
Nessas condições, a variação de entalpia padrão para a oxidação do NH3(g) é:
Considere os seguintes dados:

Nessas condições, a variação de entalpia padrão para a oxidação do NH3(g) é:
Provas
Questão presente nas seguintes provas
Prednisolona é um fármaco indicado no tratamento de vários casos de inflamação e doenças
autoimunes, tais como: asma, colite, artrite reumatoide, esclerose múltipla, lúpus, Doença de
Crohn, entre outras. Pode ser administrado por via oral, intramuscular (injetável) e ocular (colírio).

Sobre a estrutura da Prednisolona, é correto afirmar que

Sobre a estrutura da Prednisolona, é correto afirmar que
Provas
Questão presente nas seguintes provas
Em relação à Geometria Molecular de Compostos Químicos, usando a Teoria da repulsão
entre os pares eletrônicos da camada valência, analise as informações:
I A geometria da molécula de SF6 é hexagonal. II A geometria da molécula de XeF4 é tetraédrica. III A geometria da molécula de PCl5 é bipiramidal triangular. IV A geometria da molécula de SO2 é angular.
São corretas apenas:
I A geometria da molécula de SF6 é hexagonal. II A geometria da molécula de XeF4 é tetraédrica. III A geometria da molécula de PCl5 é bipiramidal triangular. IV A geometria da molécula de SO2 é angular.
São corretas apenas:
Provas
Questão presente nas seguintes provas
Dois tampões, X e Y, de pH 5.00 e 6.00, respectivamente, foram preparados a partir do ácido
HA e do sal NaA. Ambas as soluções são 0.500 M em HA. Se volumes iguais dos dois tampões
forem misturados, o pH da solução resultante será:
Dado: Ka(HA) = 1.0x10-5
Dado: Ka(HA) = 1.0x10-5
Provas
Questão presente nas seguintes provas
Considere uma pilha cuja reação global não balanceada é mostrada a seguir:
Zn + MnO2 + NH4+ → Zn2+ + MnO(OH) + NH3
Nessas condições, conclui-se que
Zn + MnO2 + NH4+ → Zn2+ + MnO(OH) + NH3
Nessas condições, conclui-se que
Provas
Questão presente nas seguintes provas
A concentração molar de uma solução de ácido sulfúrico que contém 96.0 % (em massa) de
ácido sulfúrico e apresenta uma densidade igual a 1.84 g.cm-3 é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container