Foram encontradas 640 questões.
Um estudante preparou soluções aquosas acidificadas de FeCl2 e CuCl2 com concentrações 0,001 mol/L e 0,002 mol/L, respectivamente. Posteriormente, retirou 100 mL de cada solução e misturou, chegando a 200 mL de uma solução contendo íons Fe2+ e Cu2+. A essa mistura foi adicionada solução concentrada de NaOH, gota a gota. Sabendo que os valores de Kps para Fe(OH)2 e Cu(OH)2 são 8,0 x 10-16 e 2,2 x 10−20, respectivamente, é correto afirmar que:
Provas
A pirita (dissulfeto ferroso) é um sulfeto mineral abundante e pode ser encontrado em veios de quartzo ou rocha metamórfica. Quando exposta à atmosfera, reage com oxigênio produzindo dióxido de enxofre, de acordo com a equação química abaixo:
!$ \mathbf{ { \large{ 4\,\,\,FeS_2(s) + 11\,\,O_2(g) \rightarrow 2 Fe_2 O_3(s) + 8 SO_2(g)}}} !$
Durante a escavação de um túnel em uma região rica em pirita, houve intoxicação dos trabalhadores, resultante de uma alta concentração de dióxido de enxofre. Os engenheiros responsáveis pela obra estimaram uma liberação de 1,23 m3 de gás SO2 a 1 atm e 27ºC. Calcule a massa de pirita que reagiu para formar a quantidade estimada do dióxido de enxofre liberado. Massas molares (g/mol): O = 16; S = 32; Fe = 56.
Provas
Em 1923, Lewis propôs uma teoria ácido-base que se baseava na transferência de um par eletrônico. Considerando as espécies abaixo, indique a única que pode atuar como uma base de Lewis.
Provas
O íon nitrônio (!$ NO_2^+ !$) é um importante intermediário formado em reações de nitração. É possível formar esse intermediário in situ através da reação entre ácido nítrico e ácido sulfúrico concentrados, de acordo com o mecanismo abaixo:
!$ \mathbf{ ETAPA\,\,1: HNO_3 + H_2 SO_4 { \Large { \rightarrow}} H_2 NO_3^+ HSO_4^- } !$
!$ \mathbf{ ETAPA\,\,2:\,\,\,\,\,H_2 NO_3^-{ \Large { \rightarrow}} NO_2^+ H_2^O } !$
Considerando o comportamento das moléculas e íons no mecanismo apresentado, é possível afirmar que a molécula HNO3 atua como:
Provas
Um estudante de química prepara uma solução num béquer com posterior transferência para um balão volumétrico, conforme o esquema abaixo.
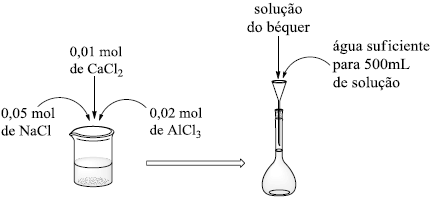
Considerando que todos os sais se dissolveram completamente, calcule a concentração molar de Cl- na solução preparada.
Provas
Uma amostra de 20 mL de uma solução aquosa 0,1 M de amônia foi diluída para um volume final de 400 mL. Calcule a concentração molar de íons OH- na solução diluída, sabendo que a amônia (NH3) possui Kb igual a 1,8 x 10-5.
Provas
Foi dada a um técnico a tarefa de determinar a solubilidade em água de uma substância X desconhecida. O técnico observou tratar-se de um sólido branco não-volátil e a partir de alguns experimentos chegou à seguinte curva de solubilidade:
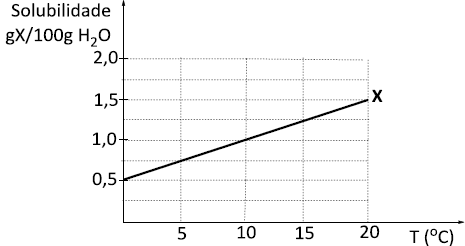
Considerando os dados apresentados, calcule o volume de água necessário para o preparo de uma solução que contenha 15,0 g do soluto X, a 5 ºC.
Provas
O petróleo bruto é uma mistura de muitos compostos, especialmente hidrocarbonetos. A refinaria é o local onde ocorre a separação desses compostos por meio de processos que se baseiam nas diferentes propriedades físicas de cada substância. Deste modo, é possível produzir a partir do óleo cru muitos derivados de petróleo, desde os mais leves, como GLP e solventes, até os mais pesados, como óleos lubrificantes e asfalto, entre outros. É correto afirmar que o principal processo de separação empregado numa refinaria é
Provas
O esquema abaixo mostra três reações cujo material de partida é o propanaldeído. A partir dele é possível obter ácido propanoico, n-propanol ou 2-butanol, por via das reações 1, 2 e 3, respectivamente.
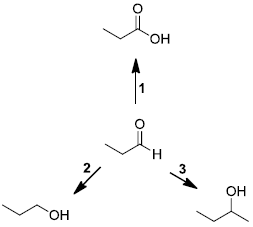
Sobre essas reações, assinale a alternativa incorreta.
Provas
Ao entregar diferentes alíquotas da mesma amostra padrão para quatro analistas, solicitou-se que a concentração de Fe3+ fosse determinada através de análise em quadruplicata.
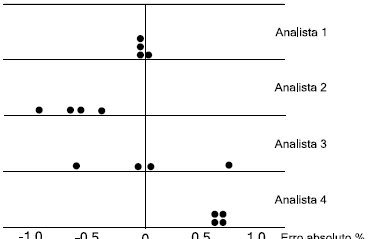
De acordo com o esquema acima, em que cada ponto representa uma medida, é correto afirmar que:
Provas
Caderno Container