Foram encontradas 353 questões.
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
A tabela a seguir apresenta as entalpias de ligações que podem ser formadas entre átomos de carbono, oxigênio e hidrogênio.
|
ligações |
entalpia de ligação |
|
C–C |
347 |
|
H–H |
436 |
|
C–H |
414 |
|
O–H |
464 |
|
O=O |
496 |
|
C=O |
743 |
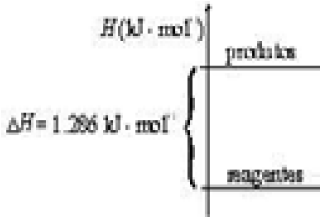
Considerando essas informações, conclui-se que o \( \varDelta \)H da reação de número X apresentada no texto, a 25 ºC e 1 atm, pode ser corretamente representado pelo gráfico abaixo.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
A diferença de eletronegatividade entre o oxigênio e o carbono faz a molécula de dióxido de carbono apresentar um momento de dipolo maior que o da molécula de hidrogênio, o que torna o dióxido de carbono mais solúvel em água que o hidrogênio.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
As taxas de desenvolvimento das reações representadas pelas equações VII, VIII e IX aumentam com a temperatura, mas as entalpias dessas reações em diferentes temperaturas, como, por exemplo, a 25 ºC e a 390 ºC, são idênticas, porque as entalpias das substâncias independem da temperatura.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
Considere que a reação VII se processe totalmente em fase gasosa em vez de em fase aquosa, seguindo a mesma estequiometria da equação apresentada, e que as substâncias que participam dessa reação se comportem segundo a lei dos gases ideais. Considere, ainda, que essa reação ocorra em um recipiente rígido e fechado, à temperatura constante e com quantidades estequiométricas dos reagentes no interior do recipiente, sob uma pressão total igual a p1. Nesse caso, é correto afirmar que, após o consumo total dos reagentes na reação, a pressão total final no interior do recipiente será igual a \( \left ( \dfrac{4n+2}{6n+m} \right )p1. \)
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
A seguinte equação química representa corretamente a reação global do processo de serpentinização mencionado no texto:
6Fe2SiO4 + 12Mg2SiO4 + 21H2O → 3H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4 + 8Mg3Si2O5(OH)4
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
Infere-se das informações do texto que os compostos Fe2SiO4 e Mg2SiO4 são óxidos básicos.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
Uma das reações mencionadas no texto é fotoquímica. Em diversos vegetais, ocorrem reações fotoquímicas, que se processam nos tilacóides e têm como conseqüência a formação de ATP.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
Na Terra, a produção de metano por microrganismos ocorre predominantemente pelo processo da quimiossíntese.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
O metano produzido na Terra contribui para o efeito estufa na atmosfera terrestre.
Provas
Durante muito tempo pensou-se em Marte como um provável lugar para abrigar vida. A descoberta de metano em sua atmosfera tornou-se a primeira evidência de que isso seria possível. Essa descoberta sugere que, nesse planeta, esteja ocorrendo uma intensa atividade subterrânea biológica ou geoquímica. Sem essas atividades, o nível de metano em Marte, provavelmente, seria zero, uma vez que esse gás é rapidamente eliminado, por exemplo, pelas reações apresentadas a seguir.
I 2CH4 ![]() C2H6 + H2
C2H6 + H2
II H2O + CH4 → H2CO + 2H2
III H2O2 + 2CH4 → 2H2CO + 3H2
Os processos astronômicos e geológicos conhecidos, como as poeiras de meteoritos e os impactos de cometas e vulcões, que são fontes convencionais de metano, não conseguiriam repor o gás consumido pelas reações apresentadas. Uma fonte possível desse gás é a hidrogeoquímica, como as emanações hidrotérmicas. Nas condições que determinam essas emanações, os silicatos ultramáficos (rochas ricas em ferro e magnésio) podem reagir para produzir hidrogênio, em um processo conhecido como serpentinização, cujas reações são as apresentadas em IV, V e VI, sendo que a reação VI se processa com o consumo de produtos gerados em IV e V.
IV 6Fe2SiO4 + 7H2O → H2(aq) + 3Fe3Si2O5(OH)4 + Fe3O4
V 2Mg2SiO4 + 3H2O → Mg3Si2O5(OH)4 + Mg(OH)2
VI 2Fe3Si2O5(OH)4 + 6Mg(OH)2 →
2H 2(aq) + 2Mg3Si2O5(OH)4 + 2Fe3O4 + 4H2O
As reações do hidrogênio produzido na reação VI com grãos de carbono, dióxido de carbono ou minerais carbonatados produzem metano, de acordo com as seguintes reações.
VII CO2(aq) + \( \left [2 + \dfrac{m}{2n} \right ] \) H2(aq) → \( \left ( \dfrac{1}{n} \right ) \) CnHm + 2H2O
VIII CO2(aq) + 4H2(aq) → CH4 + 2H2O
IX C + 2H2(aq) → CH4
Essas reações, quando realizadas em laboratório, à pressão de 400 Pa, temperatura de 390 oC e com óxidos de cromo e ferro como catalisadores, produzem grande quantidade de metano.
Uma outra fonte de metano a ser considerada é a microbiana. Na Terra, microrganismos conhecidos como metanógenos produzem metano em reações que envolvem o consumo de hidrogênio, dióxido de carbono ou monóxido de carbono. As reações a seguir ilustram esse processo.
X 4CO + 2H2O → CH4 + 3CO2
XI 4H2 + CO2 → CH4 + 2H2O
O metano produzido pode ser liberado para a atmosfera, talvez por perda gradual do gás através de rachaduras e fissuras ou por emissões esporádicas de vulcões.
Scientific American Brasil, n.o 6, jun./2007 (com adaptações).
Com base nas informações do texto, julgue os itens de 19 a 33.
Na reação II, observa-se variação do número oxidação de elementos quando são comparados os reagentes e os produtos.
Provas
Caderno Container