Foram encontradas 355 questões.
Fósseis, que são vestígios de organismos, servem como indicadores do processo evolutivo da vida na Terra. O processo mais utilizado para a datação de fósseis é aquele em que se utiliza o decaimento radioativo do isótopo carbono-14. Os nêutrons gerados pela radiação cósmica reagem com o nitrogênio atmosférico, produzindo, continuamente, carbono-14 e um próton, conforme a equação abaixo.
\( {}_0^1\!n+{}_{7}^{14}\!N\rightarrow{}_{6}^{14}\!C +{}_1^1\!H \)
Os átomos de \( {}_{6}^{14}\!C \) , recém-formados, cujo tempo de meia-vida é de 5.730 anos, combinam-se com átomos de oxigênio
da atmosfera para formar gás carbônico —\( {}_{6}^{14}\!CO_2(g) \) —, que é incorporado aos seres vivos por meio da fotossíntese, entrando, assim, na cadeia alimentar. O carbono-12 decai continuamente, restabelecendo o \( {}_{7}^{14}\!N \) e gerando uma partícula $, conforme a equação seguinte.
\( {}_{6}^{14}\!C\rightarrow{}_{7}^{14}\!N+β \)
A incorporação do carbono-12 pelos organismos cessa com a morte dos organismos, porém o decaimento radioativo desse isótopo continua, diminuindo continuamente a proporção de \( {}_{6}^{14}\!C \) em relação ao isótopo estável \( {}_{6}^{12}\!C \)ou ao \( {}_{6}^{13}\!C \). O método de datação do carbono-14 consiste em medir-se a proporção de um dos isótopos \( {}_{6}^{12}\!C \) e \( {}_{6}^{13}\!C \) em relação ao isótopo \( {}_{6}^{14}\!C \) . Comparando-se essas proporções com as encontradas na atmosfera, é possível estimar, com bastante precisão, o tempo transcorrido a partir da morte de um organismo.
Considerando as informações do texto, julgue o item seguinte.
O átomo de \( {}_{6}^{14}\!C \) é isóbaro do átomo de \( {}_{7}^{14}\!N \) .
Provas
Fósseis, que são vestígios de organismos, servem como indicadores do processo evolutivo da vida na Terra. O processo mais utilizado para a datação de fósseis é aquele em que se utiliza o decaimento radioativo do isótopo carbono-14. Os nêutrons gerados pela radiação cósmica reagem com o nitrogênio atmosférico, produzindo, continuamente, carbono-14 e um próton, conforme a equação abaixo.
\( {}_0^1\!n+{}_{7}^{14}\!N\rightarrow{}_{6}^{14}\!C +{}_1^1\!H \)
Os átomos de \( {}_{6}^{14}\!C \) , recém-formados, cujo tempo de meia-vida é de 5.730 anos, combinam-se com átomos de oxigênio
da atmosfera para formar gás carbônico —\( {}_{6}^{14}\!CO_2(g) \) —, que é incorporado aos seres vivos por meio da fotossíntese, entrando, assim, na cadeia alimentar. O carbono-12 decai continuamente, restabelecendo o \( {}_{7}^{14}\!N \) e gerando uma partícula $, conforme a equação seguinte.
\( {}_{6}^{14}\!C\rightarrow{}_{7}^{14}\!N+β \)
A incorporação do carbono-12 pelos organismos cessa com a morte dos organismos, porém o decaimento radioativo desse isótopo continua, diminuindo continuamente a proporção de \( {}_{6}^{14}\!C \) em relação ao isótopo estável \( {}_{6}^{12}\!C \)ou ao \( {}_{6}^{13}\!C \). O método de datação do carbono-14 consiste em medir-se a proporção de um dos isótopos \( {}_{6}^{12}\!C \) e \( {}_{6}^{13}\!C \) em relação ao isótopo \( {}_{6}^{14}\!C \) . Comparando-se essas proporções com as encontradas na atmosfera, é possível estimar, com bastante precisão, o tempo transcorrido a partir da morte de um organismo.
Considerando as informações do texto, julgue o item seguinte.
O átomo de \( {}_{6}^{14}\!C \) possui 6 nêutrons em seu núcleo.
Provas
Fósseis, que são vestígios de organismos, servem como indicadores do processo evolutivo da vida na Terra. O processo mais utilizado para a datação de fósseis é aquele em que se utiliza o decaimento radioativo do isótopo carbono-14. Os nêutrons gerados pela radiação cósmica reagem com o nitrogênio atmosférico, produzindo, continuamente, carbono-14 e um próton, conforme a equação abaixo.
\( {}_0^1\!n+{}_{7}^{14}\!N\rightarrow{}_{6}^{14}\!C +{}_1^1\!H \)
Os átomos de \( {}_{6}^{14}\!C \) , recém-formados, cujo tempo de meia-vida é de 5.730 anos, combinam-se com átomos de oxigênio
da atmosfera para formar gás carbônico —\( {}_{6}^{14}\!CO_2(g) \) —, que é incorporado aos seres vivos por meio da fotossíntese, entrando, assim, na cadeia alimentar. O carbono-12 decai continuamente, restabelecendo o \( {}_{7}^{14}\!N \) e gerando uma partícula $, conforme a equação seguinte.
\( {}_{6}^{14}\!C\rightarrow{}_{7}^{14}\!N+β \)
A incorporação do carbono-12 pelos organismos cessa com a morte dos organismos, porém o decaimento radioativo desse isótopo continua, diminuindo continuamente a proporção de \( {}_{6}^{14}\!C \) em relação ao isótopo estável \( {}_{6}^{12}\!C \)ou ao \( {}_{6}^{13}\!C \). O método de datação do carbono-14 consiste em medir-se a proporção de um dos isótopos \( {}_{6}^{12}\!C \) e \( {}_{6}^{13}\!C \) em relação ao isótopo \( {}_{6}^{14}\!C \) . Comparando-se essas proporções com as encontradas na atmosfera, é possível estimar, com bastante precisão, o tempo transcorrido a partir da morte de um organismo.
Considerando as informações do texto, julgue o item seguinte.
Como qualquer emissão radioativa, a radiação gerada pelo decaimento do carbono-14 é prejudicial ao organismo vivo, pois provoca danos genéticos.
Provas
Fósseis, que são vestígios de organismos, servem como indicadores do processo evolutivo da vida na Terra. O processo mais utilizado para a datação de fósseis é aquele em que se utiliza o decaimento radioativo do isótopo carbono-14. Os nêutrons gerados pela radiação cósmica reagem com o nitrogênio atmosférico, produzindo, continuamente, carbono-14 e um próton, conforme a equação abaixo.
\( {}_0^1\!n+{}_{7}^{14}\!N\rightarrow{}_{6}^{14}\!C +{}_1^1\!H \)
Os átomos de \( {}_{6}^{14}\!C \) , recém-formados, cujo tempo de meia-vida é de 5.730 anos, combinam-se com átomos de oxigênio
da atmosfera para formar gás carbônico —\( {}_{6}^{14}\!CO_2(g) \) —, que é incorporado aos seres vivos por meio da fotossíntese, entrando, assim, na cadeia alimentar. O carbono-12 decai continuamente, restabelecendo o \( {}_{7}^{14}\!N \) e gerando uma partícula $, conforme a equação seguinte.
\( {}_{6}^{14}\!C\rightarrow{}_{7}^{14}\!N+β \)
A incorporação do carbono-12 pelos organismos cessa com a morte dos organismos, porém o decaimento radioativo desse isótopo continua, diminuindo continuamente a proporção de \( {}_{6}^{14}\!C \) em relação ao isótopo estável \( {}_{6}^{12}\!C \)ou ao \( {}_{6}^{13}\!C \). O método de datação do carbono-14 consiste em medir-se a proporção de um dos isótopos \( {}_{6}^{12}\!C \) e \( {}_{6}^{13}\!C \) em relação ao isótopo \( {}_{6}^{14}\!C \) . Comparando-se essas proporções com as encontradas na atmosfera, é possível estimar, com bastante precisão, o tempo transcorrido a partir da morte de um organismo.
Considerando as informações do texto, julgue o item seguinte.
É correto concluir que a partícula \( β \), referida no texto, corresponde a um próton que abandona o núcleo do átomo de \( {}_{6}^{14}\!C \) , restabelecendo o \( {}_{7}^{14}\!N \).
Provas
Texto para o item.
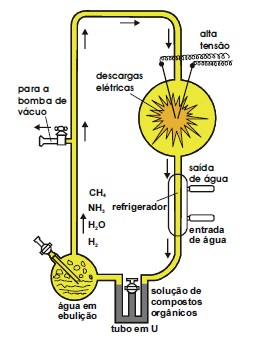
Stanley Miller ficou conhecido pelos seus trabalhos acerca da origem da vida, orientados por Harold Clayton Urey. Em um dos seus experimentos, esquematizado na figura acima, Miller introduziu, em um recipiente, uma mistura de hidrogênio, água, amônia e metano — uma versão artificial da suposta atmosfera terrestre primitiva. Por meio de dois eletrodos, ele disparou cargas elétricas para simular o efeito de relâmpagos. Após uma semana de experimento, Miller observou a produção espontânea de glicina, um dos aminoácidos que compõem os seres vivos. Esse trabalho ficou conhecido como experimento de Urey-Miller, e o material formado, composto de água quente, aminoácidos e outras substâncias que teriam se formado espontaneamente, foi denominado sopa prebiótica. Uma das hipóteses aceitas atualmente para a formação de glicina é a de que a atmosfera primitiva continha N2, CO e CO2, além dos gases previamente
mencionados. Esses gases reagiriam formando pequenas moléculas, tais como HCN e HCHO, segundo as reações descritas pelas equações abaixo.
2CH4 + N2 \( → \) 2HCN + 3H2
CO + NH3 \( → \) HCN + H2O
CO + 2H2 \( → \)CH3OH
CO2 + 3H2 \( → \) CH3OH + H2O
CH3OH \( → \) HCHO + H2
As substâncias HCN e HCHO continuariam a reagir formando substâncias mais complexas, entre os quais a glicina, como representado a seguir.
HCHO + NH3 \( → \) H2NCH2OH
H2NCH2OH \( → \) HNCH2 + H2O
HNCH2 + HCN\( → \) H2NCH2CN
H2NCH2CN + 2H2O \( → \) H2NCH2COOH + NH3
Considere que Urey e Miller tenham conseguido obter glicina, em seu experimento, por meio da reação simplificada representada pela equação a seguir.
2CH4(g) + NH3(g) + 2H2O(l) \( → \) C2H5NO2(aq) + 5H2(g)
Com base nessa consideração e admitindo ainda que a reação acima tenha sido a única ocorrida no referido experimento, julgue o próximo item.
Caso a temperatura do sistema tenha sido mantida constante ao longo de todo o experimento, então a pressão interna do recipiente caiu continuamente à medida que a glicina foi sintetizada.
Provas
Texto para o item.

Stanley Miller ficou conhecido pelos seus trabalhos acerca da origem da vida, orientados por Harold Clayton Urey. Em um dos seus experimentos, esquematizado na figura acima, Miller introduziu, em um recipiente, uma mistura de hidrogênio, água, amônia e metano — uma versão artificial da suposta atmosfera terrestre primitiva. Por meio de dois eletrodos, ele disparou cargas elétricas para simular o efeito de relâmpagos. Após uma semana de experimento, Miller observou a produção espontânea de glicina, um dos aminoácidos que compõem os seres vivos. Esse trabalho ficou conhecido como experimento de Urey-Miller, e o material formado, composto de água quente, aminoácidos e outras substâncias que teriam se formado espontaneamente, foi denominado sopa prebiótica. Uma das hipóteses aceitas atualmente para a formação de glicina é a de que a atmosfera primitiva continha N2, CO e CO2, além dos gases previamente
mencionados. Esses gases reagiriam formando pequenas moléculas, tais como HCN e HCHO, segundo as reações descritas pelas equações abaixo.
2CH4 + N2 \( → \) 2HCN + 3H2
CO + NH3 \( → \) HCN + H2O
CO + 2H2 \( → \)CH3OH
CO2 + 3H2 \( → \) CH3OH + H2O
CH3OH \( → \) HCHO + H2
As substâncias HCN e HCHO continuariam a reagir formando substâncias mais complexas, entre os quais a glicina, como representado a seguir.
HCHO + NH3 \( → \) H2NCH2OH
H2NCH2OH \( → \) HNCH2 + H2O
HNCH2 + HCN\( → \) H2NCH2CN
H2NCH2CN + 2H2O \( → \) H2NCH2COOH + NH3
Considerando o texto acima, julgue o item.
É correto concluir que, no experimento de Urey-Miller, a produção de glicina a partir dos gases mencionados é um processo endotérmico.
Provas
Texto para o item.

Stanley Miller ficou conhecido pelos seus trabalhos acerca da origem da vida, orientados por Harold Clayton Urey. Em um dos seus experimentos, esquematizado na figura acima, Miller introduziu, em um recipiente, uma mistura de hidrogênio, água, amônia e metano — uma versão artificial da suposta atmosfera terrestre primitiva. Por meio de dois eletrodos, ele disparou cargas elétricas para simular o efeito de relâmpagos. Após uma semana de experimento, Miller observou a produção espontânea de glicina, um dos aminoácidos que compõem os seres vivos. Esse trabalho ficou conhecido como experimento de Urey-Miller, e o material formado, composto de água quente, aminoácidos e outras substâncias que teriam se formado espontaneamente, foi denominado sopa prebiótica. Uma das hipóteses aceitas atualmente para a formação de glicina é a de que a atmosfera primitiva continha N2, CO e CO2, além dos gases previamente
mencionados. Esses gases reagiriam formando pequenas moléculas, tais como HCN e HCHO, segundo as reações descritas pelas equações abaixo.
2CH4 + N2 \( → \) 2HCN + 3H2
CO + NH3 \( → \) HCN + H2O
CO + 2H2 \( → \)CH3OH
CO2 + 3H2 \( → \) CH3OH + H2O
CH3OH \( → \) HCHO + H2
As substâncias HCN e HCHO continuariam a reagir formando substâncias mais complexas, entre os quais a glicina, como representado a seguir.
HCHO + NH3 \( → \) H2NCH2OH
H2NCH2OH \( → \) HNCH2 + H2O
HNCH2 + HCN\( → \) H2NCH2CN
H2NCH2CN + 2H2O \( → \) H2NCH2COOH + NH3
Considerando o texto acima, julgue o item.
O ácido cianídrico (HCN) é um ácido inorgânico fraco, que, em solução aquosa, dissocia-se de acordo com a equação HCN(aq) \( \rightleftharpoons \) H+(aq) + CN-(aq), cuja constante de equilíbrio K pode ser corretamente representada pela expressão abaixo.
\( k=\dfrac{[H^+][CN^-]}{HCN} \)
Provas
Texto para o item.

Stanley Miller ficou conhecido pelos seus trabalhos acerca da origem da vida, orientados por Harold Clayton Urey. Em um dos seus experimentos, esquematizado na figura acima, Miller introduziu, em um recipiente, uma mistura de hidrogênio, água, amônia e metano — uma versão artificial da suposta atmosfera terrestre primitiva. Por meio de dois eletrodos, ele disparou cargas elétricas para simular o efeito de relâmpagos. Após uma semana de experimento, Miller observou a produção espontânea de glicina, um dos aminoácidos que compõem os seres vivos. Esse trabalho ficou conhecido como experimento de Urey-Miller, e o material formado, composto de água quente, aminoácidos e outras substâncias que teriam se formado espontaneamente, foi denominado sopa prebiótica. Uma das hipóteses aceitas atualmente para a formação de glicina é a de que a atmosfera primitiva continha N2, CO e CO2, além dos gases previamente
mencionados. Esses gases reagiriam formando pequenas moléculas, tais como HCN e HCHO, segundo as reações descritas pelas equações abaixo.
2CH4 + N2 \( → \) 2HCN + 3H2
CO + NH3 \( → \) HCN + H2O
CO + 2H2 \( → \)CH3OH
CO2 + 3H2 \( → \) CH3OH + H2O
CH3OH \( → \) HCHO + H2
As substâncias HCN e HCHO continuariam a reagir formando substâncias mais complexas, entre os quais a glicina, como representado a seguir.
HCHO + NH3 \( → \) H2NCH2OH
H2NCH2OH \( → \) HNCH2 + H2O
HNCH2 + HCN\( → \) H2NCH2CN
H2NCH2CN + 2H2O \( → \) H2NCH2COOH + NH3
Considerando o texto acima, julgue o item.
O nome oficial (IUPAC) da substância representada por HCHO é metanal.
Provas
Texto para o item.

Stanley Miller ficou conhecido pelos seus trabalhos acerca da origem da vida, orientados por Harold Clayton Urey. Em um dos seus experimentos, esquematizado na figura acima, Miller introduziu, em um recipiente, uma mistura de hidrogênio, água, amônia e metano — uma versão artificial da suposta atmosfera terrestre primitiva. Por meio de dois eletrodos, ele disparou cargas elétricas para simular o efeito de relâmpagos. Após uma semana de experimento, Miller observou a produção espontânea de glicina, um dos aminoácidos que compõem os seres vivos. Esse trabalho ficou conhecido como experimento de Urey-Miller, e o material formado, composto de água quente, aminoácidos e outras substâncias que teriam se formado espontaneamente, foi denominado sopa prebiótica. Uma das hipóteses aceitas atualmente para a formação de glicina é a de que a atmosfera primitiva continha N2, CO e CO2, além dos gases previamente
mencionados. Esses gases reagiriam formando pequenas moléculas, tais como HCN e HCHO, segundo as reações descritas pelas equações abaixo.
2CH4 + N2 \( → \) 2HCN + 3H2
CO + NH3 \( → \) HCN + H2O
CO + 2H2 \( → \)CH3OH
CO2 + 3H2 \( → \) CH3OH + H2O
CH3OH \( → \) HCHO + H2
As substâncias HCN e HCHO continuariam a reagir formando substâncias mais complexas, entre os quais a glicina, como representado a seguir.
HCHO + NH3 \( → \) H2NCH2OH
H2NCH2OH \( → \) HNCH2 + H2O
HNCH2 + HCN\( → \) H2NCH2CN
H2NCH2CN + 2H2O \( → \) H2NCH2COOH + NH3
Considerando o texto acima, julgue o item.
A sopa prebiótica mencionada não continha inicialmente moléculas orgânicas, as quais surgiram depois, em decorrência de reações químicas estimuladas por descargas elétricas.
Provas
Texto para o item.

Stanley Miller ficou conhecido pelos seus trabalhos acerca da origem da vida, orientados por Harold Clayton Urey. Em um dos seus experimentos, esquematizado na figura acima, Miller introduziu, em um recipiente, uma mistura de hidrogênio, água, amônia e metano — uma versão artificial da suposta atmosfera terrestre primitiva. Por meio de dois eletrodos, ele disparou cargas elétricas para simular o efeito de relâmpagos. Após uma semana de experimento, Miller observou a produção espontânea de glicina, um dos aminoácidos que compõem os seres vivos. Esse trabalho ficou conhecido como experimento de Urey-Miller, e o material formado, composto de água quente, aminoácidos e outras substâncias que teriam se formado espontaneamente, foi denominado sopa prebiótica. Uma das hipóteses aceitas atualmente para a formação de glicina é a de que a atmosfera primitiva continha N2, CO e CO2, além dos gases previamente
mencionados. Esses gases reagiriam formando pequenas moléculas, tais como HCN e HCHO, segundo as reações descritas pelas equações abaixo.
2CH4 + N2 \( → \) 2HCN + 3H2
CO + NH3 \( → \) HCN + H2O
CO + 2H2 \( → \)CH3OH
CO2 + 3H2 \( → \) CH3OH + H2O
CH3OH \( → \) HCHO + H2
As substâncias HCN e HCHO continuariam a reagir formando substâncias mais complexas, entre os quais a glicina, como representado a seguir.
HCHO + NH3 \( → \) H2NCH2OH
H2NCH2OH \( → \) HNCH2 + H2O
HNCH2 + HCN\( → \) H2NCH2CN
H2NCH2CN + 2H2O \( → \) H2NCH2COOH + NH3
Considerando o texto acima, julgue o item.
A partir das equações apresentadas, é correto afirmar que a reação entre um aldeído e a amônia pode formar um aminoálcool.
Provas
Caderno Container