Foram encontradas 685 questões.
O nitrato de prata, contido em 40 mL de uma solução, reagiu com excesso de cloreto de sódio. O cloreto de prata produzido foi recolhido, seco e pesado dando 0,2868 g. A concentração molar (mol L-1) da solução de nitrato de prata era
DADOS: Ag = 107,9 g mol-1; Cl = 35,5 g mol-1; O = 16,0 g mol-1; N = 14,0 g mol-1
Provas
Sobre o ponto de equivalência, na volumetria de neutralização, é correto afirmar:
Provas
A vidraria do desenho abaixo é uma
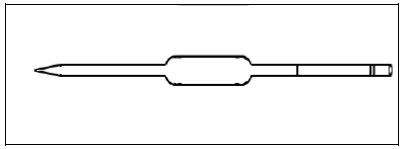
Provas
Em relação à manipulação de reagentes ácidos em laboratórios químicos, considere as seguintes afirmativas.
I. O ácido fluorídrico deve ser armazenado em frascos de plástico.
II. Na diluição de um ácido concentrado deve-se primeiro colocar a água e depois adicionar o ácido.
III. Uma solução de 3 partes de HNO3 e uma parte de HCl é conhecida como água régia.
IV. Soluções ácidas diluídas somente podem ser manipuladas em capela.
Estão corretas as afirmativas
Provas
Uma massa de 52,4 g de nitrato de bário foi completamente dissolvida com 200 mL de água em um becker. A solução foi transferida para um balão volumétrico de 500 mL e a quantidade necessária de água foi acrescentada até a aferição. A concentração de íons nitrato na solução final, em mol L-1, é
DADOS: Ba = 138,0 g mol-1; O = 16,0 g mol-1; N = 14,0 g mol-1
Provas
Para obtenção do gás nitrogênio em laboratório, utiliza-se a decomposição térmica do nitrito de amônio, segundo a reação
\( NH_4NO_2 → N_2 + 2 H_2O \)
\( \Delta \)
Sabe-se que esta reação se processa com 80% de rendimento. A massa, em gramas, de nitrito de amônio necessária para se preparar 112 g de nitrogênio é
DADOS: O = 16,0 g mol-1; N = 14,0 g mol-1; H = 1,00 g mol-1
Provas
Na figura abaixo estão desenhados quatro aparelhos de vidro usados em laboratório.
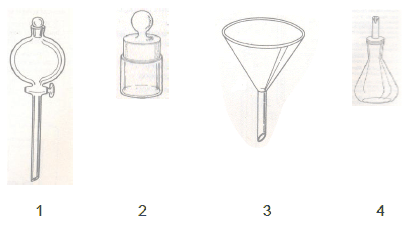
A alternativa que contém o número e a denominação correta das vidrarias é:
Provas
Observe a montagem abaixo.

O gás que está sendo produzido é o
Provas
Deseja-se preparar 5,00 x 10-1 L de uma solução de KOH 5,60% (m/v) a partir de uma solução estoque de KOH 2,50 mol L-1. O volume, em litros, que deve ser retirado da solução estoque é
DADOS: K = 39,0 g mol-1; O = 16,0 g mol-1; H = 1,00 g mol-1
Provas
O ácido clorídrico pode ser preparado pela reação, com aquecimento, de cloreto de sódio e ácido sulfúrico. Para se preparar 2433 g de uma solução 30% em massa de ácido clorídrico, a quantidade necessária de ácido sulfúrico, em gramas, é
DADOS: H = 1,00 g mol-1, O = 16,0 g mol-1, S = 32,0 g mol-1 e Cl = 35,5 g mol-1
Provas
Caderno Container