Foram encontradas 680 questões.
Numa titulação de 30 ml de um ácido fraco HA (Ka (25 ºC) = 1,34 x 10-5 mol.L-1), 0,1 mol.L-1 por NaOH 0,100 mol.L-1, o valor de pH no ponto onde [HA] = [A-] é:
Provas
Considere a reação entre piridina e água apresentada a seguir:
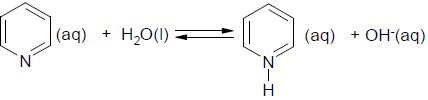
1. A piridina é uma base de Br⌀nsted-Lowry.
2. A piridina é uma base de Arrhenius.
3. A piridina é uma base fraca, pois é mais fraca que OH¯(aq).
4. OH¯(aq) é a base conjugada do ácido H2O.
Assinale a alternativa correta.
Provas
Com base na reação a seguir, identifique as afirmativas a seguir como verdadeiras (V) ou falsas (F).
LiH(s) + H2O(l) \( \longrightarrow \) Li+(aq) + OH-(aq) + H2(g)
( ) A reação descrita pela equação é de dupla troca.
( ) Nessa reação há mudança no NOX do lítio.
( ) É uma reação de oxirredução.
( ) O LiH tem caráter básico, pois ao dissolver torna o meio alcalino.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Numere a segunda coluna de acordo com sua correspondência com a primeira coluna.
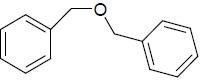
1. 
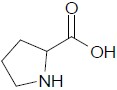
2. 
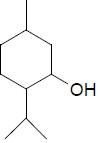
3. 
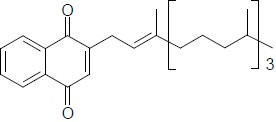
4. 
5. 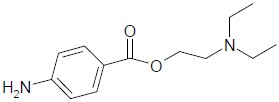
( ) Cetona.
( ) Álcool.
( ) Aminoácido.
( ) Éter.
( ) Éster.
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
Provas
Numere a segunda coluna com base na informação da primeira coluna.
1. Aℓ2O3.
2. Mg(OH)2.
3. H2SO4.
4. Na2HPO4.
( ) Sal.
( ) Ácido.
( ) Óxido.
( ) Base.
Assinale a alternativa que apresenta a numeração correta da segunda coluna, de cima para baixo.
Provas
Na fórmula estrutural do perclorato de sódio indicada a seguir, os pares de elétrons isolados foram omitidos:
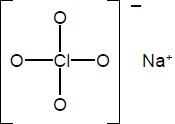
Sobre essa fórmula, considere as seguintes afirmativas:
1. A fórmula considera que a ligação entre Cℓ e O é covalente, e entre a unidade perclorato e sódio a ligação é iônica.
2. O NOX do Na é +1, do O é -2 e do Cℓ +7.
3. Nessa fórmula de Lewis, a carga formal do O é -1 e do Cℓ +1.
4. A geometria do íon perclorato é tetraédrica.
Assinale a alternativa correta.
Provas
Considere a configuração eletrônica do átomo de P (Z = 15) no estado fundamental. Para essa configuração, o último elétron preenchido ocupará o orbital de número quântico principal (n) igual a:
Provas
Ernest Rutherford, físico e químico de nacionalidade neozelandesa, foi laureado com prêmio Nobel em 1908 por suas investigações sobre a desintegração dos elementos e a química das substâncias radioativas. Por volta de 1910, Rutherford, com ajuda de um colega e de um aluno, realizou um experimento em que uma folha fina de ouro era bombardeada com partículas radioativas alfa, e um anteparo revestido com sulfeto de zinco era utilizado para detectar as partículas que atravessavam a folha de ouro. Com base nesse experimento, Rutherford propôs seu modelo atômico. Sobre esse modelo atômico, assinale a alternativa correta.
Provas
Numere a segunda coluna com base na informação da primeira coluna.
1. Grupo XVII, Halogênio.
2. Grupo II, Metal Alcalino Terroso.
3. Metal de Transição.
4. Grupo I, Metal Alcalino.
5. Lantanídeo.
6. Grupo XVI, Calcogênio.
( ) Potássio.
( ) Enxofre.
( ) Európio.
( ) Bromo.
( ) Cálcio.
( ) Zinco.
Assinale a alternativa que apresenta a numeração correta da segunda coluna, de cima para baixo.
Provas
Sabendo que o equivalente-grama do ácido clorídrico (HCℓ) é 36,5 g e que a densidade desse ácido concentrado é 1,19 g/mL, qual o volume de HCℓ concentrado necessário para o preparo de 1 L de uma solução 1 N de HCℓ?
Provas
Caderno Container