Foram encontradas 13.399 questões.
O uso de cromatografia para separar e identificar substâncias em uma mistura, é uma das técnicas experimentais mais versáteis da Química. Diversas são as técnicas: cromatografia gasosa, cromatografia de fase líquida, cromatografia de troca iônica, cromatografia por afinidade etc. Se hoje se usam colunas de cromatografia líquida super sofisticadas e de longos comprimentos, toda essa técnica nasceu da cromatografia de fase delgada e da cromatografia em papel. Mas os princípios básicos são sempre os mesmos. Trata-se de uma corrida entre moléculas que se deseja separar, identificar ou medir a concentração na mistura. Existe uma fase móvel, formada pelas moléculas sendo comparadas e um fluido carreador, que viaja através da fase estática. Essa fase estática, por sua vez, representa desafios diferenciados por afinidade ou por diferença com cada uma das moléculas que competem entre si. A medida que cada molécula termina o percurso estacionário, nessa corrida com obstáculos, seu tempo de prova pode ser registrado, que passará a identificá-la nas condições utilizadas. Instrumentos analíticos como espectrofotômetros de chama ou espectrômetros de massa etc. podem ser usados para corroborar as identificações dessas moléculas.
Ao final da corrida, plota-se um gráfico característico.
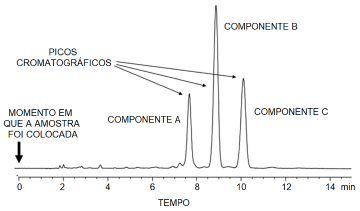
Considerando as informações do gráfico de HPLC (sigla em inglês de uma técnica cromatográfica, que se traduz como Cromatografia Líquida de Alta Performance), é correto afirmar que
Provas
A Cidade do México, Capital Federal do México, foi construída em solos formados por misturas de argila, fragmentos vulcânicos, areia e água, onde antes existia um lago profundo.
Sua consistência é pouco compactada e reage com liquefação/fluidificação momentânea na sua superfície, quando submetida a abalos sísmicos de grande magnitude, o que se repete a intervalos de algumas décadas entre si. Segundo o Professor James Jackson, Geofísico da Universidade de Cambridge, na Inglaterra, o solo macio da Cidade do México aumenta os efeitos dos sismos que lá acontecem, pois durante os abalos, o solo responde assumindo aspectos pseudoplásticos em seu comportamento, instabilizando as estruturas de sustentação das edificações. É como se suas fundações deixassem de se ancorar em terra firma durante os terremotos e se apoiassem por instantes em gelatina. Isso explica as enormes perdas em edificações e vidas humanas durante grandes terremotos, como o ocorrido em 1985.
O comportamento não newtoniano desse tipo de solos, mesmo na ausência de grandes abalos, responde também ao excesso de concentração de cargas em edifícios e permite o recalque das edificações, causando a sua inclinação ao longo do tempo. Fenômenos dessa natureza acontecem em várias partes do mundo onde areia, argila e água de origem sedimentar se acumulam por longos períodos. No Brasil, vemos o fenômeno do recalque em cerca de 65 prédios construídos na orla santista, que se inclinam um para o outro (apelidados de “edifícios amantes”).
Nesses projetos, foram utilizadas fundações de sapatas rasas, de 4 a 5 metros de profundidade, já que a investigação de solo realizada nos anos 1950s e 1960s apontou que o solo, até 12 metros de profundidade, se mostrava compacto. Porém, não sabiam que abaixo desse solo existia uma camada de solo mole e outras camadas de solos arenosos. Hoje, por segurança, as fundações de edifícios da orla santista, em especial entre os canais três e seis, são estruturas de estacas profundas, que se estendem cerca de 50 m abaixo da superfície, até atingirem rocha mãe, garantindo a estabilidade do prumo das construções mais recentes.
Alguns dos edifícios que sofreram recalques, chegaram a graus de inclinação maiores do que manda a norma e tiveram de sofrer intervenções de engenharia para solucionar seu problema.
Os casos de melhor sucesso no reajuste do prumo e estancamento das inclinações envolveram substituir as sapatas de baixa profundidade por uma elevação das estruturas rasas com macacos hidráulicos, drenagem de parte do solo inadequado, preenchimento com concreto formando um piso de sustentação, ancorado por um conjunto de estacas volumosas com profundidades ao redor de 50 m.
Com base no texto, sabe-se que os solos pseudoplásticos diminuem sua viscosidade conforme se deformam. Entretanto, a sua viscosidade também diminui com o passar do tempo em que estão sobre uma tensão (efeito tixotrópico). Quando deixados em repouso, tais solos fluidos retornam à viscosidade normal (voltam do estado liquidificado para o sólido). Também são exemplos desse mesmo tipo de comportamentos não-newtonianos a areia movediça, as tintas de paredes, as pastas de dentes e o ketchup. Apesar das semelhanças entre os problemáticos solos de comportamento não-newtonianos da Cidade do México – MX e de Santos – BR, ao longo das 5 últimas décadas, não se registraram casos de desabamento de prédios na orla santista, apesar das inclinações relatadas.
Assim, essa diferença de comportamento se deve
Provas
Ao medir alcalinidade, os resultados são normalmente expressos como ppm (ou mg/L) de Carbonato de Cálcio (CaCO3). Íons de hidróxido (OH–), íons de Bicarbonato (HCO3–) e íons de Carbonato (CO32-) também contribuem para a alcalinidade da água. A mesma unidade de medida pode ser indicadora da concentração dos íons de Ca2+.
Cátions como Ca2+ e Mg2+ devem ser controlados em águas recebidas para processos industriais, pois são fonte de sais de “dureza”. Sua presença em sistemas geradores de vapor pode ser danosa, já que sais desses cátions tendem a formar incrustrações e pontos de aderência em caldeiras e linhas de condução de vapor, prejudicando sua eficiência de troca térmica, gerando pontos de superaquecimento na tubulação e gastando mais combustível no processo. Isso se deve aos precipitados de carbonatos e sulfatos de Cálcio e Magnésio, insolúveis em água.
A melhor solução para esse problema está na prevenção, retirando tais cátions no processo de tratamento de água.
Os 2 principais tratamentos usados para garantir a qualidade da água a ser usada nas caldeiras são:
- Tratamento com fosfatos, que precipitam os sais de cálcio e magnésio, formando um lodo no fundo da caldeira que pode ser facilmente purgado;
- Tratamento com quelatos (como EDTA, por exemplo). Formam-se complexos solúveis com cálcio e magnésio, permitindo a indisponibilização dos mesmos para atacar as paredes das tubulações e da caldeira.
Em escala de laboratório, é comum se trabalhar com água deionizada por passagem em resinas de troca iônica ou até mesmo com água destilada, quando se precisa remover a dureza da água de trabalho.
Sobre essa mudança de procedimentos de trabalho entre a escala de laboratório e a escala industrial, é correto afirmar que
Provas
Alcalinidade total e pH são conceitos inter-relacionados, mas diferentes. O pH mede a concentração de íons H+ ou de OH- indicando o quanto uma solução é ácida ou básica, em uma escala absoluta e de crescimento exponencial. Por sua vez, a alcalinidade total indica quanto ácido ou base a solução pode absorver sem alterar de forma impactante seu pH. Em outras palavras, a alcalinidade total mede a capacidade de tamponamento de uma solução, uma certa elasticidade em absorver ácidos sem impactar os valores de pH. Essa capacidade de tamponamento é extremamente importante para a manutenção da vida, e é comum encontrarmos muitos exemplos de soluções tamponadas nos sistemas biológicos. Em fontes naturais de água, a alcalinidade varia de acordo com a geologia do local. Os minerais das rochas mais próximas e a permeação do solo influenciam dramaticamente a alcalinidade das águas adjacentes. Por exemplo, áreas com predominância de rochas de calcário terão uma alcalinidade maior em suas águas do que áreas com predominância de rochas graníticas. Ao medir alcalinidade, os resultados são normalmente expressos como ppm (ou mg/L) de Carbonato de Cálcio (CaCO3). Íons de hidróxido (OH–), íons de Bicarbonato (HCO3–) e íons de Carbonato (CO32-) também contribuem para a alcalinidade da água.
Diante do exposto, pode-se afirmar que o(a)
Provas
Quando se observam os catalizadores automobilísticos, vê-se que ajudam a promover a queima completa de vários gases que deixam o motor em reações de oxidação incompletas. Eles são fundamentais para a melhoria da qualidade do ar em grandes cidades, pois podem reduzir as emissões de gases altamente poluentes em até 80%.
Exemplo: Óxido de Nitrogênio, Monóxido de Carbono, Hidrocarbonetos diversos. Sua temperatura ideal de atuação catalítica gira ao redor de 400 °C até 800 °C. Os catalizadores são estruturas complexas, compostas por uma base cerâmica, com área cheia de microvilosidades, recobertos por diferentes materiais ativos, capazes de gerar sinergias entre eles. Por exemplo, a Platina é um metal nobre que atua melhor em ambientes com abundância de O2, oxidando os gases poluente de forma sequencial. Já em ambientes ou momentos com menor disponibilidade de oxigênio, o Ródio entra em ação, catalisando outros mecanismos de reação para formar gases menos poluentes.
A presença desses metais encarece o acessório dos veículos, mas a durabilidade pode se estender a toda a vida útil do automóvel, já que o catalisador nunca é consumido na reação.
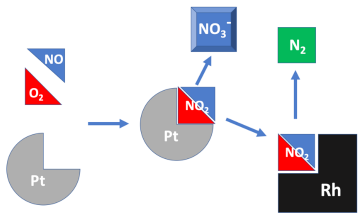
O mecanismo típico de catálise heterogênea envolve os seguintes passos:
Provas
O tratamento de água para linhas de vapor pode ser dividido em 3 partes: desaeração em “flasheamento”, tratamento químico e purgas.
Sobre o processo de purga, assinale a alternativa correta.
Provas
Considere os dados de massas atômicas e as massas molares abaixo para responder à questão.
Cl - 35,45 uma
I - 126,90 uma
Ag - 107,87 uma
Hg - 200,59 uma
Pb - 207,20 uma
AgCl - 143,32 g.mol-1
PbCl2 - 278,10 g.mol-1
Hg2Cl2 - 472,09 g.mol-1
AgI - 234,77 g.mol-1
PbI2 - 461,01 g.mol-1
Hg2I2 - 654,99 g.mol-1
O cloreto branco da questão anterior, que havia sido totalmente precipitado por solução HCl diluído, foi depois redissolvido em solução aquosa por aquecimento em banho-maria. O íon foi novamente precipitado, agora pela ação de uma solução de Iodeto de Potássio (KI), gerando um sal amarelo. Esse novo sal, foi filtrado, separado, seco e pesado em balança analítica, totalizando 9,22 g do sal de Iodeto para cada litro da amostra original.
Assinale a alternativa que apresenta a concentração molar desse íon encontrado na solução amostra original.
Provas
O precipitado branco da questão anterior (que havia sido completamente precipitado com HCl diluído), foi recolhido após filtração, recebeu mais 10 ml de água destilada e foi aquecido em banho-maria até a temperatura de ebulição da água, mantido assim por cerca de 5 minutos. Esse processo de aquecimento dissolveu todo material que estava precipitado. Isso indicou que apenas um dos 3 cloretos estava presente no sal branco que havia precipitado, já que dois deles são tão insolúveis que não se redissolveriam com o aquecimento na solução aquosa, sem que ocorressem mudanças no pH da solução.
Com base nas informações fornecidas, assinale a alternativa que apresenta qual dos 3 cátions estava presente na solução amostra: Ag+, Pb2+ ou Hg22+.
Provas
Analise as informações abaixo para responder à questão.
Os cloretos dos íons Prata (Ag+), Chumbo (Pb+2) e Mercuroso (Hg2+2) são insolúveis à temperatura ambiente em meio neutro ou ácido, e seus respectivos Kps e reações de precipitação são descritos a seguir.
Ag+ + Cl- !$ \rightarrow !$ AgCl (s) Kps = 1,82 . 10-10
Pb2+ + 2Cl- !$ \rightarrow !$ PbCl2 (s) Kps = 1,71 . 10-5
Hg22+ + 2Cl- !$ \rightarrow !$ Hg2Cl2 (s) Kps = 1,22 . 10-18
Em uma solução amostra, dentro de um tubo de ensaio, gotejou-se uma solução diluída de HCl em quantidade suficiente para causar a precipitação completa de sais brancos no fundo do tubo. A partir desse teste, sobre a composição da solução amostra antes da precipitação, pode-se concluir que
Provas
A pilha de Zinco/Óxido de Manganês pode ser representada pelas reações abaixo. A reação no ânodo será de formação de cloreto de zinco e liberação de um elétron:
Zn + 2 Cl− !$ \rightarrow !$ ZnCl2 + 2 e−
A reação no cátodo produz hidróxido de zinco e óxido de manganês (3+):
2 MnO2 + ZnCl2 + H2O + 2 e− !$ \rightarrow !$ Mn2O3 + Zn(OH)2 + 2 Cl−
A reação geral simplificada da pilha vai ser:
Zn + 2 MnO2 + H2O !$ \rightarrow !$ Mn2O3 + Zn(OH)2
Essas pilhas alcalinas fornecem um ddp de cerca de 1,5 volts, e como todas as pilhas, tendem a sofrer com a autodescarga e com reações de deterioração. Mesmo ficando sem uso, sua capacidade vai se degradando aos poucos, pois a placa de zinco na pilha vai sendo corroída com o tempo e ocorrem vazamentos que colocam os eletrólitos em contato. Esses processos de auto degradação são acelerados quando as pilhas são submetidas a temperaturas mais altas. Nesse tipo de pilha, cerca de 0,08% de sua capacidade é perdida a cada dia sob uma temperatura de 20 °C (ou seja, em 2 meses, sem usar a pilha, sua capacidade terá chegado a cerca de 94,5% do valor original). Essa degradação é fortemente acelerada, podendo chegar a 0,6% quando a temperatura ambiente é de 45 °C (em 2 meses, sem usar a pilha, sua capacidade terá chegado a cerca de 69,7% do valor original) reduzindo importantemente a vida útil da pilha.
Assim, mesmo sem estarem em uso, pilhas AAA alcalinas têm uma capacidade de armazenamento inicial que vai caindo mais ou menos rapidamente, a partir dos valores iniciais de 1250 miliamp.hora ou 1.87 watts.hora. Por conta disso, os fabricantes de pilhas recomendavam guardá-las sob refrigeração enquanto não estivessem em uso, (sempre protegidas em sacos plásticos para não entrarem em contato com alimentos). O barateamento desse tipo de pilha no mundo fez mudar tais recomendações, mas seus princípios seguem válidos. Dessa maneira, a refrigeração faria as pilhas serem melhor preservadas em sua capacidade, até o momento do uso. Segundo a equação de Arrhenius:
K = A.e -Ea /RT
Onde:
K é a constante de velocidade de uma reação química;
A é o chamado fator pré-exponencial;
Ea é a Energia de ativação da reação;
T é a Temperatura em °K .
Com base na equação acima, é correto afirmar que
Provas
Caderno Container