Foram encontradas 13.429 questões.
Leia o texto para responder a questão.
A poluição atmosférica pode ser relacionada com doenças respiratórias em uma população e com efeitos sobre a cognição dos seres humanos. Irritações nas vias respiratórias superiores, mucosas e casos de diabetes e outras são alguns dos problemas causados por esse tipo de poluição. Especificamente, os materiais particulados com dimensões inferiores a 1µm penetram no sistema respiratório até a superfície dos alvéolos pulmonares. Essas partículas, devido a sua elevada superfície específica, adsorvem e carregam poluentes orgânicos e inorgânicos para a corrente sanguínea. Tais poluentes devem ser combatidos, de modo a serem desenvolvidas políticas públicas para buscar a sua minimização.
A partir do texto, é incorreto afirmar que se deva
Provas
No mercado das carnes finas, frango, enlatados, carnes resfriadas e outros alimentos ricos em proteínas são empregadas substâncias químicas para realçar os sabores desses alimentos. A função de tais compostos, como por exemplo, o composto apresentado a seguir, se prestam a estimular as atividades das papilas degustativas, aumentando a secreção das células.
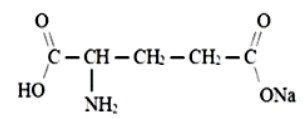
Considerando a fórmula estrutural e os grupos funcionais presentes no composto, exemplo, supramencionado, é correto afirmar que as funções orgânicas presentes no composto são
Provas
Sólidos “insolúveis”, com exceções, podem ser solubilizados de diferentes formas. No caso dos sólidos de MX (para X= C; B; Z) estes, em tese, podem ser solubilizados em água (H2O) pela adição de solução aquosa amoniacal (amônia solubilizada em água: NH4OH). Assim, para solubilizar a massa correspondente a 0,100 mol de cada um dos compostos supramencionados considerando os dados e reações com os respectivos valores de concentração de amônia total fornecidos a seguir, é correto afirmar que:
Dados de Kps MX= 1,0 x 10-10; 4 x 10-14; 8 x 10-19, respectivamente; !$ β !$= 2x10-7 ; Mol: NH3= 17; C= 36; B= 80; Z= 127; M= 108 g mol-1 ; !$ β !$ x k= kequilíbrio; CM(I)equilíbrio= 1x10-5 mol L-1.
Reações:
MX !$ \rightleftarrows !$ M+ + X-
MC + 2NH3 !$ \rightleftarrows !$ [M(NH3)2]+ + C- CNH3total= 1,2 M
MB + 2NH3 !$ \rightleftarrows !$ [M(NH3)2]+ + B- CNH3total= 2,3 M
MZ + 2NH3 !$ \rightleftarrows !$ [M(NH3)2]+ + Z- CNH3total= 140 M
Provas
Leia e analise o exposto para responder a questão.
No que tange ao solvente universal, ao se realizar a sua eletrólise, ele é decomposto nos constituintes: hidrogênio (H2) e oxigênio (O2). Após a realização do experimento de eletrólise e coletados os gases, tendo seus respectivos volumes anotados, foi possível montar o quadro anexo. Os resultados das medições de volumes, posterior à conversão à massa (vide o quadro), portanto, as medidas permitiram evidenciar que as massas dessas duas substâncias sempre estarão na mesma proporção (1:8), em acordo com a lei ponderal de Proust. Outro aspecto importante é o fato de que essas reações ocorrem, também, em acordo com a lei de Lavoisier, para um sistema reacional.
|
Experimento |
m H2O / g | m H2 / g |
m O2 / g |
| A | I | 0,5 | 4 |
| B | 9 | II | 8 |
| C | 18 | 2 | III |
| D | IV | 11,11 | 88,88 |
Quadro
Considerando o texto apresentado e o quadro anexo, é correto afirmar que as massas (expressas em g) a tomarem o lugar das indicações I, II, III e IV nos experimentos realizados de A até D, são, respectivamente
Provas
Considerando o conceito de equilíbrio ácido-base, apreendidos na etapa do ensino médio, ao se preparar uma solução aquosa, com água pura, adicionada de um sal de um ácido orgânico fraco (pka= 4,75), do tipo LiAc (Ac= CH3COO-), após o estabelecimento do equilíbrio químico a T= 25ºC, é correto afirmar que o pH da solução resultante é
(Dados: 1- CH3COO + H+ !$ \leftrightarrows !$ CH COOH; 2- H2O !$ \leftrightarrows !$ OH+ + H+)
Alternativas:
Provas
Os hidrocarbonetos são compostos orgânicos constituídos apenas por carbono (C) e hidrogênio (H). Essa classe de compostos é bastante ampla dada a estrutura eletrônica do átomo de C. Pertencendo ao grupo 14 da tabela periódica, o C pode compartilhar seus 4 elétrons de valência e formar quatro ligações covalentes fortes. Os átomos de C podem, ainda, ligarem-se uns aos outros formando cadeias longas, lineares, ramificadas e cíclicas. O átomo de carbono pode ainda utilizar duas ou mais de suas valências para formar ligações com um segundo átomo de carbono formando as, denominadas, cadeias insaturadas. Dada a grande possibilidade de conectividade, compostos com mais de três átomos de C podem apresentar a mesma fórmula molecular, porém, apresentando estruturas diferentes, as quais são denominados de isômeros. Considerando o exposto, é correto afirmar que o hidrocarboneto de fórmula C4H8apresenta um total de
Alternativas:
Provas
A reação de transesterificação é utilizada na modificação da estrutura química do óleo vegetal, de modo a torná-lo com propriedades físico-químicas compatíveis com as do óleo diesel. A reação ocorre entre as espécies químicas: triglicerídeo (vide estrutura geral na figura) com um álcool (R’OH), na presença de catalizador. Os produtos dessa reação são: ésteres alquílicos de ácidos graxos (RCOOR’) e glicerol (CH2(OH)CH(OH)CH2(OH)); produtos principais da reação. Considerando o exposto e as leis químicas, assinale a alternativa que contenha a estequiometria que define a reação química, após o balanceamento da equação química.
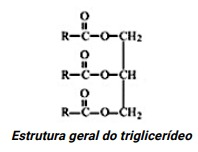
Alternativas:
Provas
O hipoclorito de sódio (NaOCl) é um composto de cloro com forte poder oxidativo. Por isto é muito utilizado como: alvejante de roupas, higienizador de superfícies e de alimentos, e na desinfecção de água para o consumo humano. No tratamento da água, por exemplo, garante a eliminação de patógenos durante o armazenamento e o transporte da água até as residências. Este produto é comercializado em concentração da ordem de 2,5% (m/m), podendo ser produzido a partir da reação da espécie química cloro com solução de hidróxido de sódio.
De acordo com o exposto, assinale a alternativa que contenha a reação que representa a formação do alvejante.
Alternativas:
Provas
Considerando o tema calor, uma situação crítica que enfrenta o planeta em muitas das regiões desenvolvidas e outras, está relacionado ao aumento brusco do teor de dióxido de carbono (CO2) na atmosfera, tendo como consequência efeitos deletérios à vida humana, animal e vegetal. Assim, é correto afirmar que, quando a energia interna de um sistema aumenta por transferência de energia, apenas na forma de calor, o parâmetro que se pode medir, e que aumentando tende a aumentar a entalpia proporcionalmente é
Alternativas:
Provas
Entre os medicamentos mais comuns consumidos para o alívio da dor está o ibuprofeno, um composto quiral com ação anti-inflamatória e efeito analgésico, que é comercializado como fármaco opticamente puro, ou seja, sem a mistura com outro isômero óptico. A fórmula estrutural plana do ibuprofeno é:
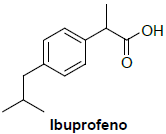
Além do ibuprofeno, destacam-se também os princípios ativos a seguir, presentes em outros medicamentos para o alívio da dor:
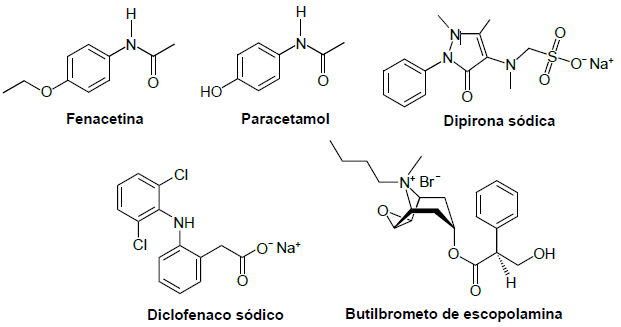
O princípio ativo que apresenta o mesmo tipo de isomeria espacial que o ibuprofeno é o(a)
Provas
Caderno Container