Foram encontradas 13.429 questões.
Considere que um mol de gás ideal, inicialmente a 27 ºC e 1 atm, contido em um sistema pistão-cilindro, se expanda isobaricamente até duplicar o seu volume inicial. A expansão ocorre gradativamente e não há atrito entre o pistão e as paredes do cilindro, tornado o processo reversível. Além disso, as paredes do sistema permitem a troca térmica entre o gás e as vizinhanças.
!$ R=8,314. Pa.m^3.K^{-1}.mol^{-1} !$
!$ PV=nRT !$
!$ T(K)=T(ºC)+2473 !$
Nesse contexto, a temperatura do gás, em ºC, ao final desse processo será igual a
Provas
Um investidor está considerando a possibilidade de implantar uma indústria de galvanização na região metropolitana de Belo Horizonte. Sobre a elaboração de um projeto básico de Engenharia para esse empreendimento, assinale com V afirmativas as verdadeiras e com F as falsas.
( ) Na elaboração de qualquer projeto, as etapas são realizadas em um processo de aproximações sucessivas.
( ) Em todo projeto trabalha-se com estimativas sobre o futuro, o que implica riscos quanto à certeza das previsões.
( ) Ao dar início a um projeto, ele deverá prosseguir até sua implantação, mesmo que as estimativas não sejam coincidentes com os valores encontrados.
Assinale a sequência correta.
Provas
Os equipamentos e as tubulações nos processos industriais são frequentemente fabricados com aço galvanizado, pelo fato de este ser um material mais resistente à corrosão do que o aço carbono. O processo de galvanização consiste em uma série de etapas, que vai desde a limpeza e o preparo das peças, passando pelas etapas de zincagem e cromagem, até a obtenção das peças finais. Nesse processo, são geradas várias correntes de efluentes que são todas reunidas em um tanque de armazenamento (ETE), conforme o diagrama apresentado a seguir.
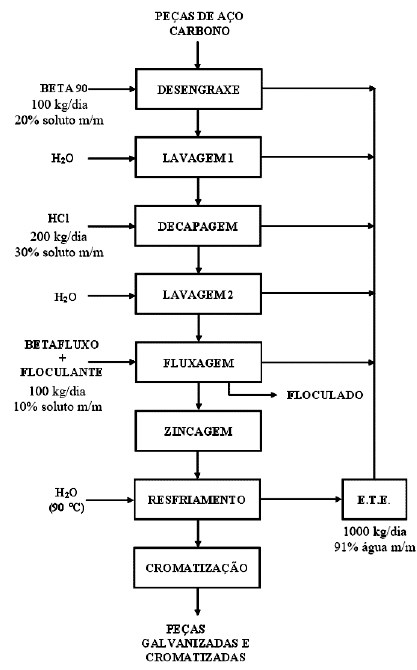
Após a realização da caracterização química do efluente, a concentração de Zn2+ encontrada foi de 654 mg.L-1.
Dados:
• Concentração de Zn2+ no efluente da ETE: 654 mg.L-1
• Massa molar do zinco: 65,4 g.mol-1
• Massa molar do oxigênio: 16,0 g.mol-1
• Volume diário de efluente recolhido na ET.E: 1000 L
• Dias trabalhados no mês: 20
Com base nas informações apresentadas, pode-se dizer que a massa de óxido de zinco, em quilogramas, acumulada na ETE em um mês de trabalho é
Provas
Os equipamentos e as tubulações nos processos industriais são frequentemente fabricados com aço galvanizado, pelo fato de este ser um material mais resistente à corrosão do que o aço carbono. O processo de galvanização consiste em uma série de etapas, que vai desde a limpeza e o preparo das peças, passando pelas etapas de zincagem e cromagem, até a obtenção das peças finais. Nesse processo, são geradas várias correntes de efluentes que são todas reunidas em um tanque de armazenamento (ETE), conforme o diagrama apresentado a seguir.

Para a caracterização química dos efluentes que chegam na ETE, é necessário determinar as concentrações dos metais presentes. Nesse contexto, analise as técnicas analíticas apresentadas a seguir.
I. Cromatografia gasosa
II. Espectrofotometria por absorção atômica
III. Espectroscopia no infravermelho por transformada de Fourier (FTIR)
É(são) técnica(s) que pode(m) ser utilizada(s) para a determinação da concentração de Zn2+ no efluente.
Provas
Os equipamentos e as tubulações nos processos industriais são frequentemente fabricados com aço galvanizado, pelo fato de este ser um material mais resistente à corrosão do que o aço carbono. O processo de galvanização consiste em uma série de etapas, que vai desde a limpeza e o preparo das peças, passando pelas etapas de zincagem e cromagem, até a obtenção das peças finais. Nesse processo, são geradas várias correntes de efluentes que são todas reunidas em um tanque de armazenamento (ETE), conforme o diagrama apresentado a seguir.

Deseja-se calcular a quantidade de água necessária, em litros/quilo de efluente total gerado, em cada uma das etapas de lavagem (lavagem 1 e lavagem 2) e na etapa de resfriamento, para um dia de processo.
Dados:
mLavagem 1 = mLavagem 2 = mResfriamento
!$ \rho !$H2O = 1000 kg/m3
Esse valor é:
Provas
Leia o texto para responder a questão.
O SARS-Cov-2, responsável pela epidemia do covid-19, nos anos de 2021 até o presente, necessitou e necessita de processo rápido e eficiente para a descontaminação de ambiente hospitalar em específico e materiais de trabalho. O ozônio (O3) foi um dos gases utilizados, solubilizado em água pura para o trabalho de desinfecção dos ambientes e materiais hospitalares, dentre outros. No entanto, problemas de ordem química se apresentam ao utilizar o ozônio devido a sua toxicidade e de seus subprodutos de reação no ambiente. Neste contexto, a literatura apresenta resultados evidenciando que em pessoas com comorbidades (asmáticos, idosos, cardíacos, entre outros) a variação na concentração de O3 pode acarretar graves efeitos colaterais, sendo que com o aumento em 10 ng/m3 , para uma exposição de curta duração, pode contribuir com 0,5% na mortalidade de pacientes/pessoas.
De acordo com o texto, é correto afirmar que o risco ao se empregar o O3 é devido a sua propriedade química de agente
Provas
Leia o texto para responder a questão.
No que tange à solubilidade das substâncias químicas, em água pura, a temperatura, T= 25 ºC, podemos ter como resultado distintos valores de concentrações, para os diferentes tipos de sais analisados em termos de suas solubilidades em g/100 g de solução. Como exemplo desses sais podem ser citados: NaCl; KIO3; AgBr; CaCO3, CaSO4; MgSO4; dentre outros. A partir do conhecimento das propriedades da Tabela Periódica e do quadro anexo, é possível apresentar uma classificação, em termos gerais de solubilidade dos compostos químicos supracitados.
Quadro. Relação entre cátions e ânions os quais poderão ser considerados solúveis ou insolúveis (praticamente)
|
Ânion |
Cátion |
Solubilidade em água |
|
Nitrato (NO 3 –1 ) |
Qualquer cátion |
Solúvel |
|
Nitrito (NO2 –1 ) |
Qualquer cátion |
Solúvel |
|
Acetato (H3C2O2 -1 ) |
Ag+1 e Hg2 +2 |
Praticamente insolúvel |
|
Halogenetos (F-1 , Cl-1 , Br-1 , l-1 ) |
Cu+1, Ag+1 , Pb+2 e Hg2 +2 |
Praticamente insolúvel |
|
Sulfato (SO4 -2 ) |
IIA (com exceção do Mg), Ag+1 , Pb+2 e Hg2 +2 |
Praticamente insolúvel |
|
Sulfeto (S-2 ) |
NH4 +1, ou metal das famílias IA e IIA |
Solúvel |
|
Carbonato (CO3 2 ) |
NH4 +1, ou metal das famílias IA |
Solúvel |
|
Fosfato (PO4 -3 ) |
NH4 +1, ou metal das famílias IA |
Solúvel |
|
Demais ânions |
NH4 +1, ou metal das famílias IA |
Solúvel |
IA e IIA: Família dos alcalinos e alcalinos-ferrosos
De acordo com o texto, é correto afirmar que os sais são
Provas
Uma grande variedade de substâncias como leite, o sangue e a gelatina fazem parte de uma classe de substâncias chamadas de coloides. Soluções verdadeiras e soluções coloidais apresentam uma única fase e não podem ser distinguidas a olho nu, e nem separadas por filtração simples. Porém a possibilidade de distinguir uma solução coloidal de uma solução verdadeira deve-se à
Provas
Efetivar o balanceamento químico do equilíbrio de oxido-redução é uma tarefa um tanto quanto difícil, pois além do balanço de massa deve ser efetivado o balanço de carga. No entanto, o balanceamento se torna mais fácil quando se conhece o número de elétrons trocados na reação, caso contrário o químico pode ser facilmente induzido ao erro. Assim, ao examinar a reação entre os íons Cr2O72- (íon dicromato, de coloração amarelada em meio aquoso) e as moléculas de peróxido de hidrogênio (H2O2, incolor), em meio de H2SO4 (ácido sulfúrico-incolor), e sabedor de que os produtos da reação são os íons, Cr(III), gás oxigênio (O2) e água (H2O) é possível escrever as equações químicas apresentadas a seguir:
I. Cr2O72- + 3 H2O2 + 8 H+ !$ \rightleftarrows !$ 2 Cr(III) + 3O2 + 7 H2O
II. 2 Cr2O72- + H2O2 + 6 H+ !$ \rightleftarrows !$ 2 Cr(II) + 3 O2 + 4 H2O
III. Cr2O72- + 3 H2O2 + 6 H+ !$ \rightleftarrows !$ 2 Cr(II) + 4 O2 + 7 H2O
IV. 2 Cr2O72- + 7 H2O2 + 8 H+ !$ \rightleftarrows !$ 2 Cr(III) + 6 O2 + 10 H2O
V. Cr2O72- + 7 H2O2 + 6 H+ !$ \rightleftarrows !$ 2 Cr(III) + 5O2 + 10 H2O
De posse das reações apresentadas e dos conceitos de balanceamento de reações químicas, assinale a alternativa com a equação redox corretamente balanceada.
Provas
Leia o texto para responder a questão.
O uso de CFC em muitos produtos comerciais encontra, na atualidade, uso restrito apenas à alguns equipamentos. Vários gases, na contemporaneidade, são dispensados na atmosfera e denominados de gases-estufa; outros gases também comprometedores são lançados na atmosfera e são passíveis de sofrerem reações químicas/fotoquímicas em presença do vapor de água, e acabam por originar a chuva ácida.
Considerando o texto apresentado, é correto afirmar que se apresentam como gases e vapor
Provas
Caderno Container