Foram encontradas 13.430 questões.
O presidente da Empresa Brasileira de Pesquisa e Inovação Industrial (Embrapii), Jorge Guimarães, avalia a ausência de um DNA independente no Brasil como um processo estrutural: “A maioria dos insumos químicos importados não é refinada, é coisa bem simples. O Brasil é o maior exportador de laranja e, mesmo assim, importa ácido cítrico. Bem como é o maior produtor de sacarose e importa glicose, que é metade da molécula. Tem coisas difíceis de explicar, responsáveis por gerar fragilidade. Esse efeito é responsável também pela deficiência no setor de medicamentos. A defasagem tecnológica ocorre continuamente com a importação dos quimioterápicos, ou seja, da grande parte dos princípios ativos e insumos que compõem os remédios, gerando enorme déficit na balança de pagamentos”.
Alana Ambrosio. Por que Brasil ainda é tão dependente de importações na área farmacêutica?
In: VivaBem UOL. Internet: <www.uol.com.br> (com adaptações).
O ácido cítrico (C6H8O7), também conhecido como ácido 2-hidroxi-1,2,3-propanotricarboxílico, é um ácido fraco triprótico, cujos pKa são: !$ pK_{a_1}\, = \, 3,15; \,\, pK_{a_2} \, = \, 4,77; \, pK_{a_3} \, = \, 6,40. !$
O suco de laranja possui densidade de 1.030 kg/m3, sendo a concentração de ácido cítrico no suco de laranja igual a 1,5 g/L.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3, julgue o item e assinale a opção correta no item, que é do tipo C.
A primeira constante de dissociação ácida do ácido cítrico !$ (K_{a_1}) !$ é superior a 10−3.
Provas
O presidente da Empresa Brasileira de Pesquisa e Inovação Industrial (Embrapii), Jorge Guimarães, avalia a ausência de um DNA independente no Brasil como um processo estrutural: “A maioria dos insumos químicos importados não é refinada, é coisa bem simples. O Brasil é o maior exportador de laranja e, mesmo assim, importa ácido cítrico. Bem como é o maior produtor de sacarose e importa glicose, que é metade da molécula. Tem coisas difíceis de explicar, responsáveis por gerar fragilidade. Esse efeito é responsável também pela deficiência no setor de medicamentos. A defasagem tecnológica ocorre continuamente com a importação dos quimioterápicos, ou seja, da grande parte dos princípios ativos e insumos que compõem os remédios, gerando enorme déficit na balança de pagamentos”.
Alana Ambrosio. Por que Brasil ainda é tão dependente de importações na área farmacêutica?
In: VivaBem UOL. Internet: <www.uol.com.br> (com adaptações).
O ácido cítrico (C6H8O7), também conhecido como ácido 2-hidroxi-1,2,3-propanotricarboxílico, é um ácido fraco triprótico, cujos pKa são: !$ pK_{a_1}\, = \, 3,15; \,\, pK_{a_2} \, = \, 4,77; \, pK_{a_3} \, = \, 6,40. !$
O suco de laranja possui densidade de 1.030 kg/m3, sendo a concentração de ácido cítrico no suco de laranja igual a 1,5 g/L.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3, julgue o item e assinale a opção correta no item, que é do tipo C.
A seguir, é apresentada a fórmula estrutural correta do ácido cítrico.
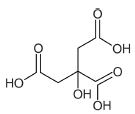
Provas
|
combustível |
fórmula | densidade (g/cm3) |
ponto de |
|
etanol |
C2H6O | 0,8 |
-114 |
|
octano |
C8H18 | 0,7 | -57 |
Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue o item e assinale a opção correta no item, que é do tipo C.
No etanol, os comprimentos das ligações entre os átomos de hidrogênio e os átomos vizinhos são equivalentes entre si.
Provas
|
combustível |
fórmula | densidade (g/cm3) |
ponto de |
|
etanol |
C2H6O | 0,8 |
-114 |
|
octano |
C8H18 | 0,7 | -57 |
Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue o item e assinale a opção correta no item, que é do tipo C.
Considere que um íon dicromato (Cr2O72-), de coloração alaranjada, tenha reagido em meio ácido para formar o íon cromo (III), de coloração verde, conforme semirreação a seguir.
Cr2O7 2− + 14 H+ + 6 e− !$ \rightarrow !$ 2 Cr3+ + 7 H2O
Considere, ainda, que, após gotejar excesso de uma solução ácida de dicromato em dois tubos de ensaio, um contendo octano e outro etanol, um dos tubos tenha formado uma solução verde. Dessas informações conclui-se que o tubo de ensaio cuja solução ficou verde continha etanol e que um dos produtos formados foi o ácido etanoico.
Provas
|
combustível |
fórmula | densidade (g/cm3) |
ponto de |
|
etanol |
C2H6O | 0,8 |
-114 |
|
octano |
C8H18 | 0,7 | -57 |
Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue o item e assinale a opção correta no item, que é do tipo C.
Considere-se que a densidade da água seja 1,0 g/cm3 e que o seu ponto de fusão seja 0 ºC. Nesse caso, é correto afirmar que, em uma mistura que contém partes iguais de octano, etanol e água, a 25 ºC, os seus componentes, após o equilíbrio, se posicionarão como apresentado na figura a seguir.
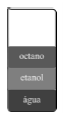
Provas
Desde a chegada dos europeus, os recursos naturais do Brasil têm sido explorados de maneira predatória. Madeira, insumos vegetais, ouro e outros minérios, que, antes, eram embarcados em navios como produtos da colônia, hoje são explorados por empresas e países estrangeiros.
Entre esses recursos naturais, o ferro metálico pode ser obtido de minérios como a siderita (FeCO3) e a hematita (Fe2O3).
Em um processo simplificado, a hematita reage com monóxido de carbono para formar a magnetita (Fe3O4). Em reações sucessivas, o Fe3O4 e o FeO reagem com o CO para produzir o Fe. As equações balanceadas desse processo estão mostradas a seguir, em que !$ \Delta H_I, \, \Delta H_{II}, \,\, e \,\, \Delta H_{III}, !$ representam as variações de entalpia das reações I, II e III, respectivamente.
I - 3 Fe2O3 + CO !$ \rightarrow !$ 2 Fe3O4 + CO2 !$ \Delta H_I !$
II - 2 Fe3O4 + 2 CO !$ \rightarrow !$ 6 FeO + 2 CO2 !$ \Delta H_{II} !$
III - FeO + CO !$ \rightarrow !$ Fe + CO2 !$ \Delta H_{III} !$
Tendo como referência as informações precedentes, julgue o item que se seguem.
Considere que, em um processo de garimpo manual, grãos de ouro tenham sido separados em uma bacia onde fora colocada uma porção de solo e rocha moída e que, por meio da introdução de água corrente e movimentos circulares, a terra, a areia e os sólidos menos densos que o ouro tenham arrastados para fora da bacia. Considere, ainda, que o ouro, mais denso, tenha ficado no fundo desse aparato. Com base nessas informações, é correto afirmar que o processo descrito consiste na separação de uma mistura heterogênea e é classificado como levigação.
Provas
Desde a chegada dos europeus, os recursos naturais do Brasil têm sido explorados de maneira predatória. Madeira, insumos vegetais, ouro e outros minérios, que, antes, eram embarcados em navios como produtos da colônia, hoje são explorados por empresas e países estrangeiros.
Entre esses recursos naturais, o ferro metálico pode ser obtido de minérios como a siderita (FeCO3) e a hematita (Fe2O3).
Em um processo simplificado, a hematita reage com monóxido de carbono para formar a magnetita (Fe3O4). Em reações sucessivas, o Fe3O4 e o FeO reagem com o CO para produzir o Fe. As equações balanceadas desse processo estão mostradas a seguir, em que !$ \Delta H_I, \, \Delta H_{II}, \,\, e \,\, \Delta H_{III}, !$ representam as variações de entalpia das reações I, II e III, respectivamente.
I - 3 Fe2O3 + CO !$ \rightarrow !$ 2 Fe3O4 + CO2 !$ \Delta H_I !$
II - 2 Fe3O4 + 2 CO !$ \rightarrow !$ 6 FeO + 2 CO2 !$ \Delta H_{II} !$
III - FeO + CO !$ \rightarrow !$ Fe + CO2 !$ \Delta H_{III} !$
Tendo como referência as informações precedentes, julgue o item que se seguem.
O ânion do composto da siderita tem geometria molecular tetraédrica.
Provas
Desde a chegada dos europeus, os recursos naturais do Brasil têm sido explorados de maneira predatória. Madeira, insumos vegetais, ouro e outros minérios, que, antes, eram embarcados em navios como produtos da colônia, hoje são explorados por empresas e países estrangeiros.
Entre esses recursos naturais, o ferro metálico pode ser obtido de minérios como a siderita (FeCO3) e a hematita (Fe2O3).
Em um processo simplificado, a hematita reage com monóxido de carbono para formar a magnetita (Fe3O4). Em reações sucessivas, o Fe3O4 e o FeO reagem com o CO para produzir o Fe. As equações balanceadas desse processo estão mostradas a seguir, em que !$ \Delta H_I, \, \Delta H_{II}, \,\, e \,\, \Delta H_{III}, !$ representam as variações de entalpia das reações I, II e III, respectivamente.
I - 3 Fe2O3 + CO !$ \rightarrow !$ 2 Fe3O4 + CO2 !$ \Delta H_I !$
II - 2 Fe3O4 + 2 CO !$ \rightarrow !$ 6 FeO + 2 CO2 !$ \Delta H_{II} !$
III - FeO + CO !$ \rightarrow !$ Fe + CO2 !$ \Delta H_{III} !$
Tendo como referência as informações precedentes, julgue o item que se seguem.
O valor da variação de entalpia molar da reação em relação à hematita, que reage com o monóxido de carbono, produzindo apenas ferro metálico e dióxido de carbono, é !$ 3 \, \Delta H_I, \, + \, 2 \, \Delta H_{II} \, + \, \Delta H_{III}. !$
Provas
Desde a chegada dos europeus, os recursos naturais do Brasil têm sido explorados de maneira predatória. Madeira, insumos vegetais, ouro e outros minérios, que, antes, eram embarcados em navios como produtos da colônia, hoje são explorados por empresas e países estrangeiros.
Entre esses recursos naturais, o ferro metálico pode ser obtido de minérios como a siderita (FeCO3) e a hematita (Fe2O3).
Em um processo simplificado, a hematita reage com monóxido de carbono para formar a magnetita (Fe3O4). Em reações sucessivas, o Fe3O4 e o FeO reagem com o CO para produzir o Fe. As equações balanceadas desse processo estão mostradas a seguir, em que !$ \Delta H_I, \, \Delta H_{II}, \,\, e \,\, \Delta H_{III}, !$ representam as variações de entalpia das reações I, II e III, respectivamente.
I - 3 Fe2O3 + CO !$ \rightarrow !$ 2 Fe3O4 + CO2 !$ \Delta H_I !$
II - 2 Fe3O4 + 2 CO !$ \rightarrow !$ 6 FeO + 2 CO2 !$ \Delta H_{II} !$
III - FeO + CO !$ \rightarrow !$ Fe + CO2 !$ \Delta H_{III} !$
Tendo como referência as informações precedentes, julgue o item que se seguem.
Na reação III, há redução do ferro em um processo que envolve a transferência de dois mols de elétrons por mol de FeO.
Provas
Tem-se como exemplo do colonialismo e biopirataria no Brasil o caso do cupuaçu, fruto amazônico de sabor doce e polpa grossa, que serve como fonte de alimento tanto para as populações indígenas quanto para os animais que vivem na região. O cupuaçu é rico em substâncias importantes para a saúde, como fósforo e vitaminas B1 (tiamina), B2 (riboflavina) e B5 (ácido pantotênico). Após uma empresa estrangeira registrar o nome cupuaçu como a Cupuacu International Inc., todos os produtores brasileiros eram obrigados a pagar royalties a essa empresa, sempre que exportassem produtos à base do fruto amazônico. Graças à repercussão desse caso, as ONGs, junto à opinião pública, conseguiram pressionar o escritório de patentes estrangeiro para cancelar o registro da marca “cupuaçu”.
Internet: <internacionaldaamazonia.com/> (com adaptações).
|
substância |
fórmula estrutural |
|
tiamina |
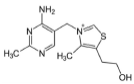 |
|
riboflavina |
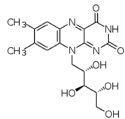 |
|
ácido pantotênico |
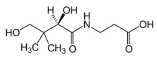 |
A partir do texto e das fórmulas estruturais mostradas na tabela precedente, julgue o próximo item.
Considerando-se o poli(tereftalato de etileno), um polímero de condensação obtido pela esterificação de um monômero com o etilenoglicol, e as fórmulas moleculares constantes da tabela a seguir, é correto afirmar que o monômero que reage com o etilenoglicol, para formar o poli(tereftalato de etileno), é o ácido benzoico.
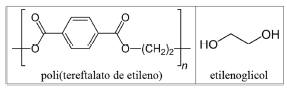
Provas
Caderno Container