Foram encontradas 13.432 questões.
Um analista utilizou para a determinação de Fe3+ uma solução de Mg-EDTA. Em uma primeira etapa, ocorre a seguinte reação:
Fe3+ + MgY2- → FeY- + Mg2+
Posteriormente, os íons Mg2+ são titulados com solução padrão de EDTA. Assinale a opção que apresenta o nome correto do procedimento adotado para essa titulação com EDTA.
Provas
As curvas de titulação de neutralização nos apresentam o comportamento do sistema ao longo do procedimento. As características dos ácidos e das bases nos dão indícios do formato que será obtido na curva de titulação. Considere a figura abaixo (pH versus volume de base adicionado, Vb) representando duas titulações de dois diferentes ácidos monopróticos de mesma concentração molar, sujeitos à neutralização com uma solução de hidróxido de sódio 0,5M.
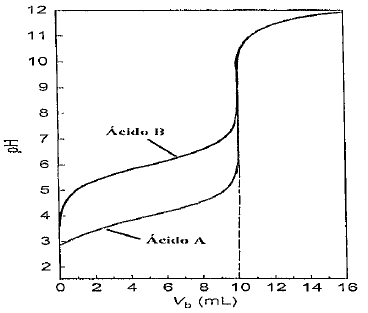
Sabendo que foram utilizados 20ml de ácido em cada titulação, assinale a opção que apresenta a concentração molar dos ácidos titulados e a sua força.
Provas
As análises químicas devem fornecer resultados o mais próximo possível da realidade. Apesar disso, interferências distanciam a resposta analítica do resultado verdadeiro. Alguns erros podem ser reduzidos conforme alguns procedimentos. Com base nisso, analise as afirmativas abaixo.
I- A precisão de um resultado analítico pode ser estabelecida por meio de métodos de análise independentes.
II- A determinação do branco de uma amostra equivale a realizar a análise nas mesmas condições experimentais, porém sem a presença da substância de interesse.
III- A calibração de instrumentos reduz erros aleatórios da análise.
Assinale a opção correta.
Provas
A espectrofotometria é a denominação dada para qualquer técnica que utilize luz para a medição das concentrações das espécies químicas. A Lei de Lambert-Beer estabelece uma relação importante para o cálculo da concentração de soluções diluídas. Uma alíquota de 5 mL de uma solução concentrada foi diluída a 50 mL para a análise em espectrofotômetro, e a absorbância medida na análise foi de 0,700 em uma cubeta de 1,00 cm de caminho ótico. Sabendo que, no comprimento de onda utilizado, a absortividade molar é 2000 M-1 .cm-1 e a absorbância medida no branco da análise foi de 0,050, qual é a concentração da solução concentrada em mM?
Provas
Na análise quantitativa é fundamental o conhecimento correto das concentrações das substâncias utilizadas nos procedimentos. As soluções de referência, denominadas padrões, são utilizadas para caracterizar as amostras. Os padrões primários são obtidos diretamente por meio da pesagem das substâncias secas.
Assim, assinale a opção que NÃO apresenta um padrão primário.
Provas
Três metodologias analíticas foram avaliadas por um analista para a determinação da concentração de um analito. Foi utilizada uma solução com concentração conhecida de 7,50 g/L, e os resultados das repetições das análises para cada metodologia estão apresentados na seguinte tabela:
| Metodologia | Resultados (g/L) | |||
| A | 7,12 | 7,51 | 7,72 | 7,42 |
| B | 7,62 | 7,61 | 7,67 | 7,65 |
| C | 7,40 | 7,63 | 7,45 | 7,56 |
Com base nesses resultados, o analista pode concluir que:
Provas
Sabe-se que dois compostos A e B reagem em solução de acordo com a estequiometria A + B → C + D, que segue uma cinética de primeira ordem tanto em relação a A quanto a B, com velocidade específica de reação k = 10-3 L mol-1 s-1. Em um recipiente, são adicionados 2 mols de cada um dos reagentes e um solvente adequado até completar 1 L de solução. Considerando que A é totalmente solúvel e B tem uma solubilidade igual a 0,1 mol L-1, obtenha a taxa de reação (!$ v !$ em mol L-1 s-1) em função da conversão de A, dada por X = (2-nA) /2 (onde nA é o número de mols de A em um dado instante).
Provas
Seja a reação !$ A(g) \rightleftharpoons 2B(g) !$, a 298 K e 1 atm, com !$ \Delta G^0_r = 0 !$, sendo A e B gases ideais. Considere as seguintes afirmativas.
I. No equilíbrio, o valor da pressão parcial de A é igual ao quadrado do valor da pressão parcial de B, para qualquer temperatura.
II. Um aumento na pressão parcial de A, a partir da situação de equilíbrio, causará o deslocamento da reação para a direita.
III. Se a reação direta for exotérmica, um aumento da temperatura da reação, favorecerá a formação de produto.
Está(ão) correta(s) a(s) afirmativa(s):
Provas
Considere
| Substância | Energia Livre de Gibbs padrão de Formação (kJ.mol-1), a 25 ºC |
| Benzeno (líquido) | +124 |
| Benzeno (gasoso) | +129 |
Dados:
• R=0,08 atm.L/ K.mol = 8,3 J/ K.mol = 62,3 mmHg.L/ K.mol
A pressão de vapor do benzeno em atm, a temperatura de 298 K, é aproximadamente:
Provas
A validade de um resultado analítico depende do conhecimento da quantidade de um dos reagentes usados. Assinale a alternativa correta.
Provas
Caderno Container