Foram encontradas 13.432 questões.
Bebidas podem ser refrigeradas de modo mais rápido utilizando-se caixas de isopor contendo gelo e um pouco de sal grosso comercial. Nesse processo ocorre o derretimento do gelo com consequente formação de líquido e resfriamento das bebidas. Uma interpretação equivocada, baseada no senso comum, relaciona esse efeito à grande capacidade do sal grosso de remover
calor do gelo.
Do ponto de vista científico, o resfriamento rápido ocorre em rezão da
Provas
Questão presente nas seguintes provas
Na produção industrial dos comercialmente chamados leites “sem lactose”, o leite integral é aquecido a altas temperaturas. Após o resfriamento, adiciona-se ao leite a enzima lactase. Com esse processo, o produto gera menos desconforto aos intolerantes à lactose, que é o carboidrato presente no leite integral.
Na fabricação do produto, descrita no texto, aguardar o resfriamento do leite tem a finalidade de evitar o seguinte processo em relação à lactase:
Provas
Questão presente nas seguintes provas
Estudos relacionados ao efeito estufa mostram que os efeitos do aumento do CO2 variam muito entre as espécies vegetais, podendo ocorrer aumento na biomassa e melhoria quanto à eficiência no uso da água pelas plantas. A elevação da temperatura, entretanto, pode ser um fenômeno devastador para as plantas, podendo, inclusive, comprometer totalmente as colheitas. Esse é um dos aspectos mais preocupantes no contexto de mudanças climáticas, por afetar diretamente a disponibilidade de alimentos e a segurança alimentar da humanidade.
Disponível em: http://www.cienciahoje.org.br.
Acesso em: 4 nov. 2018 (adaptado).
O referido aumento na biomassa devido ao efeito estufa está relacionado ao aumento da
Provas
Questão presente nas seguintes provas
Apresentam os mesmos pares de valores, para as propriedades coligativas de cada substância, soluções aquosas 1 mol/L de
Provas
Questão presente nas seguintes provas
A cinética química é um importante estudo das reações químicas, capaz de determinar a velocidade com que elas ocorrem, ou seja, a variação da quantidade de reagentes e produtos em certo período de tempo. Em relação à velocidade de uma reação, analise as afirmativas a seguir:
I. A energia de ativação de uma reação é a energia máxima necessária para que ela possa ocorrer.
II. Para reações que envolvam reagentes gasosos, quanto maior a pressão do reator, maior será a velocidade da reação.
III. Quanto maior a energia de ativação, mais rápida será a reação.
IV. O catalisador de uma reação possui a função de diminuir a energia de ativação da reação. Porém, normalmente é uma substância com alto custo e que ao final da reação tem a sua massa diminuída.
V. Em uma reação com reagentes em diferentes fases, quanto maior for a superfície de contato do reagente sólido, mais rápida será a reação.
Estão corretas as afirmativas:
Provas
Questão presente nas seguintes provas
Admita que uma solução aquosa 0,0400 molar de ácido tricloroacético congele a −0,1395 ºC. Considere, ainda, que a constante de abaixamento do ponto de congelamento !$ (K_c) !$ da água seja 1,860 ºC.!$ kg.mol^{−1} !$ e que 1,00 L de solução contenha 1,00 kg de solvente. O valor da constante de dissociação !$ (K_a) !$ do ácido tricloroacético será:
Provas
Questão presente nas seguintes provas
Uma amostra sólida, sem cavidades ou poros, poderia ser constituída por um dos seguintes materiais metálicos: alumínio, bronze, chumbo, ferro ou titânio. Para identificá-la, utilizou-se uma balança, um recipiente de volume constante e água. Efetuaram-se as seguintes operações: 1) pesou-se a amostra; 2) pesou-se o recipiente completamente cheio de água; 3) colocou-se a amostra no recipiente vazio, completando seu volume com água e determinou-se a massa desse conjunto. Os resultados obtidos foram os seguintes:
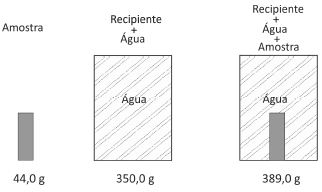
Note e adote:
Densidades (g/cm3):
água = 1,0; alumínio = 2,7; bronze = 8,8;
chumbo = 11,3; ferro = 7,9; titânio = 4,5.
Densidades (g/cm3):
água = 1,0; alumínio = 2,7; bronze = 8,8;
chumbo = 11,3; ferro = 7,9; titânio = 4,5.
Dadas as densidades da água e dos metais, pode-se concluir que a amostra desconhecida é constituída de
Provas
Questão presente nas seguintes provas
Usando um densímetro cuja menor divisão da escala, isto é, a diferença entre duas marcações consecutivas, é de !$ 5,0 \times 10^{-2} \, g \, cm^{-3} !$, um estudante realizou um teste de densidade: colocou este instrumento na água pura e observou que ele atingiu o repouso na posição mostrada.
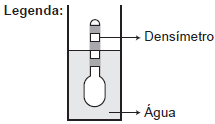
Em dois outros recipientes A e B contendo 2 litros de água pura, em cada um, ele adicionou 100 g e 200 g de NaCI, respectivamente.
Quando o cloreto de sódio é adicionado à água pura ocorre sua dissociação formando os íons !$ Na^+ !$ e !$ Cl^- !$. Considere que esses íons ocupam os espaços intermoleculares na solução.
Nestes recipientes, a posição de equilíbrio do densímetro está representada em:
Provas
Questão presente nas seguintes provas
A glicose é um dos carboidratos mais importantes presentes na biologia. Em hospitais, é comum a utilização de soluções de glicose para o tratamento de desidratação, hipoglicemia e como veículo de medicações compatíveis.
Quando uma solução é preparada a partir da adição de 18 g de glicose a 100g de água, qual é a variação da temperatura de ebulição da água?
Dados: massa molecular da glicose = 180 g.mol-1 e constante ebulioscópica (Ke) da água = 0,52°C.molal-1
Provas
Questão presente nas seguintes provas
Suponha que a decomposição de uma certa substância gasosa seja irreversível e tenha velocidade igual a 0,84 mol/(L.min) (mol por litro por minuto) quando a concentração do gás é de 0,7 mol/L (mol por litro). Quanto aos valores da constante de velocidade para quando a reação for de terceira e primeira ordem, respectivamente, assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container