Foram encontradas 13.432 questões.
O monóxido de carbono, também conhecido como ligante carbonil, apresenta o seguinte diagrama de orbitais moleculares:
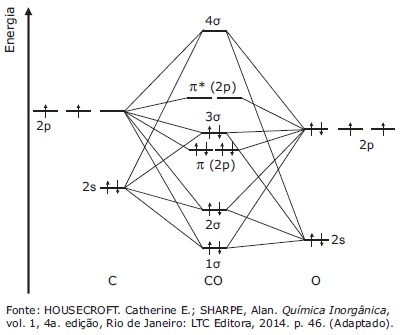
As carbonilas metálicas são compostos organometálicos que apresentam uma rica Química de Coordenação. Podem ser preparadas diretamente da reação do metal com monóxido de carbono, em condições controladas de temperatura e pressão. A ligação entre o centro metálico e o ligante carbonil obedece o modelo da retroligação. Assinale a alternativa que contém a informação correta a respeito da química do ligante CO.
Provas
Provas
Provas
Para responder a questão, utilize o enunciado a seguir.
Diversas aplicações industriais de soluções exploram, simplesmente, os efeitos da presença de partículas de umsoluto num sistema, independentemente da sua natureza. Uma das situações mais familiares é a adição de etilenoglicol (“anticongelante”) ao líquido de arrefecimento dos radiadores dos carros. Isto é necessário, pois o congelamento da água no motor pode provocar danos na estrutura devido à expansão da água (aumento de volume) durante o congelamento. O etilenoglicol diminui a temperatura de congelamento da água (crioscopia), prevenindo o congelamento em dias de temperatura abaixo de 0 °C; este aditivo também aumenta o ponto de ebulição (ebulioscopia) permitindo que o sistema do motor opere acima de 100 ºC sem criar altas pressões; a pressão de vapor também diminui (tonoscopia), e o fluxo de solvente é afetado quando uma solução é separada do solvente puro por uma membrana semipermeável (osmose). Estas são propriedades coligativas de soluções.
A pressão osmótica II corresponde à diferença de pressão entre os dois lados de uma membrana semipermeável que separa o solvente puro de uma solução que contém o mesmo solvente.
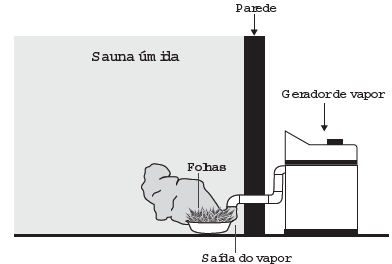
A figura a seguir representa um tubo em forma de U que contém água pura (direita) separada da água do mar (esquerda) por uma membrana semipermeável. Este sistema pode ser usado para recuperar água pura (dessalinizada) a partir da água do mar em locais onde o acesso à primeira é difícil.

Considere que a concentração molar de NaCl na água do mar seja 1/6 mol∙dm-3, que o sistema opere a uma temperatura de 300 K, e que R=0,082 atm∙L∙mol-1 ∙K-1 .
Assinale a alternativa que indique corretamente i) o nome do processo de recuperação de água pura a partir da água do mar e ii) a pressão externa (Pext) que deve ser aplicada para elevar o nível de água pura do lado esquerdo e, assim, obter água dessalinizada para consumo humano.
Provas
As curvas-padrão são comumente utilizadas em procedimentos de determinação da concentração de analitos. Também denominadas de curvas analíticas, elas mostram como a resposta do instrumento (sinal analítico) varia em função da concentração. Para construir uma curva analítica, o técnico utiliza uma série de soluções com concentrações diferentes, porém conhecidas, e, em seguida, registra a variação do sinal analítico. Dentro da faixa dinâmica, a resposta é linear, e, assim, o sinal analítico de uma amostra desconhecida pode ser correlacionado com a sua respectiva concentração. No caso de uma análise por colorimetria ou espectrofotometria, a absorbância e sua relação com a absorção molar permitem determinar a concentração do analito. A exatidão do método é determinada pela análise de um material de referência certificado.
Considere a curva analítica mostrada na figura a seguir que fora incluída num relatório técnico. A linha pontilhada corresponde à regressão linear feita pelo método dos mínimos quadrados cuja equação é indicada no topo da figura.
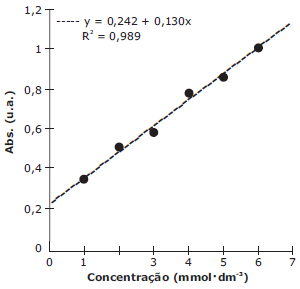
Em relação à figura mostrada, analise as afirmações a seguir.
I → O coeficiente angular corresponde ao valor numérico da absortividade molar da amostra.
II→Supondo uma análise espectrofotométrica, o coeficiente linear indica a presença de um erro sistemático que certamente afetará a exatidão do valor determinado na medida da concentração do analito.
III → A concentração do analito na amostra desconhecida deve estar dentro do limite de linearidade, porém este limite não pode ser determinado a partir da curva mostrada na figura.
Está(ão) correta(s)
Provas
Provas
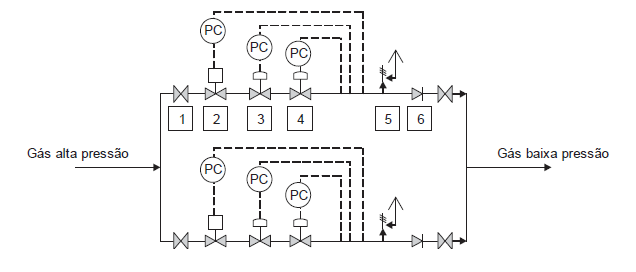 Os equipamentos que compõem esta estação, conforme a sequência numérica, são:
Os equipamentos que compõem esta estação, conforme a sequência numérica, são:Provas
Provas
Provas
A porção gasosa do ar seco, uma mistura de gases, tem ao nível do mar sua composição ponderal composta quase exclusivamente dos gases nitrogênio e oxigênio. Em um recipiente com capacidade de 4,4 L, contendo uma quantidade de matéria (n) de gás nitrogênio a uma temperatura T e pressão de 0,4 atm, é adicionado 0,01 mol de gás oxigênio e, para manter a pressão constante, o recipiente é resfriado a uma temperatura de 9 ºC. Supondo comportamento ideal dos gases, a temperatura aproximada T (em K) antes da adição do oxigênio é
(dado: R = 0,082 atm.L.mol-1.K-1)
Provas
Caderno Container