Foram encontradas 13.432 questões.
Provas
A ressonância magnética nuclear (RMN) é a principal técnica de identificação de compostos orgânicos e está baseada numa propriedade denominada spin nuclear. Informações sobre alguns isótopos importantes são mostradas na tabela a seguir.
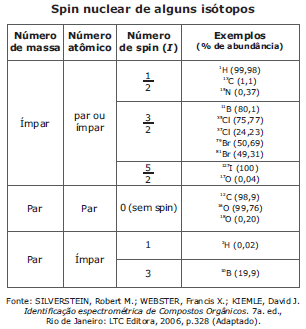
O nuclídeo mais empregado em RMN é o 1H; suas elevadas abundância natural e sensibilidade ao campo magnético tornam a técnica de RMN de 1H rotineira em laboratórios de síntese orgânica. Um bom espectro de RMN de 1H associado a dados complementares de outros métodos instrumentais pode permitir a elucidação estrutural completa de muitos compostos orgânicos. A tabela a seguir lista os deslocamentos químicos típicos exibidos por átomos de hidrogênio vinculados a alguns grupos funcionais importantes.
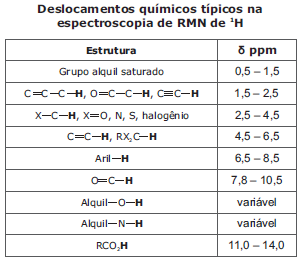
Uma determinada amostra de um composto apresenta os seguintes dados extraídos de um espectro de RMN de 1H:
- multipleto, !$ \delta !$ = 2,32 ppm, 2 H;
- tripleto, !$ \delta !$ = 3,68 ppm, 2 H;
- simpleto, !$ \delta !$ = 3,95 ppm, 1 H;
- multipleto, !$ \delta !$ = 5,75 - 6,35 ppm, 2 H.
O espectro de massas, deste mesmo composto, mostra picos M+ e [M+2]+ numa razão de 3:1.
Assinale a alternativa que contém o composto cuja estrutura é consistente com os dados apresentados.
Provas
Muitos dispositivos eletrônicos modernos utilizam semicondutores. Os semicondutores são materiais que exigem extremo cuidado na sua preparação, de modo que o seu funcionamento adequado só ocorre quando o nível de impurezas é menor do que 1 em 109 (ppt). A obtenção do silício de alta pureza para aplicações tecnológicas é feita através de um processo chamado de refino por zona, no qual um aquecedor elétrico móvel percorre lentamente uma peça cilíndrica do sólido impuro, produzindo fusão em pequenas porções da amostra. Esse processo é repetido até a amostra atingir o grau de pureza desejado. A figura a seguir ilustra o diagrama de fases relacionado à variação da composição do sistema no refino por zona.
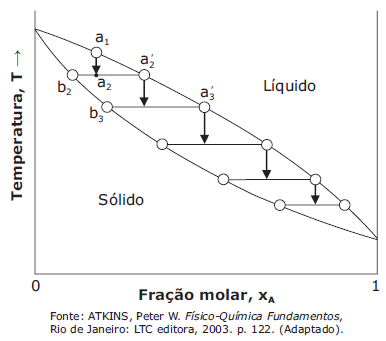
Assinale verdadeira (V) ou falsa (F) nas afirmativas a seguir.
( ) As impurezas são mais solúveis na fase fundida, por isso são arrastadas pela passagem do aquecedor.
( ) No diagrama, a passagem do ponto a1 para o a2 corresponde à formação de um eutético.
( ) O composto A do diagrama é a impureza.
( ) O nivelamento por zona, processo análogo ao do refinamento, pode ser utilizado para introduzir impurezas de modo controlado (dopagem).
A sequência correta é
Provas
Provas
Provas
Provas
Para responder a questão, utilize o enunciado a seguir.
Diversas aplicações industriais de soluções exploram, simplesmente, os efeitos da presença de partículas de umsoluto num sistema, independentemente da sua natureza. Uma das situações mais familiares é a adição de etilenoglicol (“anticongelante”) ao líquido de arrefecimento dos radiadores dos carros. Isto é necessário, pois o congelamento da água no motor pode provocar danos na estrutura devido à expansão da água (aumento de volume) durante o congelamento. O etilenoglicol diminui a temperatura de congelamento da água (crioscopia), prevenindo o congelamento em dias de temperatura abaixo de 0 °C; este aditivo também aumenta o ponto de ebulição (ebulioscopia) permitindo que o sistema do motor opere acima de 100 ºC sem criar altas pressões; a pressão de vapor também diminui (tonoscopia), e o fluxo de solvente é afetado quando uma solução é separada do solvente puro por uma membrana semipermeável (osmose). Estas são propriedades coligativas de soluções.
Um técnico de laboratório de química calculou a temperatura de fusão de uma solução saturada de cloreto de sódio que ele pretendia utilizar como líquido de arrefecimento num banho termostatizado para a manter a temperatura de um sistema constante a –20 ºC.
Considere os dados a seguir.
→Solubilidade do NaCl a 0 ºC=36 g NaCl /100 g H2O
→Solubilidade do KCl a 0 ºC = 28 g KCl /100 g H2O
→ Constante crioscópica de soluções aquosas (Kf) = 2,0 °C∙kg∙mol-1
Agora, assinale a alternativa que representa a conclusão apresentada pelo técnico, assumindo que sua análise tenha sido conduzida de acordo com os fundamentos de crioscopia e propriedades coligativas de soluções.
Provas
Um químico executou a reação do 1-cloro-1-metilciclo-hexano com uma base forte. Ao final da reação, o sólido obtido foi purificado e analisado. O espectro de RMN de 13C composto purificado é mostrado a seguir.
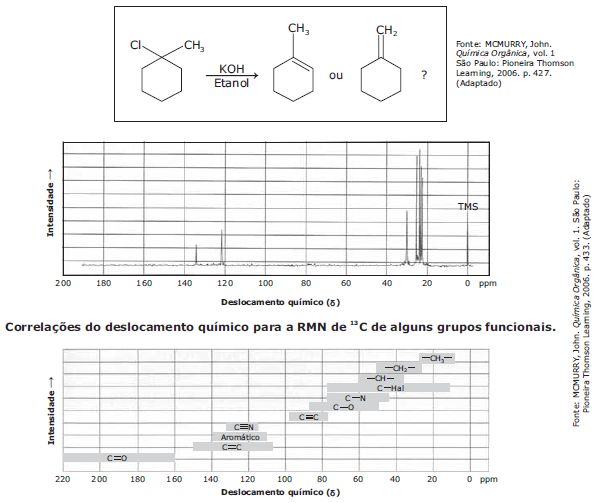
Assinale a alternativa correta.
Provas
Provas
Um químico misturou, acidentalmente, cloreto de potássio sólido com sulfato de potássio sólido. A mistura poderia, entretanto, ainda ser aproveitada em um experimento que ele estava planejando, desde que a percentagem em massa de sulfato de potássio fosse conhecida.
Diante disso, o químico utilizou a técnica de absorção atômica para concluir que a mistura de 6,70 g dos sais continha 3,12 g de potássio.
Assumindo, nesta questão em particular, que as massas atômicas do K, Cl, S e O são, respectivamente, 39 u.m.a., 35 u.m.a, 32 u.m.a. e 16 u.m.a., qual é, aproximadamente, a percentagem em massa do sal sulfato de potássio na mistura?
Provas
Caderno Container