Foram encontradas 13.432 questões.
Sobre fotometria, considere as afirmativas a seguir.
I. Em reações químicas avaliadas por fotometria na faixa visível do espectro luminoso (400 – 750 nm), a transmitância diminui com o aumento da concentração da solução analisada.
II. Em reações químicas avaliadas por fotometria na faixa visível do espectro luminoso (400 – 750 nm), a absorbância aumenta com o aumento da concentração da solução analisada.
III. Reações químicas, em que os produtos resultantes se comportam de acordo com a Lei de Lambert- -Beer, são avaliadas fotometricamente utilizando luz policromática irradiada através da solução analisada.
IV. Quando um produto colorido analisado por fotometria segue a Lei de Lambert-Beer, a relação gráfica (abscissas versus ordenadas) entre a absorção de luz pelas moléculas da solução e a sua respectiva concentração é demonstrada por uma reta que não passa pela origem do gráfico.
Assinale a alternativa correta.
Provas
Uma amostra de água potável foi submetida ao ensaio de cromo por absorção atômica. 100,0 mL de amostra foram tratados em um sistema de extração e pré-concentração do analito, sendo este recuperado a partir da eluição do sistema com solução ácida concentrada. O volume final da solução contendo o analito foi de 5,00 mL. Esta solução foi finalmente submetida ao ensaio de absorção atômica. A absorvância da solução foi de 0,50.
Dados: Curva Analítica de Cromo por Absorção Atômica.
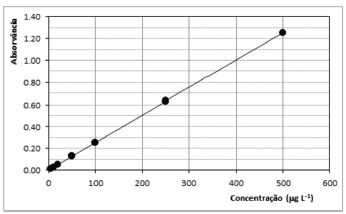
A concentração de cromo na amostra, em μg.L-1, é:
Provas
Para a determinação de chumbo em uma amostra de água subterrânea foi adotada a técnica potenciometria usando um eletrodo de íon seletivo. A curva analítica se mostrou linear para concentrações de chumbo entre 1,00x10–5 até 1,00x10–1 mol.L–1 , com coeficiente angular de 30 mV dec–1 . O potencial padrão do eletrodo, obtido por extrapolação, foi de 340 mV. O potencial apresentado pela amostra foi de 250 mV. A concentração de chumbo na amostra, em mol.L–1, é:
Provas
Uma solução padrão de β-caroteno em éter de petróleo com concentração 1,54 x 10–4 mol.L–1 apresentou no ultravioleta visível, absorbância igual a 0,400u.a. em comprimento de onda 450 nm em uma cubeta de 1 cm. Neste mesmo comprimento de onda, uma outra solução de β-caroteno em éter de petróleo com concentração desconhecida foi analisada. Nas mesmas condições de análise, a solução desconhecida apresentou absorbância igual a 0,850u.a. Nessas condições as amostras obedecem à lei de Beer. A concentração (em mol.L–1) da solução de concentração desconhecida de β-caroteno, nas condições da análise é igual a:
Provas
Na gravimetria por precipitação, o analito é convertido em um composto pouco solúvel. Após tratamento adequado, o composto final é separado e pesado. As relações estequiométricas definidas entre o composto final e o analito permitem a quantificação deste na amostra. Avalie se, para que esse método possa ser aplicado, o composto final obtido deve:
I. apresentar a composição química definida;
II. ter alta pureza ao precipitar;
III. deve ser filtrável apenas através de papel de filtro qualitativo.
Assinale a alternativa correta:
Provas
O teor de cobre em amostra de latão foi determinado por volumetria. 0,15g de amostra foi tratada com HNO3 à quente, até completa dissolução. Após resfriamento, adicionou-se soluções de H2SO4 e de H3PO4 e 10 mL de solução de iodeto de potássio 40%. Titulou-se a solução obtida com uma solução padrão 0,1 mol.L-1 de tiossulfato de sódio até aparecimento de coloração amarelo claro. Então se adicionou 3 mL de solução de amido (1%) e procedeu-se a titulação até desaparecimento da coloração azul por completo. O volume gasto de titulante foi 16,5 mL. O teor de cobre na amostra é:
Provas
Na determinação de ferro por dicromatometria, 10,00 mL de amostra devidamente tratada foram colocados em um erlenmeyer. Adicionou-se ao erlenmeyer 35 mL de água destilada, 5 mL de H3PO4 85% e gotas de difenilamina sulfonato de sódio 0,2%. Essa mistura foi titulada contra solução padrão de dicromato de potássio 0,020 mol.L-1, consumindo 5,00 mL de titulante.
A concentração de ferro na amostra, em mol.L-1, é:
Provas
Uma amostra de água contaminada com uma fração de petróleo foi submetida ao procedimento de extração líquidolíquido, usando diclorometano como solvente, para extrair a contaminação orgânica. A fração orgânica foi concentrada e analisada por cromatografia gasosa. No procedimento de extração, é sempre mais eficiente:
Provas
A determinação da viscosidade de soluções de polímeros é muito usada para estimar a massa molecular média do polímero. A maneira mais comum, mas não a única, é se medir o tempo de escoamento do solvente (t0) e o tempo de escoamento da solução (t) pelo mesmo capilar (na mesma temperatura). Considerando a medida da viscosidade de soluções poliméricas, avalie se as afirmativas a seguir são falsas (F) ou verdadeiras (V):
- Quanto maior o tempo de escoamento da solução através do capilar, menor a viscosidade da solução.
- O tempo de escoamento da solução contendo o polímero deve ser menor que o tempo de escoamento do solvente puro.
- Quanto maior a massa molecular do polímero, maior será a viscosidade da solução.
As afirmativas são respectivamente:
Provas
Laboratórios de ensaios químicos e físico-químicos devem dispor de formulários específicos, ou outra sistemática padronizada, para registrar os dados brutos gerados nos ensaios e calibrações, com campos para o registro das informações suficientes para o desenvolvimento do resultado do ensaio. Além disso, os registros devem permitir a identificação dos fatores que afetam a incerteza e a rastreabilidade do ensaio. Considere um formulário específico de uma análise de teor de ferro por técnica volumétrica. Alguns dados brutos fundamentais para o desenvolvimento do resultado analítico são:
Provas
Caderno Container