Foram encontradas 13.430 questões.
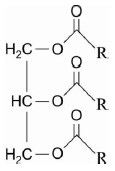
O óleo de macaúba tem despertado grande interesse comercial devido à sua aplicabilidade nas indústrias farmacêutica, alimentícia e de biocombustíveis. Esse óleo é formado por moléculas de triglicerídeos, conforme figura acima, em que R representa cadeias hidrocarbônicas que podem ser iguais ou não entre si. Um dos métodos de caracterização das propriedades físicoquímicas de um óleo vegetal é o índice de saponificação, que consiste na quantidade de hidróxido de potássio necessária para reagir, por saponificação, com 1 grama desse óleo. A reação de saponificação do óleo de macaúba forma, principalmente, os sais de ácido láurico e de ácido oleico, ambos ácidos de fórmula geral RCOOH. Para o ácido láurico, R consiste em uma cadeia aberta saturada de 11 átomos de carbono e, para o ácido oleico, em uma cadeia aberta de 17 átomos de carbono com uma insaturação.
Tendo como referência as informações acima, julgue o item a seguir.
Considere que a análise das cinzas geradas pela queima da casca do fruto de macaúba tenha evidenciado a presença de 0,040 g de óxido de sódio e 0,044 g de óxido de magnésio. Nesse caso, a massa de sódio presente na casca analisada é superior à massa de magnésio.
Provas
|
componente |
fórmula molecular |
massa molar (g/mol) |
porcentagem |
| água | H2O | 18,0 | 20,0 |
| frutose | C6H12O6 | 180,0 | 38,0 |
| glicose | C6H12O6 | 180,0 | 32,0 |
| sacarose | C12H22O11 | 342,0 | 4,0 |
A tabela acima apresenta a porcentagem, em massa, dos componentes mais abundantes em uma amostra de mel e suas respectivas massas molares. Além desses, foram identificados outros componentes como o ácido metanoico e o ácido etanoico. Considerando essas informações, julgue o item a seguir.
A acidez dessa amostra de mel pode ser determinada pela titulação, em presença de um indicador ácido-base, com ácido clorídrico diluído, da solução formada pela dissolução do mel em água.
Provas
|
componente |
fórmula molecular |
massa molar (g/mol) |
porcentagem |
| água | H2O | 18,0 | 20,0 |
| frutose | C6H12O6 | 180,0 | 38,0 |
| glicose | C6H12O6 | 180,0 | 32,0 |
| sacarose | C12H22O11 | 342,0 | 4,0 |
A tabela acima apresenta a porcentagem, em massa, dos componentes mais abundantes em uma amostra de mel e suas respectivas massas molares. Além desses, foram identificados outros componentes como o ácido metanoico e o ácido etanoico. Considerando essas informações, julgue o item a seguir.
Entre os compostos apresentados na tabela, a água é o que se encontra em maior fração de quantidade de matéria.
Provas
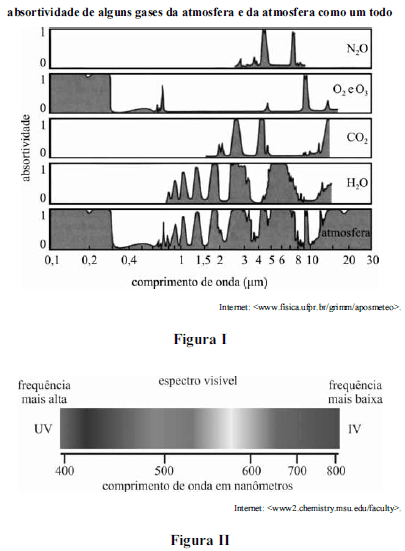
A figura I, acima, apresenta gráficos representativos da absortividade de alguns gases da atmosfera e da atmosfera como um todo, enquanto a figura II representa o espectro na faixa de luz visível. Tendo como base essas figuras e considerando o número de Avogadro igual a 6 x 1023 e a velocidade da luz igual a 3 x 108 m/s, julgue o item a seguir.
A figura II poderia corretamente representar o espectro de um átomo ou molécula.
Provas

A figura I, acima, apresenta gráficos representativos da absortividade de alguns gases da atmosfera e da atmosfera como um todo, enquanto a figura II representa o espectro na faixa de luz visível. Tendo como base essas figuras e considerando o número de Avogadro igual a 6 x 1023 e a velocidade da luz igual a 3 x 108 m/s, julgue o item a seguir.
Sabendo-se que, entre 50 km e 110 km acima da superfície da Terra, ocorre o processo de fotodissociação, no qual o oxigênio é dissociado na forma O2(g) + hv → 2O(g), infere-se que esse processo é o principal responsável pela proteção da superfície da Terra contra os raios ultravioletas.
Provas
Uma amostra de NaCl comercial pesando 0,50 g foi dissolvida. À solução resultante, adicionou-se excesso de AgNO3 e o precipitado obtido foi filtrado, lavado e após seco em estufa pesou 1,148 g. [N = 4,00; O = 16,00; Na = 23, Cl = 35,50 e Ag = 108,00]. Determinada em porcentagem, o teor de NaCl, na amostra é:
Provas
Um volume de 50,00 mL de água industrial foi titulado com solução de Na2-EDTA 0,010 mol/L, utilizando-se o indicador EBT e tampão de pH 10. O volume da solução de Na2-EDTA consumido na titulação foi de 35,00 mL. Titulando-se 50,00 mL dessa mesma amostra com a mesma solução de Na2-EDTA, utilizando-se calcon como indicador em pH 12 (adição de solução de NaOH) até o ponto final foram consumidos 19,50 mL da solução titulante. [C = 12,00; O = 16,00; Mg = 24,00 e Ca = 40,00]. A dureza total da amostra expressa como mg/L de CaCO3 e de MgCO3 na amostra são respectivamente:
Provas
Uma amostra de um efluente doméstico (biossólido) pesando 0,50 g foi digerido e alcalinizado com excesso de solução de NaOH. Após a destilação, a amônia (NH3) liberada foi recolhida em 20,00 mL de solução de H2SO4 0,05 mol/L. A titulação do excesso da solução de H2SO4 utilizando solução de NaOH 0,10 mol/L na presença do indicador vermelho de metila consumiu 5,00 mL da solução alcalina. [H = 1,00; N = 14,00; O = 16,00; Na = 23,00 e S = 32,00;]. O teor de nitrogênio total na amostra, expresso em porcentagem, é:
Provas
O oxigênio dissolvido nas águas naturais é imprescindível para a vida aquática. O método e os reagentes necessários para a sua determinação quantitativa estão indicados na alternativa
Provas
O estado do Pará possui as maiores reservas de minério de ferro do planeta. O seu grau de pureza pode ser avaliado usando-se o método dicromatométrico representado pela seguinte equação química:
6Fe2+ + Cr2O72- + 14H+ → 2Cr2+ + 6Fe3+ + 7H2O
Uma amostra desse minério pesando 0,56 g consumiu 40,00 mL de solução de K2Cr2O7 0,10 N para sua titulação. [H = 1,00; O = 16,00; K = 39,00; Cr = 52,00; Fe = 56,00]. Ao determinar em porcentagem(%) teor de ferro na amostra, o resultado encontrado é
Provas
Caderno Container